套细胞淋巴瘤的诊断和治疗:英国血液学会指南
时间:2023-11-03 20:42:50 热度:37.1℃ 作者:网络
套细胞淋巴瘤诊疗指南
《British Journal of Haematology》近日发表英国血液学会(BSH)指南委员会的套细胞淋巴瘤(MCL)诊疗指南,题目为“Diagnosis and management of mantle cell lymphoma: A British Society for Haematology Guideline”,旨在为医疗保健专业人员提供套细胞淋巴瘤患者诊断和治疗的明确指导。
现整理重点内容供参考(治疗部分的研究过多,因此主要整理指南建议),水平有限,如有错误请谅解。

治疗前评估
组织病理学评估
套细胞淋巴瘤细胞起源具有异质性,对应于初级淋巴滤泡和次级淋巴滤泡外套膜区的成熟 B 细胞亚群。大多数病例为生发中心前起源(pregerminal in origin),其特征为很少/无免疫球蛋白重链可变区 (IGHV) 基因体细胞突变;约15%-20%为生发中心后起源(postgerminal centre in origin),与较高的体细胞 IGHV 突变负荷相关。经典型 MCL 累及淋巴结和淋巴结外部位,包括肝脏、脾脏和胃肠道 (GI)。惰性和侵袭性变异型具有非淋巴结白血病形式。
淋巴结结构特征包括经典型、母细胞样、多形性、边缘区样和小细胞类型。母细胞样和多形性类型与较差的生存率相关。TP53基因畸变是免疫化疗反应差、早期疾病进展和死亡率的最强预测因子。
淋巴结和骨髓 (BM) 组织应进行组织形态学、免疫表型和遗传分析(表1)。如果免疫组织化学显示 MCL 的免疫表型为细胞周期蛋白 D1 阴性,则应对 CCND1 重排进行荧光原位杂交 (FISH) 检测,如果结果为阴性,则应对 CCND2 和 CCND3 进行进一步检查。常规染色体核型分析的临床价值尚不清楚,应局限于临床试验。
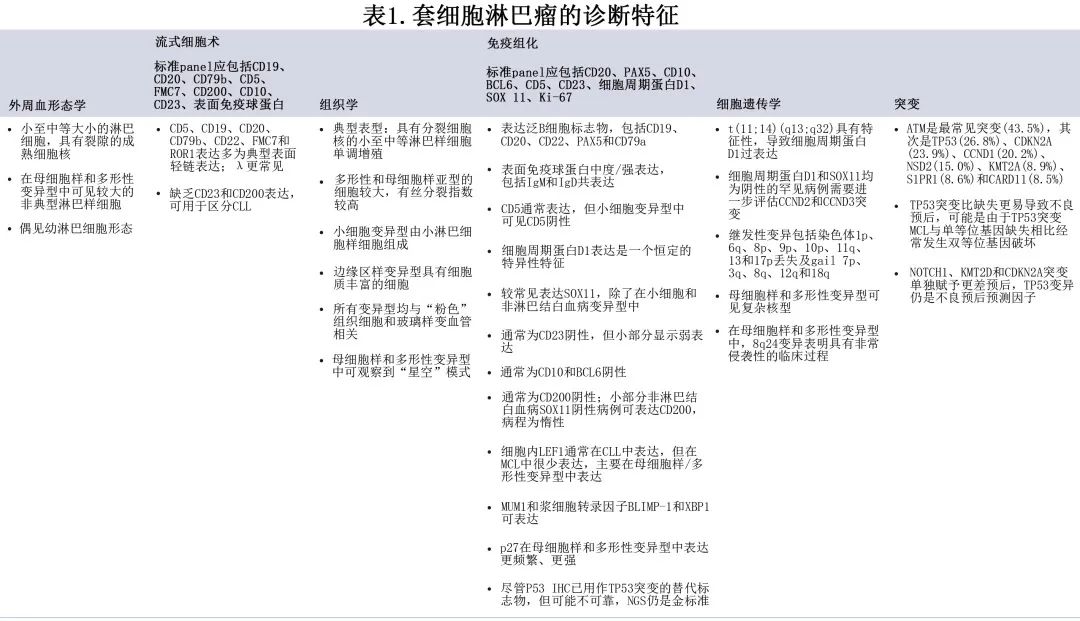
初步临床评估
应评估患者的 B 症状、肝脾肿大和淋巴结肿大(包括 Waldeyer 环)以及神经和 GI 症状。还应评估东部肿瘤协作组体能状态 (ECOG PS) 和是否适合免疫化疗,并确定虚弱程度(Frailty)。血液检查应包括全血细胞计数及血涂片、生化(包括尿酸盐和乳酸脱氢酶 [LDH])、人类免疫缺陷病毒 (HIV) 和乙型肝炎/丙型肝炎病毒学。应考虑超声心动图,并在相关情况下提供生育能力咨询/保存。
虚弱评估
MCL 中没有特定的评估手段,通常外推自针对虚弱的弥漫性大 B 细胞淋巴瘤 (DLBCL) 患者的建议。如果采用强化化疗治疗,虚弱患者的结局较差,因此识别虚弱以优化可逆性问题,并促进关于治疗强度和预后的讨论非常重要。正式的虚弱评估工具优于非正式手段,因为它们更敏感。Geriatric 8筛查工具是一种 3-5分钟的虚弱筛查工具。老年疾病累计评分表(Cumulative Illness Rating Scale for Geriatrics)和血液学老年评估(Geriatric Assessment in Haematology)是专门为血液恶性肿瘤开发的 10-15分钟工具,可以根据具体情况在临床试验中考虑。
分期
现行国际指南建议使用氟脱氧葡萄糖 (FDG)-正电子发射断层扫描/计算机断层扫描 (18F-FDG PET/CT) 对 FDG 高摄取淋巴瘤(包括MCL)进行分期,其依据是 PET/CT 的分期准确性高于传统CT,约20%的分期结果不一致。PET/CT 在检测淋巴结和脾脏受累方面最准确,较高的标准化摄取值 (SUV) 率与更具侵袭性的变异型相对应。PET/CT 检测淋巴结外受累的特异性仍然很高,但灵敏度较低且可变性高;最近的一项荟萃分析报告,与 BM 活检相比,平均灵敏度为36%,与内镜±活检相比,平均灵敏度为39%。基线和中期 PET/CT 的预后作用仍不确定,而诱导结束 PET/CT 评估与达到完全代谢缓解的患者(包括接受自体干细胞移植[ASCT]巩固治疗的患者)的生存结局改善相关。
BM 是最常累及的淋巴结外部位 (50%-90%),由于 PET/CT 的检出率较低,所有病例均应考虑常规 BM 活检±穿刺进行组织学和免疫组化检查;通常足以鉴别浸润,如果仍不确定可辅以多参数流式细胞术。用于微小残留病 (MRD) 评估的 BM 检查正在不断发展,但尚未成为标准实践。
约15%-30%的患者有症状性 GI 受累,但常规内镜检查很少改变治疗策略,应仅考虑用于有症状的患者或在计划放疗时等待确认早期疾病的患者(见“早期MCL”部分)。在这些情况下,仅应考虑上消化道内镜检查,因为 PET/CT 与胃受累内镜检查的一致性较低,但与结直肠疾病的一致性足够高,可避免无症状患者的结肠镜检查。
诊断时 CNS 受累不常见。仅当存在相关神经系统体征或症状时,建议进行腰椎穿刺及脑脊液 (CSF) 分析(细胞离心涂片和免疫表型)和颅脊柱磁共振成像 (MRI)。CSF 细胞形态和免疫表型特征与外周组织相似(表1)。白血病 MCL 的外周血污染可能导致假阳性结果。
预后模型
MCL的预后模型见表2,这些模型通常在接受一线治疗的临床试验患者中得到验证,在常规实践中不应用于影响何时启动一线治疗。独立验证的 MCL 国际预后指数 (MIPI) 可以很容易地应用,可预测 MCL2 研究中接受治疗的患者的总生存期 (OS) 和无进展生存期 (PFS)。
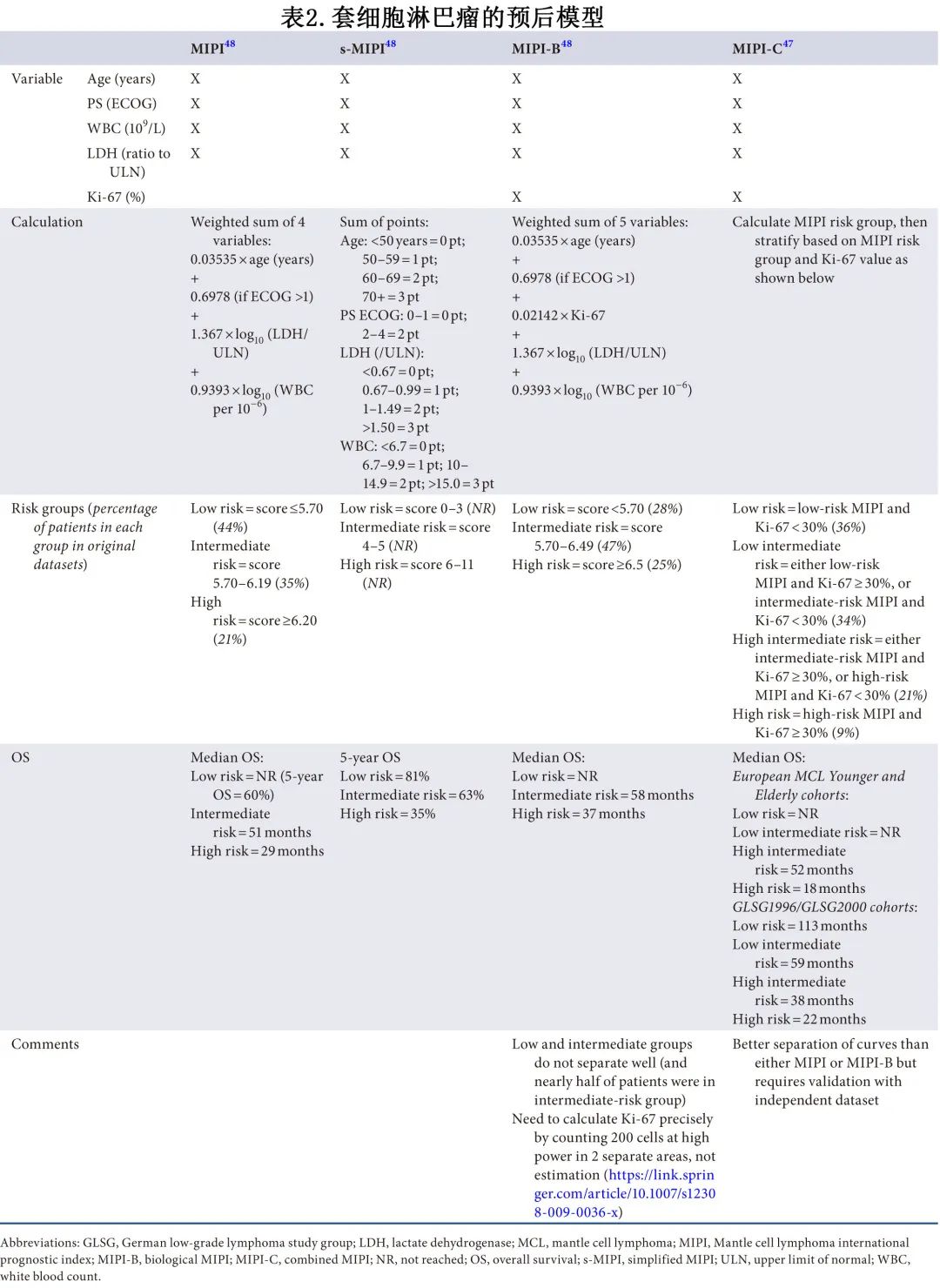
此外还有简化MIPI s-MIPI、生物学MIPI(MIPI-B,纳入Ki-67) 评分和联合MIPI (MIPI-C,MIPI和Ki-67的权重相等)。MIPI-C的区分精度似乎优于MIPI,但需要验证。
建议
患者应接受临床评估、血液检查(包括FBC)、血涂片、常规生化(包括尿酸盐和LDH)、乙型肝炎/丙型肝炎和HIV血清学检查 (1C)。
组织学报告应包括正式的形态学亚型和流式细胞/免疫组化表型 (1C)。
应尽可能在所有MCL活检组'织中报告Ki-67%(或等同物),并至少报告为<30%和≥30%(1B)。
诊断时所有患者进行TP53突变分析(优先于17p缺失的FISH分析)(1B)。
考虑对细胞周期蛋白D1阴性、t11:14阴性、SOX11阳性病例进行CCND2和CCND3检测,这些病例在其他临床病理学上与MCL一致 (2B)。
考虑对潜在虚弱患者进行正式的虚弱评估 (2C)。
应酌情向患者提供生育能力咨询或保存 (1B)。
建议使用18F-FDG-PET/CT或CT对患者进行分期,因为两者都是MCL的有效初始分期模式 (1B)。
如果正式分期需要,进行骨髓活检±穿刺,或评估治疗前血细胞减少,因为PET/CT检测骨髓受累的灵敏度较低 (2B)。
对具有疑似CNS受累的临床特征的患者进行腰椎穿刺和CSF免疫表型分析。建议对这些患者进行颅脊柱MRI(1B)。
患者应使用MIPI或 MIPI-C进行治疗前基线风险分层(1A)。
早期MCL建议
适合局部RT的CT诊断的早期MCL患者,应考虑更广泛的分期,包括PET-CT、骨髓活检和胃镜检查 (2B)。
考虑局部 RT(4-24Gy) 或积极观察早期MCL(2B)。
一线适合ASCT的患者建议
Fit的年轻患者应接受含利妥昔单抗和大剂量阿糖胞苷的一线诱导方案 (1A)。
应向诱导治疗获得客观缓解的患者提供巩固ASCT(1B)。
ASCT后应向患者提供利妥昔单抗维持治疗(皮下或静脉)(1A)。
考虑 TP53 突变患者进行替代巩固策略,最好是在临床试验的背景下(2C)。
在 R-CHOP/R-DHAP 诱导的 R-CHOP 部分提供伊布替尼,以及2年维持治疗代替ASCT(1A)。
不适合移植的MCL的一线治疗建议
对于不适合大剂量阿糖胞苷诱导和 ASCT 的患者,提供 R-化疗联合治疗作为现行标准治疗 (1A)。
对于不适合 ASCT 的既往未经治疗的患者,可提供R-CHOP、R-苯达莫司汀、R-BAC和 VR-CAP 作为选择 (1A)。
在 R-CHOP 诱导后给予利妥昔单抗维持治疗 (1A)。
考虑在 R-苯达莫司汀诱导治疗后进行利妥昔单抗维持治疗 (2B)。
在临床试验之外,勿在 R-BAC 后提供利妥昔单抗维持治疗 (2A)。
虚弱MCL患者的初始治疗建议
考虑由老年科医生审查,并对虚弱MCL患者进行类固醇预治疗 (2B)。
对于适合细胞毒性治疗的虚弱患者,考虑使用 R-苯丁酸氮芥、R-CVP、减毒 R-苯达莫司汀或减毒R-CHOP(2B)。
特点患者考虑最佳支持/姑息治疗(包括放疗)(2B)。
考虑入组靶向新型治疗的前瞻性研究 (2C)。
惰性MCL的管理建议
考虑对未经治疗的无症状、低体积淋巴结病变MCL 患者进行积极观察(2B)。
表现为孤立性脾脏和骨髓/外周血受累的未经治疗的无症状 MCL 患者考虑积极观察 (2B)。
在临床试验的背景下考虑无毒靶向治疗早期干预(2B)。
首次复发的管理建议
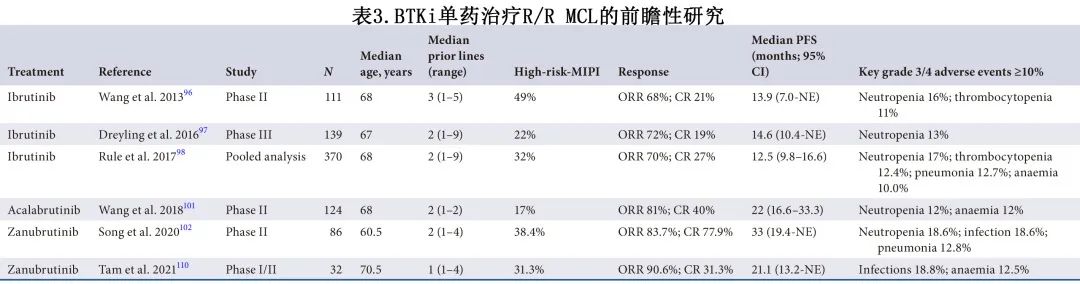
一线免疫化疗后复发的患者应提供共价BTKi(1A)。
在首次复发时提供伊布替尼单药治疗作为标准治疗选择 (1B)。
当可以选择伊布替尼、阿可替尼或泽布替尼时,应根据每种药物的特定毒性特征进行个体化治疗 (1B)。
如果共价 BTKi 已作为连续治疗用于一线治疗,考虑在首次复发时进行临床试验或免疫化疗 (2B)。
CAR-T细胞疗法
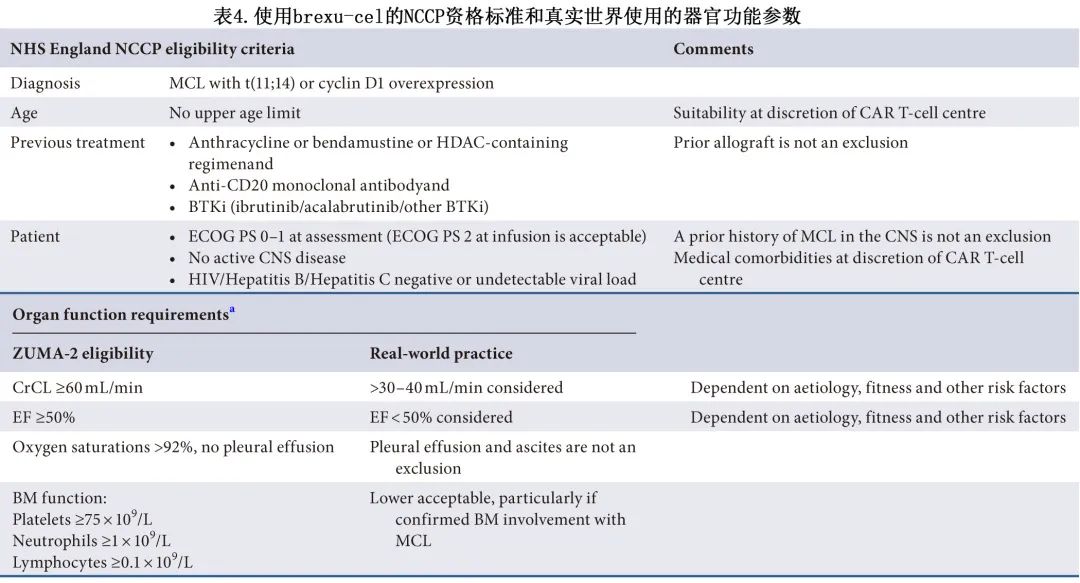
该指南对首次复发的潜在 CAR-T 候选患者提出了基于风险的监测策略,目标是识别早期伊布替尼治疗失败的高危患者,并捕获此类患者的早期难治性或疾病进展 (PD),见图1。
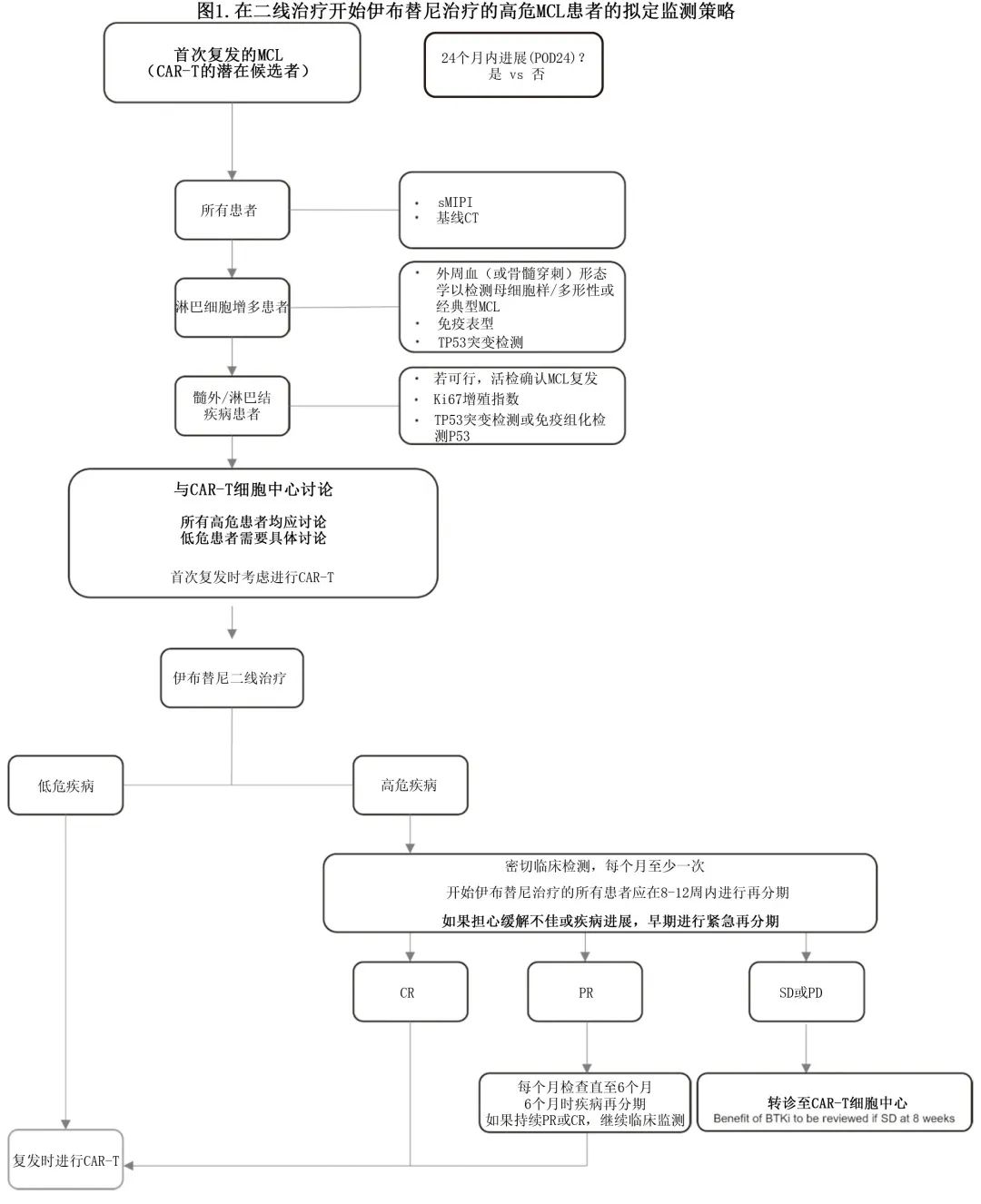
建议
接受含抗 CD20 抗体的免疫化疗和 BTKi 后复发或难治性(包括疾病稳定)的合格 MCL 患者应提供Brexu-cel(1A)。
CAR-T 治疗的潜在候选者应在开始 BTKi 治疗前首次复发时进行风险评估。应与 CAR-T 细胞中心讨论所有高危病例。高危因素包括:母细胞样/多形性形态、Ki67%>50、TP53突变、高危sMIPI、体积>5cm或POD24(1B)。
在潜在候选患者中进行的 BTKi 前评估应包括 CT 再分期、血液/组织活检 sMIPI 评分以确定形态学、Ki67%和 TP53 突变状态(如可行)(1B)。
开始伊布替尼治疗的高危患者应在8-12周内进行 CT 或 PET-CT 再分期(如果担心,可提前)。伊布替尼治疗期间缺乏早期缓解(疾病稳定或进展),应紧急转诊至 CAR-T 细胞中心 (1B)。
共价BTK抑制剂治疗失败且不适合CAR-T或已接受CAR-T的患者的治疗选择建议
建议接受共价 BTKi 治疗后复发的患者继续接受该治疗,直至开始后续治疗,以避免疾病复发的风险 (2C)。
在不适合 CAR-T 或 CAR-T 后的患者中,共价 BTKi 后复发时没有标准的治疗方法。应尽可能考虑临床试验。根据合并症、体能状态和可用选项考虑个体化方法 (2B)。
如果考虑免疫化疗,则可首选R-BAC(2B)。
考虑使用非共价 BTK 抑制剂,如pirtobrutinib(如可选)(2B)。
异基因造血干细胞移植(alloSCT)的当前作用建议
对于免疫化疗、cBTKi和CAR-T失败后有适当供者的适合移植患者,考虑alloSCT(2B)。
CNS MCL的管理建议
不建议在一线 MCL 治疗方案中使用 CNS 穿透药物进行一级 CNS 预防 (2C)。
既往未经 cBTKi 治疗的患者,建议使用伊布替尼治疗CNS 复发 (2C)。
参考文献
Eyre TA, et al.Diagnosis and management of mantle cell lymphoma: A British Society for Haematology Guideline.Br J Haematol . 2023 Oct 25. doi: 10.1111/bjh.19131


