2023 ESMO:肺癌LBA重点研究盘点!
时间:2023-11-01 17:39:22 热度:37.1℃ 作者:网络

前言
2023年欧洲肿瘤内科学会(ESMO)年会将于欧洲中部夏令时间10月20日-24日在西班牙马德里召开,届时将公布众多领域前沿进展和重磅研究成果。
目前ESMO官网在线发布了入选研究的常规摘要和LBA,而LBA研究作为所有研究的重中之重,可能对临床实践产生重大影响。e路新干线小编第一时间整理肺癌药物治疗LBA重点研究,供各位医学同道参考。
1 早期NSCLC
摘要号:LBA 1
与新辅助化疗相比,围术期纳武利尤单抗+新辅助化疗显著改善可切除NSCLC患者EFS
题目:Ⅲ期CheckMate 77T研究:纳武利尤单抗+化疗 vs. 安慰剂+化疗新辅助治疗后手术切除,再行纳武利尤单抗或安慰剂辅助治疗既往未经治可切除Ⅱ-ⅢB期NSCLC
报告人:Tina Cascone
背景
纳武利尤单抗(NIVO)+化疗新辅助治疗相比于化疗使可切除NSCLC患者获益。然而,围术期NIVO +化疗的疗效尚未在Ⅲ期研究中进行评估。在此报告了预先指定的CheckMate 77T研究的期中分析结果,该研究是一项评估NIVO+化疗 vs. 安慰剂+化疗后手术切除,再行NIVO或安慰剂辅助治疗可切除Ⅱ-ⅢB期NSCLC的随机、双盲、Ⅲ期研究。
方法
纳入既往未经治疗的、EGFR/ALK野生型、ECOG PS≤1的可切除ⅡA(>4 cm)-ⅢB(N2)期NSCLC(AJCC v8)成人患者,分层因素为肿瘤组织学、PD-L1表达和疾病分期。患者按照1:1随机分配至NIVO 360 mg Q3W +含铂双药化疗(4周期)后手术,再行NIVO 480 mg Q4W(1年)辅助治疗或安慰剂Q3W +含铂双药化疗(4周期)后手术,再行安慰剂Q4W(1年)。主要终点为EFS(BICR根据RECIST v1.1评估)。次要终点为pCR和MPR(均由BIPR评估)、OS和安全性。
结果
两组间基线特征平衡(NIVO+化疗/NIVO组,n=229;化疗/PBO组,n=232)。在最少15.7个月的随访中,NIVO+化疗/NIVO组与化疗/PBO组相比显著改善了EFS(中位数[95% CI],NR[28.9-NR] vs. 18.4个月[13.6-28.1];HR [97.36% CI],0.58 [0.42-0.81];P=0.00025)。NIVO+化疗/NIVO组与化疗/PBO组相比也提高了pCR率(25.3% vs. 4.7%;OR=6.64 [95% CI,3.40-12.97])和MPR率(35.4% vs. 12.1%;OR=4.01 [2.48-6.49])。NIVO+化疗/NIVO组与化疗/PBO组的最终手术率分别为78%和77%;其中R0切除率分别为89%和90%。在NIVO +化疗/NIVO组和化疗/PBO组中,3-4级治疗相关AE发生率分别为32%和25%;与手术相关AE发生率分别为12%和12%。
结论
CheckMate77T达到其主要终点,在可切除NSCLC患者中,NIVO+化疗新辅助治疗后手术,再行NIVO辅助治疗与化疗/PBO相比具有统计学意义和临床意义的EFS改善。NIVO+化疗/NIVO方案未发现新的安全性信号。
摘要号:LBA 56
KEYNOTE-671研究第二个主要终点OS报阳
题目:KEYNOTE-671研究OS数据:帕博利珠单抗围术期治疗早期NSCLC
报告人:Jonathan D. Spicer
背景
在可切除早期NSCLC的Ⅲ期KEYNOTE-671研究(NCT03425643)预先指定的首次期中分析中,与单独新辅助化疗和切除相比,帕博利珠单抗(pembro)+化疗新辅助治疗后手术切除,再行pembro辅助治疗显著改善了EFS、mPR和pCR,且安全性可控。在此报告了方案指定的第二次期中分析的结果。
方法
可切除Ⅱ期、ⅢA期或ⅢB期患者随机1:1分配至pembro 200 mg(n=397)或安慰剂(n=400)Q3W。患者接受4个周期的新辅助pembro或安慰剂联合以顺铂为基础的化疗和≤13周期的辅助pembro或安慰剂治疗。双主要终点为EFS(从随机分组到局部进展、无法切除的肿瘤、研究者根据RECIST v1.1评估的疾病进展或复发、任何原因死亡)和OS。
结果
从随机化至数据截止日期2023年7月10日,中位时间为36.6个月(范围,18.8-62.0)。当发生254起(31.9%)死亡事件时,pembro组的OS显著改善(HR=0.72 [95% CI 0.56-0.93];P=0.00517)。pembro组的中位OS未达到(NR)(95% CI:NR-NR),而安慰剂组为52.4个月(95% CI:45.7-NR);36个月OS率为71.3% vs. 64.0%。pembro组的EFS持续改善(HR=0.59 [95% CI:0.48-0.72];中位数[95% CI] 47.2个月[32.9-NR] vs. 18.3个月[14.8-22.1];36个月EFS率为54.3% vs. 35.4%)。≥3级治疗相关AE发生率:45.2% vs. 37.8%;导致停止治疗AE发生率:20.2% vs. 9.3%;导致死亡AE发生率:1.0% vs. 0.8%(自首次期中分析以来没有出现新的治疗相关死亡事件)。
结论
在可切除的Ⅱ期、ⅢA期或ⅢB(N2)期NSCLC患者中,与单独新辅助化疗和切除相比,pembro+化疗新辅助治疗后手术切除,再行pembro辅助治疗的OS具有统计学意义和临床意义的改善。在没有新的安全性信号的情况下,KEYNOTE-671研究OS数据改善确立了围术期pembro方案可作为可切除早期NSCLC新的标准治疗。
摘要号:LBA 58
与新辅助化疗相比,替雷利珠单抗+化疗新辅助治疗可切除Ⅱ-ⅢA期NSCLC患者具有临床意义和统计学意义的MPR和pCR改善
题目:Ⅲ期RATIONALE-315研究:替雷利珠单抗+含铂双药化疗新辅助治疗可切除Ⅱ-ⅢA期NSCLC的病理缓解
报告人:岳东升 教授(天津医科大学肿瘤医院)
背景
化疗+抗PD-(L)1单抗新辅助治疗可切除NSCLC显示良好的病理缓解率(即主要病理缓解[MPR]和病理完全缓解[pCR])。Ⅲ期RATIONALE-315研究(NCT04379635)评估了替雷利珠单抗(TIS,抗PD-1单抗)或安慰剂(PBO)+化疗新辅助治疗,然后TIS或PBO辅助治疗可切除Ⅱ-ⅢA期NSCLC患者的疗效和安全性。
方法
纳入标准为既往未经治疗的、可切除、确诊鳞状或非鳞状Ⅱ-ⅢA期NSCLC患者,患者符合含铂双药化疗条件、ECOG PS≤1且无已知EGFR突变(非鳞状)或ALK基因易位(鳞状&非鳞状)。分层因素为组织学、疾病分期和PD-L1表达(≥1% vs. <1%)。患者随机(1:1)分配至3-4个周期的TIS 200 mg IV Q3W或PBO,联合含铂双药化疗后手术,再行8个周期的TIS 400 mg IV Q6W或PBO辅助治疗。主要终点为盲态独立审查委员会(IRC)根据RECIST v1.1评估的完成新辅助治疗后的MPR率和EFS。关键次要终点为pCR率。
结果
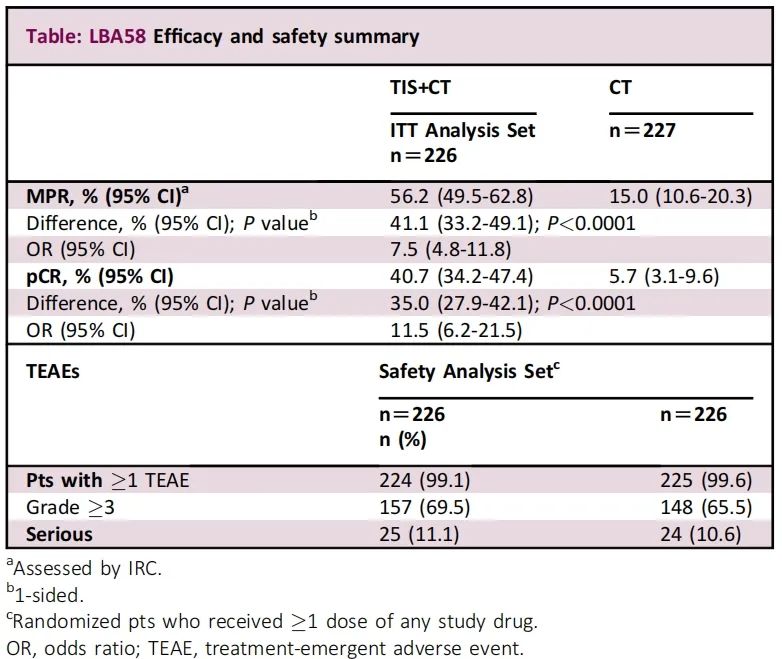
截至2023年2月20日(中位随访时间:16.8个月),453例患者(TIS+化疗组,n=226;化疗组,n=227)被随机分配至意向治疗(ITT)人群,两组基线特征相似。在452例(99.8%;每组n=226)新辅助治疗阶段患者中,421例(92.9%)完成了新辅助治疗 (TIS+化疗组,n=211[93.4%];化疗组,n=210[92.5%])。90例(19.9%)未接受手术(TIS+化疗组,n=36[15.9%];化疗组,n=54[23.8%])。新辅助治疗阶段的疗效和安全性数据见表1;TIS+化疗组与化疗组相比显著提高了MPR和pCR率(P<0.0001)。TIS+化疗不影响手术的可行性。
表1:疗效和安全性结果
结论
与PBO+化疗相比,TIS+化疗新辅助治疗显示MPR和pCR率具有临床意义和统计学意义的改善。TIS+化疗的安全性与单独每种治疗方案已知的安全性一致,并且在可切除Ⅱ-ⅢA期NSCLC患者中是可控的,进一步支持了TIS+化疗可作为该类患者的治疗组合方案。
摘要号:LBA 2
与辅助化疗相比,阿来替尼辅助治疗显著改善可切除ALK+ NSCLC患者DFS
题目:ALINA研究:阿来替尼 vs. 化疗辅助治疗早期ALK+ NSCLC的疗效和安全性
报告人:Ben J. Solomon
背景
对于可切除ALK+ ⅠB-ⅢA期NSCLC患者,术后推荐的治疗方案是含铂化疗,但该方案改善生存有限。在晚期ALK+ NSCLC中,阿来替尼是首选的一线治疗方法。在此报告了ALINA研究(NCT03456076)预先指定的期中分析结果,该研究是一项评估阿来替尼 vs. 化疗辅助治疗完全切除的ALK+ NSCLC患者的有效性和安全性的全球、开放、随机、Ⅲ期研究。
方法
纳入标准为年龄≥18岁、ECOG PS 0/1、完全切除的ALK+ ⅠB(>4 cm)-ⅢA期NSCLC(UICC/AJCC第7版)。患者按照1:1随机分配接受阿来替尼 PO 600 mg BID或含铂化疗 IV,每21天为一个周期,最多4个周期。分层因素为分期(ⅠB期 vs. Ⅱ期 vs. ⅢA期)和种族(亚洲 vs. 非亚洲)。阿来替尼给药最多24个月或直到疾病复发、出现不可耐受毒性或撤回知情。主要终点为研究者评估的DFS,分层检验首先在Ⅱ-ⅢA期人群中进行,然后是ITT人群(ⅠB-ⅢA期)。其他终点包括CNS-DFS、OS和安全性。
结果
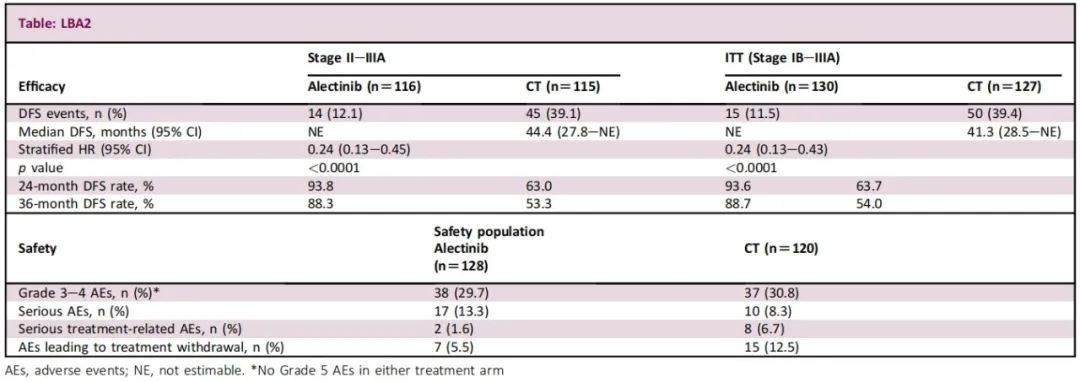
共有257例患者随机接受阿来替尼(n=130)或化疗(n=127)。两组间基线特征总体平衡。至数据截止日期(2023年6月26日),中位随访时间为27.8个月,阿来替尼 vs. 化疗具有显著的DFS获益,Ⅱ-ⅢA期人群:HR=0.24;95% CI:0.13-0.45;ITT人群:HR=0.24;95% CI:0.13-0.43,结果见表2。在ITT人群中观察到有临床意义的CNS-DFS获益(HR=0.22;95% CI:0.08-0.58)。OS数据不成熟。未发现新的安全性信号。
表2:疗效和安全性结果
结论
与化疗相比,阿来替尼是首个能显著改善DFS的ALK抑制剂,为可切除ALK+ NSCLC患者提供了一种有效的新型治疗策略。
2 局部晚期NSCLC
摘要号:LBA 61
sCRT后度伐利尤单抗治疗与cCRT后度伐利尤单抗治疗不可切除Ⅲ期NSCLC患者具有相似的安全性
题目:PACIFIC-6研究的最终分析:序贯放化疗后度伐利尤单抗治疗不可切除Ⅲ期NSCLC
报告人:Marina C. Garassino
背景
在安慰剂对照Ⅲ期PACIFIC研究中,同步放化疗后(cCRT)度伐利尤单抗治疗显著改善了不可切除Ⅲ期NSCLC患者的生存,且安全性可控。由于许多患者不适用于cCRT,Ⅱ期PACIFIC-6研究(NCT03693300)评估了序贯放化疗(sCRT)后度伐利尤单抗治疗的安全性和有效性。期中数据表明,该方案与PACIFIC研究中cCRT后使用度伐利尤单抗具有相似的安全性,初步疗效令人鼓舞。在此报告了PACIFIC-6研究的最终分析。
方法
纳入标准为ECOG PS≤2、含铂sCRT后无进展的不可切除Ⅲ期NSCLC患者,患者接受度伐利尤单抗 1500 mg IV,Q4W,持续24个月或直至进展、出现不可耐受毒性或撤回知情。主要终点(既往报道)为6个月内3/4级可能相关的AE(PRAE)发生率。次要终点包括OS和PFS(研究者评估;RECIST v1.1),采用KM法进行分析。
结果
截至2023年3月20日,共纳入117例患者。大多数患者为PS 1/2(59.8%;PS 1:n=67;PS 2:n=3),年龄≥65岁(65.8%;年龄范围:39-85),ⅢB/ⅢC期NSCLC(63.2%)。几乎所有患者既往/目前存在合并症(98.3%),主要是血管性疾病(59.0%)、呼吸性疾病(53.0%)和代谢性疾病(51.3%)。中位治疗时间为41.0周(范围:4-108)。总体而言,4.3%(95% CI:1.4-9.7)的患者在6个月内出现3/4级PRAE,6.0%的患者在整个研究期间出现3/4级PRAE(1例患者发生导致死亡的PRAE)。肺炎是所有等级(17.1%)和3/4级(1.7%)中最常见的PRAE。27.4%的患者因任何原因AE而停用度伐利尤单抗。进行OS评估患者的中位随访时间为32.6个月(范围:4.4-45.7),中位OS为39.0个月(95% CI:30.6-NC),3年OS率为56.5%(95% CI:46.4-65.5),中位PFS为13.1个月(95% CI:7.4-19.9)。
结论
sCRT后度伐利尤单抗治疗与PACIFIC研究中cCRT后度伐利尤单抗治疗具有相似的安全性,并且在身体状况较差的人群中显示出令人鼓舞的疗效,研究结果支持对不适合进行cCRT的患者使用该方案。
3 转移性NSCLC
摘要号:LBA 67
与单独化疗相比,阿替利珠单抗联合贝伐珠单抗和化疗使靶向治疗进展的EGFR或ALK突变NSCLC患者临床获益
题目:随机、Ⅲ期ATTLAS,KCSG-LU19-04研究:阿替利珠单抗+贝伐珠单抗+化疗治疗EGFR或ALK突变NSCLC
报告人:Myung-Ju Ahn
背景
在具有驱动基因突变的NSCLC治疗中,抗PD-(L)1抗体在酪氨酸激酶抑制剂(TKI)后的作用尚不清楚。这项随机、开放、多中心、Ⅲ期研究评估了阿替利珠单抗联合贝伐珠单抗和化疗在TKI治疗进展的EGFR或ALK突变NSCLC患者中的疗效。
方法
阿替利珠单抗+贝伐珠单抗+紫杉醇+卡铂(ABCP组),随后阿替利珠单抗+贝伐珠单抗维持治疗 vs. 培美曲塞+卡铂或顺铂(PC组),随后培美曲塞维持治疗。主要终点为PFS。
结果
从韩国16个中心共纳入228例EGFR突变(n=215)或ALK易位(n=13)患者,以2:1的比例随机分配至ABCP组(n=154)或PC组(n=74)。中位随访时间为26.1个月(95% CI:24.7-28.2)。ABCP组的ORR高于PC组(69.5% vs. 41.9%,P<0.001)。ABCP组的中位PFS显著优于PC组(8.48个月 vs. 5.62个月,HR=0.62 [0.45-0.86],P=0.004)。PFS获益随着PD-L1表达量的增加而增加,PD-L1≥1%、≥10%和≥50%的HR分别为0.47、0.41和0.24。ABCP组和PC组之间的OS相似(20.63个月 vs. 20.27个月,HR=1.01 [0.69-1.46],P=0.975)。ABCP组的安全性与既往报道一致,没有额外的安全性信号。
结论
本研究是首个证明抗PD-L1抗体联合贝伐珠单抗和化疗使靶向治疗进展的EGFR或ALK突变NSCLC获益的随机Ⅲ期研究。
摘要号:LBA 5
埃万妥单抗+化疗有望成为EGFR Ex20ins晚期NSCLC患者新的标准一线治疗
题目:随机、全球、Ⅲ期PAPILLON研究主要结果:埃万妥单抗+化疗 vs. 化疗一线治疗EGFR 20号外显子插入突变晚期NSCLC
报告人:Nicolas Girard
背景
埃万妥单抗(ami)是一种具有免疫细胞导向活性的EGFR-MET双特异性抗体。ami联合卡铂/培美曲塞在Ⅰ期CHRYSALIS研究中显示了良好的安全性和抗肿瘤活性。PAPILLON研究(NCT04538664)评估了ami+化疗 vs. 化疗一线治疗EGFR 20号外显子插入突变(EGFR Ex20ins)晚期NSCLC。
方法
既往未经治疗的患者按照1:1随机接受ami+化疗或化疗。主要终点为PFS。次要终点包括ORR、首次后续治疗后的PFS(PFS2)、OS和安全性。化疗组在进展时允许交叉到ami单药治疗。
结果
总体而言,308例患者进行随机分组(ami+化疗组:153;化疗组:155),中位年龄分别为61/62岁,女性56/60%,亚洲人64/59%,脑转移史23/23%。中位随访14.9个月,ami+化疗组中位PFS为11.4个月(95% CI:9.8-13.7),化疗组为6.7个月(95% CI:5.6-7.3)(HR=0.40;95% CI:0.30-0.53;P<0.001)。18个月PFS率为31% vs. 3%。ami+化疗在各亚组具有一致的PFS获益。ORR为73%(95% CI:65-80) vs. 47%(95% CI:39-56)(OR=2.97;95% CI:1.84-4.79;P<0.001)。中位PFS2为NE vs. 17.2个月(HR=0.49;95% CI:0.32-0.76;P=0.001)。尽管疾病进展后接受二线ami的患者比例为66%,OS期中分析(33%成熟度)显示ami+化疗与化疗相比具有获益趋势(HR=0.67;95% CI:0.42-1.09;P=0.106)。ami+化疗组最常见的TEAE(≥40%)是中性粒细胞减少症、甲沟炎、皮疹、贫血、输注相关反应和低白蛋白血症,没有新的安全性信号。导致ami停药的治疗相关AE发生率为7%。
结论
在EGFR Ex20ins晚期NSCLC患者中,ami+化疗的PFS优于化疗。安全性与每种药物的安全性一致。PAPILLON研究确立了ami+化疗可作为EGFR Ex20ins晚期NSCLC新的一线标准治疗。
摘要号:LBA 4
与化疗+帕博利珠单抗相比,塞普替尼在晚期RET+ NSCLC患者中具有统计学意义和临床意义的PFS改善
题目:塞普替尼 vs. 化疗+帕博利珠单抗一线治疗RET融合阳性NSCLC的随机Ⅲ期研究
报告人:Herbert Ho Fung Loong
背景
塞普替尼是一种高度选择性和强效脑渗透性RET抑制剂,已被批准用于治疗晚期RET融合阳性(RET+)NSCLC。塞普替尼既往未在随机研究中进行过评估。
方法
LIBRETTO-431(NCT04194944)是一项评估一线塞普替尼vs. 化疗(顺铂/卡铂+培美曲塞)±帕博利珠单抗的随机、开放、Ⅲ期研究。主要终点为BICR评估的PFS,首先在对照组中研究者分层的帕博利珠单抗意向治疗(ITT-pembro)患者中进行检验,然后在ITT人群中进行检验。在ITT-pembro人群中发生98起PFS事件后进行BICR预先指定的期中疗效分析。在对照组进展后允许交叉到塞普替尼组。
结果
共纳入来自23个国家的261例患者。研究组之间的基线特征是平衡的。中位随访约19个月时,塞普替尼组PFS优于对照组,ITT-pembro人群:HR=0.465,95% CI:0.309-0.699;P=0.0002;ITT人群:HR=0.482,95% CI:0.331-0.700;P=0.0001。在ITT-pembro人群中,塞普替尼组中位PFS为24.8个月(95% CI:16.9-NE),而对照组为11.2个月(95% CI:8.8-16.8)。与对照组相比,塞普替尼组ORR、DOR和颅内缓解也有临床意义的改善。塞普替尼组与对照组相比至CNS进展的时间更长(特定原因HR=0.26;95% CI:0.11-0.59;P=0.0006)。塞普替尼组和对照组观察到的不良事件与既往报道基本一致。
结论
与化疗+帕博利珠单抗相比,塞普替尼在晚期RET+ NSCLC中具有统计学意义和临床意义的PFS改善。LIBRETTO-431是首个在生物标志物选择的患者群体中证明靶向治疗的PFS优于化疗+检查点抑制剂的随机研究。这些数据支持晚期RET+ NSCLC患者在诊断和使用塞普替尼一线治疗时进行全面基因组检测。
摘要号:LBA 65
阿达格拉西布+帕博利珠单抗治疗既往未经治的KRAS G12C突变、PD-L1≥50%晚期NSCLC患者显示令人鼓舞的疗效和可控的安全性
题目:KRYSTAL-7研究:阿达格拉西布+帕博利珠单抗治疗既往未经治的KRAS G12C突变晚期NSCLC疗效和安全性
报告人:Marina C. Garassino
背景
阿达格拉西布(ada)是一种不可逆的KRAS G12C抑制剂,具有半衰期长(23小时)、剂量依赖性PK和CNS渗透性等特点。优化的非共价结合亲和力和ada相关的半胱氨酸反应性最小化可以限制肝脏和其他器官部位的脱靶效应。ada+帕博利珠单抗(pembro)初步数据显示了可控的安全性和令人鼓舞的临床活性。在此报告了KRYSTAL-7研究(NCT04613596)中接受ada+pembro治疗的更多患者更新的疗效和安全性数据。
方法
在Ⅱ期KRYSTAL-7研究中,未经治疗的KRAS G12C突变的晚期NSCLC患者同时接受ada 400 mg PO BID+pembro 200 mg IV Q3W。研究目的包括疗效(研究者评估的ORR、DOR、PFS和OS)和安全性。
结果
截至2023年6月19日,148例患者接受了ada+pembro治疗(中位随访8.7个月)。中位年龄为67岁,女性为48%,ECOG PS 0/1为39%/61%。在PD-L1≥50%患者中(中位随访10.1个月),ORR为63%(32/51);DCR为84%;中位DOR为NR(95% CI:12.6-NE);中位PFS为NR(95% CI:8.2-NE)。在所有患者中,94%(139/148)患者发生了任何等级TRAE;55% 3级;9% 4级;1% 5级。TRAE导致4%的患者同时停用ada和pembro(6%单独停用ada,11%单独停用pembro)。无患者因ALT/AST增加或肝脏TRAE而停用两种药物。因肝转氨酶升高,1例患者停用ada,3例患者停用pembro。研究者将会报告额外的疗效和安全性分析。
结论
经过较长时间的随访,ada+pembro治疗PD-L1≥50%患者继续显示出令人鼓舞的初步疗效,且安全性可控。研究结果支持了一项评估ada+pembro vs. pembro治疗既往未经治的KRAS G12C突变和PD-L1≥50% NSCLC患者的3期研究的启动(NCT04613596)。
摘要号:LBA 12
与多西他赛相比,Dato-DXd显著改善了既往经治的晚期/转移性NSCLC患者PFS
题目:随机Ⅲ期TROPION-Lung01研究:datopotamab deruxtecan(Dato-DXd) vs. 多西他赛治疗既往经治晚期/转移性NSCLC
报告人:Aaron E. Lisberg
背景
Dato-DXd是一种新型靶向TROP2的抗体-药物偶联物,目前正在进行的临床研究中应用于多种肿瘤类型。此次为TROPION-Lung01研究(NCT04656652)的首次报告,该研究是一项评估Dato-DXd vs. 多西他赛(DTX)治疗既往经治的、有/无可操作基因突变的晚期/转移性NSCLC患者的随机、全球、开放的Ⅲ期研究。
方法
患者按1:1随机接受Dato-DXd 6 mg/kg或DTX 75 mg/m2 Q3W。双主要终点为PFS(BICR评估)和OS。次要终点包括ORR、DOR和安全性。
结果
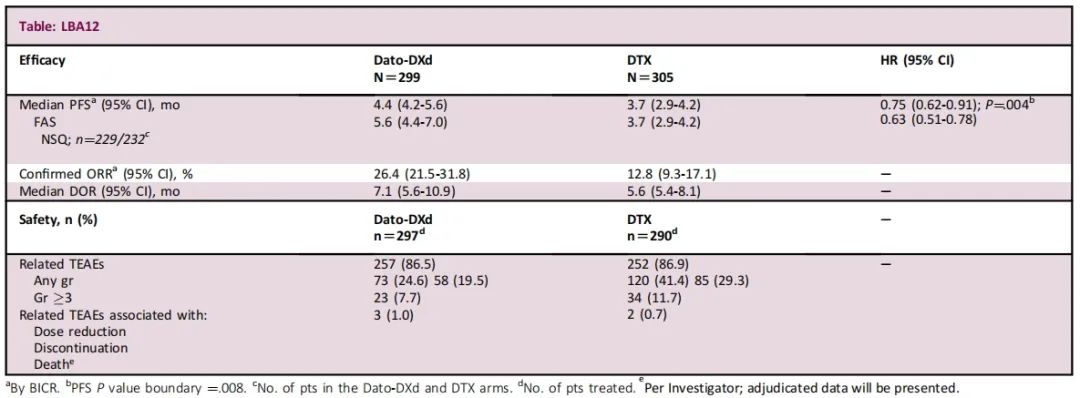
604例患者被纳入全分析集(FAS);43.1%的患者既往接受过≥2次全身治疗。中位年龄为64岁(范围:24-88)。在FAS中,Dato-DXd相比于DTX显著改善了PFS(HR=0.75;95% CI:0.62-0.91;P=0.004;中位数,4.4 vs. 3.7个月)。确认的ORR分别为26.4%(Dato-DXd)和12.8%(DTX),中位DOR分别为7.1和5.6个月。在预先指定的非鳞状组织学亚组中观察到较长的中位PFS(5.6个月 vs. 3.7个月)。Dato-DXd组的中位治疗时间为4.2个月(范围:0.7-18.3),DTX组为2.8个月(范围:0.7-18.9)。Dato-DXd组最常见的TEAE为口腔炎(49.2%,多为1/2级)和恶心(37%)。Dato-DXd组3.4%患者发生了药物相关间质性肺病,DTX组为1.4%。与DTX组相比,Dato-DXd组中与药物相关的≥3级TEAE和导致剂量减少或停药的AE发生率更低。疗效和安全性总结见表3。
表3:疗效和安全性结果
结论
与DTX相比,Dato-DXd治疗既往经治的晚期/转移性NSCLC患者PFS显著获益。非鳞状患者似乎获益最多。Dato-DXd耐受性良好,安全性可控。该研究将一直持续到最终的OS分析。
会议网址:https://www.esmo.org/


