深圳大学任祥忠/南洋理工大学赵彦利团队ACS Nano:仿生纳米酶修饰水凝胶利用H₂O₂激活氧化调节糖尿病伤口的免疫微环境
时间:2023-08-31 13:46:31 热度:37.1℃ 作者:网络
糖尿病是指由遗传因素、内分泌功能紊乱或膳食不平衡等各种致病因子作用,导致胰岛功能减退、胰岛素抵抗等而引发的糖、蛋白质、脂肪、水和电解质等一系列代谢紊乱综合征。糖尿病足溃疡(Diabetic Foot Ulcers, DFU)是糖尿病患者常见的严重慢性并发症,致残率及致死率较高。15%~25%的糖尿病患者一生将出现DFU,其中28%患者需要接受不同方式的截趾/肢治疗。DFU患者死亡风险比单纯糖尿病患者高40%,截肢后死亡率高达74%。基于此,设计和开发具有快速促进伤口愈合的伤口敷料具有广阔的应用前景。目前,多种功能性纳米纤维、多孔泡沫、海绵、高分子膜和水凝胶已被开发并用于DFUs的治疗。与其他传统伤口敷料相比,导电水凝胶因其具有传统高分子材料和有机导体的协同优势,例如含水量高、三维网络结构、良好的电子传输与离子传输能力和高度可调的弹性模量等。基于以上优点,导电水凝胶具有保持DFUs伤口湿润,吸收伤口渗透液,允许物质交换和气体运输等特点,在促进DFUs伤口修复方面具有独特的魅力。
尽管基于导电水凝胶的DFUs伤口敷料,但是这些常规的导电水凝胶仍然无法对DFUs伤口复杂的微环境进行调节。这是因为DFUs伤口严苛的微环境(长期炎症、强烈的蛋白质水解、过度的氧化应激)会导致伤口处巨噬细胞从促炎性M1表型转变成抗炎性M2表型的能力减弱,从而导致M1巨噬细胞的富集,进一步加重DFUs的病情。基于此背景,开发具有改善DFUs伤口病理微环境的导电水凝胶伤口敷料具有重要意义。尤其是能够向修复组织输送氧气,并消除大量堆积的活性氧自由基(Reactive Oxygen Species,ROS)的导电水凝胶伤口敷料开发,对于实现DFUs病理微环境的调控,并促进伤口愈合,具有重要研究意义。
近期,深圳大学任祥忠教授、新加坡南洋理工赵彦利教授等合作团队在仿生纳米酶修饰水凝胶利用H2O2激活氧化调节糖尿病伤口的免疫微环境(图1)。相关成果以标题“Biomimetic Nanozyme-Decorated Hydrogels with H2O2‑Activated Oxygenation for Modulating Immune Microenvironment in Diabetic Wound”发表在“ACS Nano”上。深圳大学和南洋理工大学联合培养的博士后赵月为论文第一作者。此研究得到国家自然科学基金以及博士后派出计划等项目联合资助。

【文章要点】
仿生学是构建多功能平台的一种可行策略,同时也克服了水凝胶的局限性。在生命系统中,一系列天然酶参与复杂的生物催化过程,对生命起着至关重要的作用。最令人印象深刻的例子之一是过氧化氢酶(CAT),它可以通过将H2O2转化为氧气来去除皮肤上的H2O2。由于天然酶具有成本高、稳定性低、对外部条件敏感、回收和储存困难等内在局限性,在恶劣条件下难以进行反应。在这项研究中,作者将MnCoO@PDA纳米酶,PAN,HA和PVA超分子自组装,制备出一种全新的皮肤启发的多功能导电水凝胶。从功能上讲,以皮肤的多功能为灵感,制备出集大范围可调的机械性质以及优异的加工性能等多功能于一身的导电水凝胶MnCoO@PDA/CPH。从应用上讲,MnCoO@PDA/CPH有催化H2O2分解产生O2的功能,此作用进一步加强伤口处巨噬细胞从促炎性M1表型转变成抗炎性M2表型的能力,从而减少M1巨噬细胞的富集改善伤口处炎症状况。动物实验表明,MnCoO@PDA/CPH可以直接粘附在潮湿溃烂的伤口表面,为伤口的愈合提供一个适宜的环境。免疫荧光染色实验结果证明,水凝胶可以通过促进血管生成以及促进胶原沉积等途径,有效地促进创面愈合(图1)。
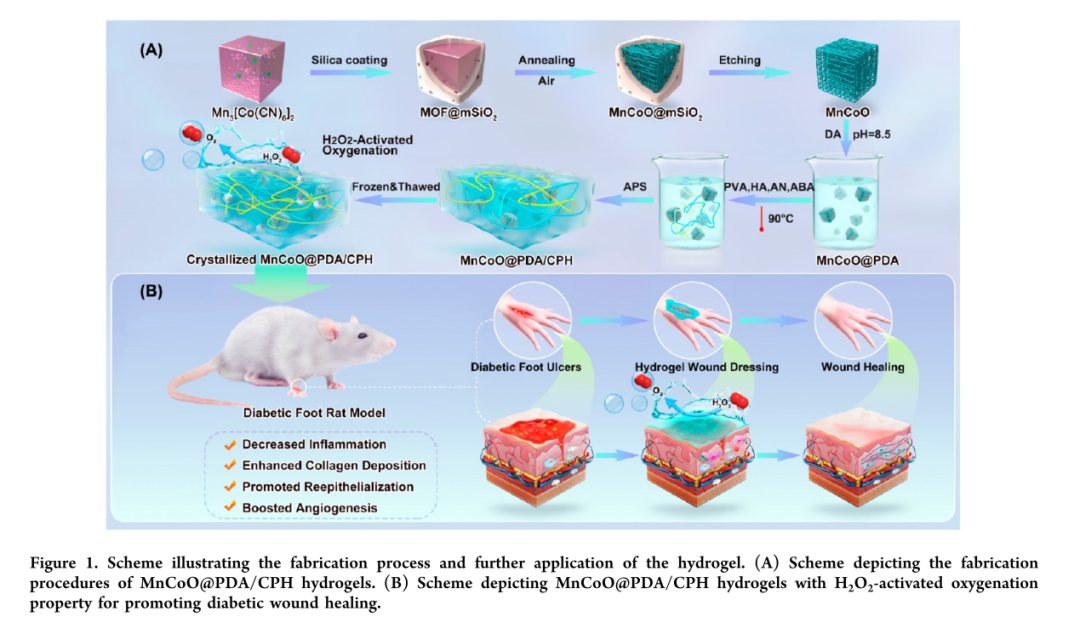
图1:水凝胶制备及其应用
研究表明,在伤口愈合过程中,局部炎症反应是伤口向修复期转化的关键,适当的炎症反应对于创面的修复有积极作用。相反,当炎症细胞聚集过多时,反而会对伤口微环境造成影响,进而延缓创面愈合并加剧瘢痕组织的增生。巨噬细胞是伤口愈合最重要的调节因子之一,它们通过多样化和连续的生物活动控制伤口愈合的炎症反应阶段。在正常的伤口微环境中,巨噬细胞可以从促炎M1表型转变为抗炎M2表型,从而有助于组织愈合。在DFUs微环境中,巨噬细胞在氧化应激的条件下难以从M1向M2的表型转化,从而导致伤口的炎症延长和过度氧化应激。值得注意的是,制备的MnCoO@PDA/CPH水凝胶可以调节巨噬细胞极化并减轻DFUs的炎症反应。高浓度的促炎细胞因子是DFUs的另一个标志。其中,M1巨噬细胞分泌的TNF-α和IL-1β与炎症反应有关并阻碍伤口愈合过程。相反,M2巨噬细胞分泌的IL-10和TGF-β参与抗炎反应并促进组织修复。为了进一步证实纳米酶修饰的导电水凝胶是否可以诱导巨噬细胞极化,利用ELISA试剂盒测定了TNF-α、IL-1β、IL-10和TGF-β的浓度。MnCoO@PDA/CPH水凝胶可以通过清除ROS和产生O2将巨噬细胞的极化方向从M1改变为M2,从而对炎症性DFUs伤口愈合具有良好的治疗效果(图2)。
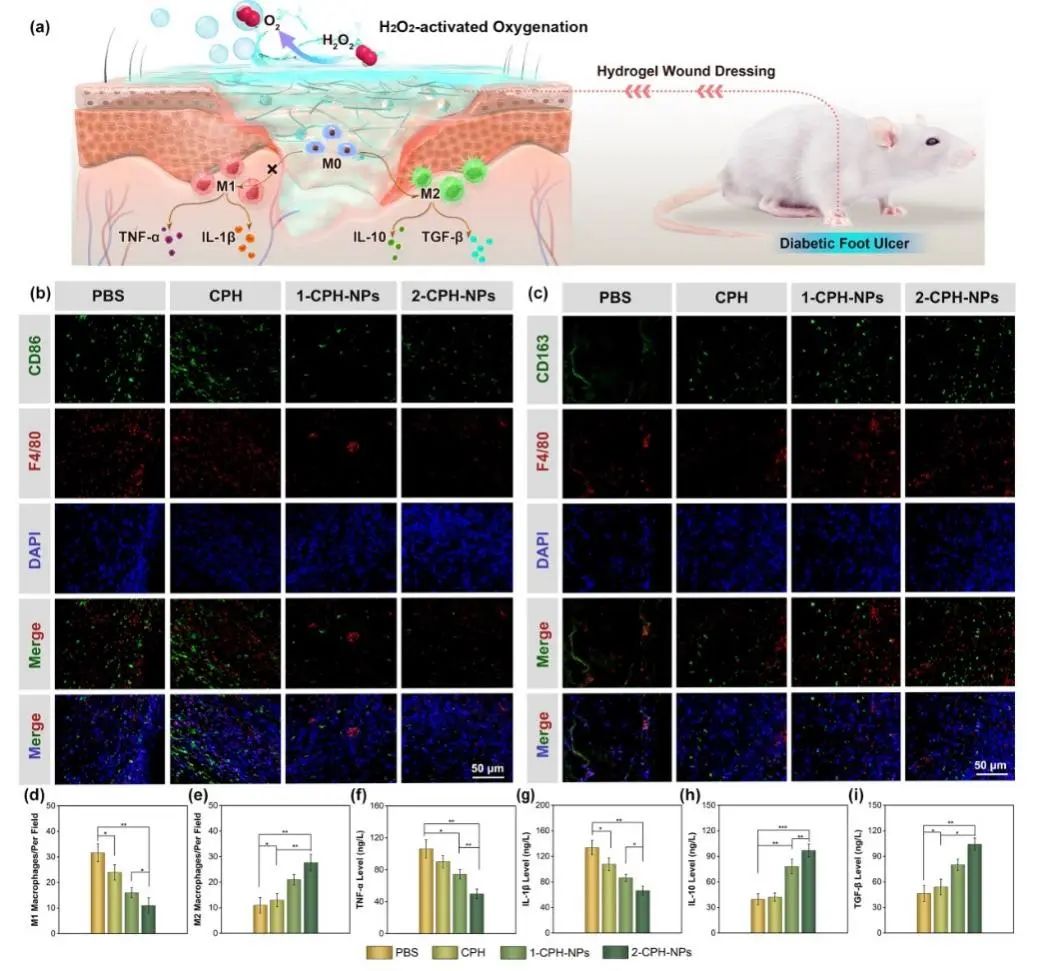
图2:水凝胶调节巨噬细胞极化
【结论与展望】
从机理上讲,作者开发了一种全新的皮肤启发的多功能导电水凝胶。该纳米酶修饰的导电水凝胶具有催化H2O2分解产生O2的功能,此作用进一步加强伤口处巨噬细胞从促炎性M1表型转变成抗炎性M2表型的能力,从而减少M1巨噬细胞的富集改善伤口处炎症状况。动物实验进一步表明,该水凝胶还具有促进血管和胶原生成等作用,对糖尿病足创面的治疗具有显著效果(图3)。预计这种双赢的整合具有纳米酶和水凝胶的共同优势治疗平台,可以协调炎症微环境,为糖尿病足的治疗和干预提供潜在的解决方案。
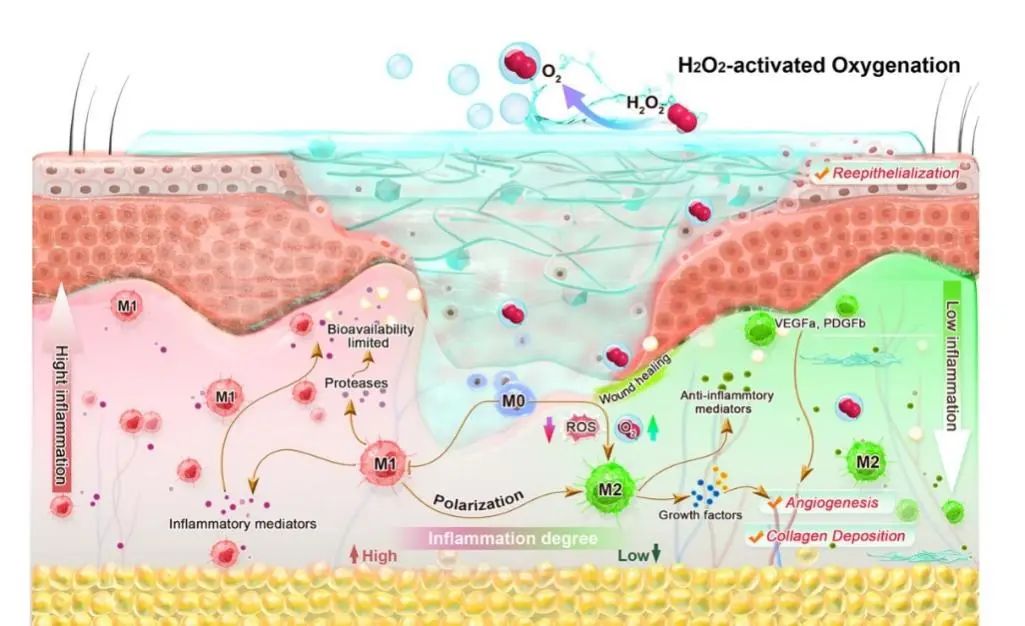
图3:水凝胶作用机理
原文链接:
https://pubs.acs.org/doi/10.1021/acsnano.3c03761


