脓毒性休克患者我是如何实施个性化的液体治疗策略的?
时间:2023-04-01 15:33:34 热度:37.1℃ 作者:网络
在感染性休克期间,液体治疗的目的是增加心排血量和改善组织氧合,但它有两个问题:它具有不一致的和短暂的效果,它有许多证据充分的有害影响。我们建议,在循环衰竭的各个阶段,根据患者的特点和临床情况,采取个性化治疗。在液体复苏的液体选择上,等渗盐水可导致高氯酸中毒,但只适用于非常大的剂量。我们建议采取平衡的解决办法预留给已经接受大剂量治疗且体内氯血症正在上升的患者。最初的液体复苏,旨在补偿感染性休克初始阶段的持续低血容量,不能只适应患者的体重,正如幸存的脓毒症运动所建议的,但也应该考虑由体液损失引起的潜在绝对低血容量。初始输液后,前负荷反应性可能迅速消失,应进行评估。用于此目的的测试之间的选择取决于是否有机械通气,监测是否到位以及积液过多的风险。在非插管患者中,被动抬腿试验和滴定式液体复苏是合适的。在没有心排血量监测的患者中,可以使用潮气量实验、被动抬腿测试和滴定式液体复苏等测试,因为它们可以通过测量脉压变化进行,并通过动脉线进行评估。在已经接受大量输液的患者中,不应重复使用滴定式输液复苏。评估积液的变量取决于临床情况。在急性呼吸窘迫综合征中,肺动脉闭塞压、血管外肺水和肺血管通透性指数比动脉氧合更能评估肺泡水肿恶化的风险。如果出现腹部问题,应考虑腹内压。最后,考虑到患者在稳定期的体液明显过剩。液体的去除可以通过前负荷反应性测试来指导,因为在前负荷依赖状态的患者中,血流动力学的恶化很可能发生。
背景
感染性休克的第一个治疗措施是扩容,看似简单:在几分钟内静脉注射数百毫升液体。然而,在脓毒症患者中使用液体的策略并不简单。今天有几种不同类型的液体可用。液体推注的效果是不一致的和短暂的。补液是有风险的治疗方法,尤其是在感染性休克期间。然后,在实践中会提出很多问题。选择哪种液体?应该输液吗?如何评估其风险并避免输液?如何预测其影响?如何评价他们?对于这些问题,人们可以提供标准的、明确的答案。这就是当前指南所做的没有根据临床背景和患者特征进行区分。目标很可能使它们具有足够的通用性以得到广泛应用,这无疑是值得称赞的。另一个原因是这些指南是基于现有的随机对照试验,而这些试验往往很少关注所纳入患者的特殊性。因此,虽然这些建议很有价值,但可能还有更多个性化液体管理的空间。与“通用”策略相反,“一刀切不适合所有人”的观点多年来一直被重症医学中的几种策略所捍卫。个性化治疗的需要已成为追求的良性目标,尤其是在感染性休克中。与任何其他治疗一样,液体也是如此。在这篇综述中,我们将不仅基于现有的出版物,而且基于液体影响背后的病理生理学概念,描述脓毒性休克的个性化液体策略是什么。从液体类型的选择到去除过量液体的决定,我们将努力证明,在每个阶段,选择都可以合理地个性化。如何自定义液体类型的选择?没有胶体,而是平衡的晶体……在感染性休克中,晶体液是 Surviving Sepsis Campaign (SSC) 的首选。然而,尽管很少有证据支持这种选择,但对于低白蛋白血症和可能有液体过负荷的患者,可以选择等渗白蛋白来增加血浆渗透压。目前的争论主要是在平衡或不平衡晶体的使用之间。使用生理盐水作为主要液体来源可诱发高氯性酸中毒,这可能会降低肾皮质灌注,并可能诱发肾功能衰竭。多项研究表明,与富含氯化物的溶液相比,平衡溶液可降低肾衰竭的发生率,并可能降低死亡率。因此,2021 年 SSC 指南建议在所有脓毒性休克患者中优先使用平衡晶体液。这一弱推荐主要基于 SMART 研究,该研究有其自身的局限性(单一中心、没有个体随机化和脓毒症的可疑识别)。
平衡晶体液,但适用于所有患者?
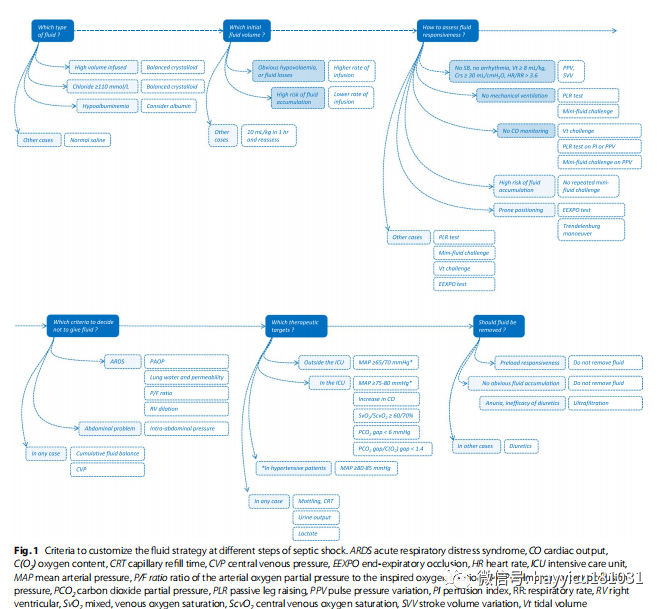
我们是否应该将这些平衡的解决方案作为所有感染性休克患者的首要意图?与其他作者一样,我们认为这种选择应该是个性化的。生理盐水可能会诱发高氯血症,但前提是大量给药。对于体重 70 公斤的患者,必须输注 12 升水才能使血液中的碳酸氢盐水平下降 10 毫摩尔/升。逻辑上,平衡晶体液应保留给需要大量液体且氯血症显着升高的患者。此外,在创伤性脑损伤的情况下,必须首选不平衡晶体和低氯血症。在任何情况下,都应测量氯血症以调整液体类型。在感染性休克的不同阶段定制液体策略的标准。ARDS急性呼吸窘迫综合征、CO心输出量、C(O2 )氧含量、CRT毛细血管再充盈时间、CVP中心静脉压、EEXPO呼气末阻塞、HR心率、ICU重症病房、MAP平均动脉压、P/ F ratio动脉氧分压与吸入氧分压之比,PAOP肺动脉闭塞压,PCO2二氧化碳分压,PLR被动抬腿、PPV脉压变异度、PI灌注指数、RR:呼吸频率、RV右心室、SvO2混合、静脉血氧饱和度、ScvO2中心静脉血氧饱和度、SVV每搏输出量变异度、Vt潮气量。PLUS 研究的结果间接地强化这一观点。先前的研究表明,与0.9% 盐水相比,平衡晶体液具有有益的或中性的作用。PLUS 研究比较 PlasmaLyte与生理盐水在危重患者(不仅是脓毒症)中的效果。该研究结果是否定的:死亡率和急性肾功能衰竭的风险并没有因平衡晶体液而降低,包括在脓毒症患者中。但这令人惊讶吗?该研究包括重症病房 (ICU) 患者的危重人群,他们在前 2 天每天接受少于 2 升的液体。然后,氯血症最终在各组之间几乎没有差异,因此平衡溶液无法在治疗组中发挥任何益处。如果平衡溶液的使用以输注量和氯血症为条件,则该研究可能是阳性的。
我们必须个性化脓毒性休克患者的体液平衡!
液体是有害的......但测试液体限制的研究表明对死亡率没有影响
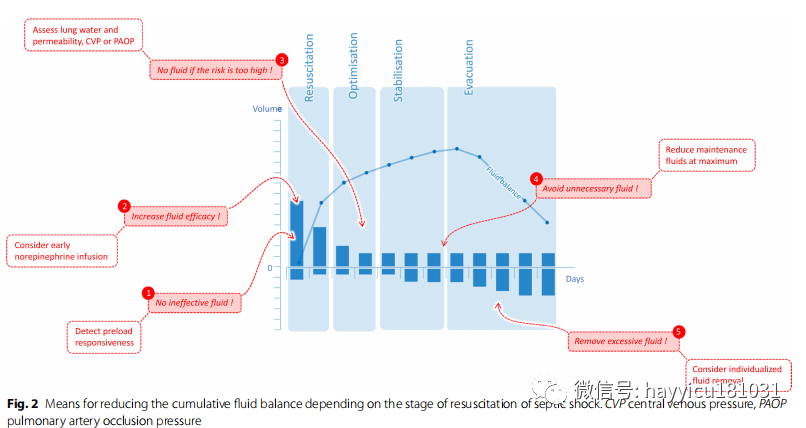
一方面,ICU 期间的液体过负荷是有害的。大量研究表明,累积液体平衡会独立影响 ICU 患者的死亡率,尤其是在感染性休克和急性呼吸窘迫综合征 (ARDS) 期间。另一方面,几项比较“自由”与“保守”或“限制”液体策略的干预研究提供一致的结果:这些策略减少体液平衡,没有有害影响,尤其是对肾脏,但没有降低死亡率,即使这不是一些研究的主要目标。一些研究表明,体液平衡的降低减少了机械通气的持续时间和 ICU 停留时间。但它们有两个主要缺陷,首先,只有为此目的使用所有可能的方法才能最大程度地减少体液平衡。然而,研究限制了复苏液体,或维持和更换液体,或协议化的液体去除,但从未同时使用这三者。在 CLASSIC 研究中,液体限制仅限于液体推注。然后,给药总量在各组之间几乎没有差异(在第 5 天,限制组仅节省 700mL), 减少观察结果差异的机会。相反,在 RADAR-2 研究中,基于限制维持液体和去除液体的策略在更大程度上减少累积液体平衡(第 5 天为 3300 mL)。根据感染性休克复苏阶段减少累积液体平衡的方法。CVP中心静脉压、PAOP肺动脉闭塞压。第二个缺点是这些研究没有根据患者特征个体化策略。有些患者包括特别有体液积聚风险的患者,例如 ARDS 患者;其他研究是在不明确的人群中进行的,其中包括保守策略的预期获益必然较少的患者。此外,还没有研究测试过个体化液体限制对患者生理状态的影响。例如,虽然已知这会降低体液平衡,但并未考虑前负荷响应性。因此,如果降低累积液体平衡似乎是感染性休克患者追求的目标,那么实现这一目标的策略就不应该标准化。我们建议采用一种考虑所有复苏阶段且个性化的方法。
如何自定义初始液体量?
最新的 SSC 指南指出,伴有低血压或血乳酸升高的脓毒症患者应在就诊后 3 小时内接受≥30 mL/kg 的晶体液。本卷仅基于一项观察性研究,旨在补偿初始感染性休克期间的相对和绝对低血容量。患者体重是个体化的唯一参数。然而,初始容量不足的程度在患者之间明显不同。首先,相对低血容量与静脉血管舒张有关,这取决于休克的严重程度。其次,在一些患者中,体液丢失可能是绝对低血容量的原因,这也必须得到补偿。例如,腹膜炎期间的体液不足一定比肺炎期间大。30 mL/kg 的任意体积的推荐不可避免地导致一些患者复苏不足和其他患者液体超载。此外,对液体给药的耐受性也取决于心脏功能。然后应个体化初始液体治疗。例如,仅根据患者情况决定减少初始输注量会增加死亡率。在最开始的阶段,由于低血容量是恒定的,因此测试前负荷反应性是没有必要的,并且可能会延迟复苏。之后,应根据前负荷反应程度个体化扩容,以避免不必要的液体输注。这是 SSC 推荐的,在这一点上,建议个体化治疗。不应延迟评估前负荷反应性,因为它会在感染性休克发作后迅速消失。在 ANDROMEDA-SHOCK 研究中,在接受 27 mL/kg 的液体后,70% 的患者在纳入时仍然有前负荷反应,其中,<20% 在四小时后仍然如此。通过评估感染性休克期间的前负荷反应性来指导初始液体治疗可以降低液体平衡。
如何自定义前负荷反应性的测试或指标选择?
可以在其他地方找到详细说明检测前负荷反应性的指标和测试的评论。我们在这里的目标是描述导致选择一个而不是另一个的原因。选择取决于三个问题。
患者气管插管了吗?
被动抬腿 (PLR) 测试和微量输液挑战不需要机械通气。这使得它们可以在例如急诊室使用,而患者尚未插管]。当然,基于心肺相互作用的测试只能用于插管和通气的患者。脉压变异度(PPV)和每搏量变异度(SVV)(绝对值)只能用于无自主呼吸、潮气量(Vt)≥8 mL/kg、呼吸系统顺应性≥30的患者mL/cmH 2 O,无腹腔内高压,窦性心律,心率与呼吸率之比≥3.6,即少数休克患者。下腔静脉和上腔静脉直径的变化具有相同的局限性(心律失常除外,上腔静脉呼吸频率高)。即使在最佳使用条件下,它的诊断价值也较低,尤其是对于下腔静脉的扩张性。呼气末闭塞 (EEXPO) 测试(呼气末暂停 15 秒,这会在前负荷反应的情况下增加心输出量 (CO),即使在心律失常的情况下也可用于通气患者,无论Vt 和呼气末正压水平。然而,患者必须忍受这种相当长的呼吸中断。在 Vt 为 6 mL/kg 的通气患者中,Vt 挑战(Vt 暂时增加到 8 mL/kg,这会在前负荷反应性的情况下增加 PPV )对自主呼吸有效,这使得它可以广泛使用。它的有效性越来越好地证明了。复张操作 仅适用于 ARDS 患者,而不是常规操作,这极大地限制了它们的使用。最后,在俯卧位时,Trendelenburg 动作可用于将血液输送到心腔并检测前负荷反应。目前它几乎没有得到验证。在俯卧位,Vt 挑战也是有效的 。
进行哪些血液动力学监测?
Vt 挑战、PLR 测试 以及可能的滴定式液体复苏的巨大优势在于它们可以使用简单的 PPV 进行,即只需要一根动脉管路。对于 PLR 测试,许多其他变量可以替代 CO,例如通气患者的呼气末二氧化碳,或体积描记法的灌注指数。EEXPO 测试需要精确测量 CO,因为诱发的每搏输出量变化很小。如果使用超声心动图,应结合呼气末和吸气末暂停以放大速度时间积分的变化,并使其与超声心动图的度更相符。
液体过负荷的风险是什么?
滴定式液体复苏需要注射 100-150 mL 液体,如果无效则不能撤回。如果液体过负荷的风险很高,那么不重复它是合理的。从这个角度来看,它可能比 ICU 更适合手术室。
如何个性化决定在液体中添加血管升压药?
血管加压药可能与液体有协同作用
一旦液体推注不再发挥任何益处,通常会开始使用去甲肾上腺素,以增加动脉压。然而,它对全身静脉回流的影响不容忽视,因为它们可能有助于限制感染性休克期间的液体平衡。通过与静脉 α-肾上腺素能受体结合,去甲肾上腺素诱导血管收缩,从而增加应激血容量的一部分。它增加平均全身压力,发挥类似液体的作用。此外,在血管升压药下进行的扩容可能对心脏前负荷产生更大的影响,因为它发生在收缩的静脉区域。
血管加压药可能在某些患者早期使用
去甲肾上腺素的这些静脉作用与补液协同作用,可能会减少复苏补液量。对脓毒症患者的观察性研究表明,尽早开始使用去甲肾上腺素可能会降低体液平衡,其中一项与倾向评分相匹配的患者表明,在极早的情况下使用去甲肾上腺素可提高生存率。然而,已经报道相反的观察结果。CLOVERS 研究将患者随机分为限制性策略(优先考虑较低的静脉输液量和血管加压药)和宽松策略(在开始使用血管加压药之前优先考虑较高的液体量)。尽管在最初 24 小时内给予的液体较少,但第 90 天的死亡率在各组之间没有差异。然而,介入组将早期去甲肾上腺素给药与限制性液体策略相结合,存在上述研究的缺陷,因此无法从这些结果中推断出仅早期去甲肾上腺素给药对预后的影响。此外,在这项研究中,没有选择较早使用去甲肾上腺素的患者。对于大多数低血压的脓毒症患者,应该考虑早期给予去甲肾上腺素,以促进血压恢复。此外,去甲肾上腺素可能对血管明显扩张的患者最有效,如低舒张压(例如 <40 mmHg)所示。舒张期休克指数(心率除以舒张动脉压)比单独使用每个变量更能预测死亡,也可考虑用于此目的。此外,液体推注对 CO 的有效性是短暂的。在围手术期,250 mL 晶体液对 CO 的影响在 10 分钟后消失。由于血管扩张和毛细血管渗漏,脓毒症患者的持续时间可能更短。即使尚未进行调查,液体推注对微循环的影响也可能是短暂的。因此,在脓毒症患者中,用去甲肾上腺素恢复血液动力学可能会产生更持久的效果,尽管这尚未得到证实。
如何自定义停止输液的标准?
良好的液体管理应包括安全标准,表明液体输注的风险超过预期益处。在纠正初始低血容量后,这些标准在稳定阶段尤为重要。两种临床情况可能证明监测特定指标是合理的。对于ARDS 患者,为了警惕额外输液的风险,人们通常使用动脉氧分压 (PaO2 ) 与吸气分数 (FiO2) 的比值。然而,它也可以通过肺实变、与微血栓相关的分流等而降低,这些不受额外液体输注的影响。先进血液动力学监测技术可以更直接地估计液体复苏的肺部风险。肺动脉导管估计肺毛细血管压力,推动液体进入间质。在重症患者中,通过超声心动图估计这种压力的可靠性很差。经肺热稀释法测量的血管外肺水和肺血管通透性直接反映液体向间质和肺泡渗漏的风险。肺水的最大值影响 ARDS 患者的预后,独立于其他严重程度标准。肺部超声通过 B 线证明间质性肺水肿。虽然诊断间质性水肿可靠,但其量化肺水肿总量的价值只能通过繁琐的 B 线计数。此外,它忽略肺泡水肿,因此它不能很好地反映肺水总量。
腹内高压患者
特别是在有腹部问题的患者中,应考虑腹内压 (intra-abdominal pressure, IAP) 来估计液体过负荷的风险,液体过负荷通过内脏和壁层水肿增加 IAP。腹内高压会损害腹部器官(主要是肾脏)的灌注,并独立影响 ICU 患者的预后。在决定在稳定阶段进行液体推注之前,必须考虑这个变量。
不要忘记CVP!
无论患者如何,即使 CVP 不能预测前负荷反应性,其测量也提供大量经常被忽视的信息。CVP 是器官血流的反向压力,CVP 水平升高与器官功能障碍有关。限制 CVP 的增加可能是合理的目标,并且可能有理由对 CVP 升高的患者设定更高的平均动脉压目标。
如何个性化治疗靶点?
液体推注旨在增加平均全身压力、心脏前负荷,从而增加每搏输出量和 CO,并最终改善组织氧合。然而,治疗目标必须适应可用的血液动力学监测和环境。
重症病房外
在病房、院前或急诊进行液体治疗时,临床检查必须寻找组织灌注改善的临床体征:皮肤花斑消失,毛细血管再充盈时间缩短,消失较快,即使在单次液体推注后也可能发生变化。由于观察时间非常短,器官功能改善,尤其是利尿增加很少见。尽管应始终寻找这些迹象,但它们不能很好地反映 CO 变化。大量液体的主要作用是增加 CO,而动脉压升高只是偶然发生的。值得注意的是,平均动脉压的目标可能会根据既往高血压的存在进行调整。然而,脉压是监测 CO 变化时应观察的脉压,因为它是最能反映每搏输出量的压力值。平均动脉压的变化减弱,因为交感神经系统倾向于在 CO 变化时保持恒定。令人惊讶的是,恢复平均动脉压可被视为液体治疗的目标。然而,即使脉压的变化也不能完全反映 CO,通过肱袖套进行评估时可能更是如此。同样,心率的降低对于检测液体引起的 CO 增加是不可靠的。这就是在可能情况下直接测量 CO 以更好地评估液体影响原因。
在ICU病房
更多变量可用于估计液体功效。CO 很容易测量,无论是通过经肺热稀释法、肺动脉导管,推荐用于最严重的患者,还是通过超声心动图。如果无法直接测量 CO 但有动脉管路,则 PPV 的降低反映前负荷反应性的降低,并证明对液体的反应。在插管和完全稳定通气的患者中,呼气末二氧化碳的增加与 CO 的增加平行。正如一些研究表明的那样,由灌注指数量化的体积描记信号的振幅也可以反映液体引起的 CO 增加。此外,必须评估对组织氧合的影响,因为增加的 CO 并不总是会导致耗氧量增加,因为耗氧量和输送是独立的或因为微循环紊乱。在 ICU 中,有几个变量可用于此目的。乳酸的减少与良好的预后相关,是有效的治疗目标。通过经常插入的中心静脉导管,静脉血氧饱和度和二氧化碳衍生变量显示改善的组织氧合作用。如果肺动脉导管就位,则可以更可靠地从混合静脉血中测量这些变量。在静脉血氧饱和度正常的情况下,静脉-动脉二氧化碳分压差与动静脉氧含量差之比,即呼吸商的估计值,被认为是无氧代谢的标志,反应比乳酸和较少的假阳性。据报道,其正常值 <1.4 尽管已报道不同的阈值。
如何定制液体消耗?
减少总液体平衡的方法之一是在复苏-优化-稳定-撤离 (ROSE) 概念的“撤离”阶段进行主动液体消耗。事实上,仅减少复苏液体是不够的,因为维持和置换液体占 ICU 输注液体的很大一部分。这种降级的方式是可变的,它们应该通过考虑有用性和安全性来个性化。
哪些患者应该积液清除?
体液耗尽对体液积聚最多的患者最有益,如上述变量所示:左心室充盈压高、CVP 高、肺水过多、CT 扫描显示肺充血迹象和 IAP 升高。软组织水肿的存在不一定是必需的,因为它们可能相反地伴随着血管内部分的耗尽。相反,如果积液量低,例如感染性休克很容易解决,则液体耗竭的好处就不那么明显了。因此,必须权衡实施它的风险和可能的收益。
如何去除积液?
首先使用利尿剂。然而,在少尿或无尿的情况下,肾脏替代治疗期间的超滤是替代解决方案。在低白蛋白的情况下,20% 高渗白蛋白可以对液体去除产生协同作用。在因急性肺损伤进行通气的患者中,将呼气末正压调整为 IAP,然后输注高渗白蛋白和呋塞米的策略导致负累积液体平衡并减少肺水和 IAP 。
如何判断去液体负荷的量?
抽取过多液体的风险是改变血液动力学状态。为确保液体消耗的安全性,必须考虑生理条件,这在实践中很少进行。首先,血流动力学状态必须稳定,升压药必须低剂量或停药。然后,通过去除液体来降低心脏前负荷。相反,如果心室对前负荷无反应,则必须很好地耐受液体排出。人们应该将抽取液体的决定限制在存在前负荷无反应性的情况下。在一项针对处于休克稳定期的危重患者的研究中,通过超滤去除液体不会导致没有前负荷反应性的患者出现透析内低血压,并且在耗竭前通过阴性 PLR 测试证明。即使在体外回路启动时,CO 的减少在前负荷反应性情况下比在前负荷无反应性情况下更频繁,其他因素也可能导致透析内低血压。然而,事实仍然是前负荷反应性的存在必须促使不要抽出额外的液体。
结论
尽管液体疗法看似简单,但它却是复杂的。液体是药物,效果不一致,并具有显著的有害作用。像任何药物一样,它们必须以正确的剂量使用,并且只给需要它们的患者。为了指导液体治疗,而不是依赖于所有患者的相同策略,有可能做出个性化的决定。考虑患者的特征(血管舒张的严重程度,液体积聚的重要性),临床病史(评估初始低血容量的深度),生理状况(特别是负荷前反应性),应从逻辑上确保有效和安全的液体输送和排出。如果不考虑这些个人标准,调查各种液体治疗策略的临床研究仍然是负面的。

Monnet et al. Critical Care (2023) 27:123 https://doi.org/10.1186/s13054-023-04363-3


