Front.aging neurosci-阿尔滋海默病小鼠中运动障碍与纹状体纤维和血管变性相关
时间:2023-03-28 10:11:50 热度:37.1℃ 作者:网络
越来越多的证据表明脑血管功能障碍在阿尔滋海默病(AD)的进展中起着关键作用。流行病学研究表明,AD发展的风险与动脉粥样硬化、高血压和高胆固醇血症等血管疾病之间存在很强的相关性。强有力的证据表明,淀粉样蛋白 β (Aβ) 与纤维蛋白原(一种大的糖蛋白,是血栓的主要成分)的相互作用一定程度上直接有关。AD 小鼠模型也表现出改变的血栓形成和纤维蛋白溶解,以及纤维蛋白原的减少,过多的纤维蛋白原通过结合和改变紧密连接以及与多种免疫细胞相互作用导致促炎通路激活来增加内皮细胞壁的通透性。
10-40% 的 AD 患者在疾病进展早期表现出运动功能障碍的迹象,包括步态、运动和平衡缺陷,而大多数患者在疾病后期会出现严重的运动障碍。此外,运动功能的变化可能会引发 AD 的其他症状,并与严重程度和死亡率增加相关。尽管 AD 患者经常发生运动功能障碍,但人们对影响这种行为的机制知之甚少。虽然人类和动物模型研究表明 AD 中的运动和平衡功能障碍。但这些行为的特定大脑区域和分子基础表型尚未阐明。在其他几种神经系统疾病中,例如中风和血管性帕金森病 (VP),脑血管损伤是疾病进展过程中运动功能障碍的基础。在基底神经节发生梗塞的中风患者中可以看到对运动功能的严重影响,这是血管功能障碍与改变运动能力之间关系的证据。这些观察共同提出了这样一种可能性,即血管缺陷可能是 AD 患者和 AD 小鼠模型中表现出的一些运动功能障碍的基础。

作者分析了 Tg6799 小鼠大脑皮层、纹状体、海马和丘脑等多个脑区在7个月和 15 个月时的年龄依赖性纤维蛋白(原)外渗,以确定脑区和动物年龄对纤维蛋白的影响(原)外渗。作者发现,与野生型 (WT) 同窝小鼠相比,两个年龄段的AD小鼠的皮层和纹状体中纤维蛋白(原)外渗显着增加,并且发现沉积物的年龄依赖性增加。此外发现15个月大的 AD小鼠纹状体中的血管密度显着降低。

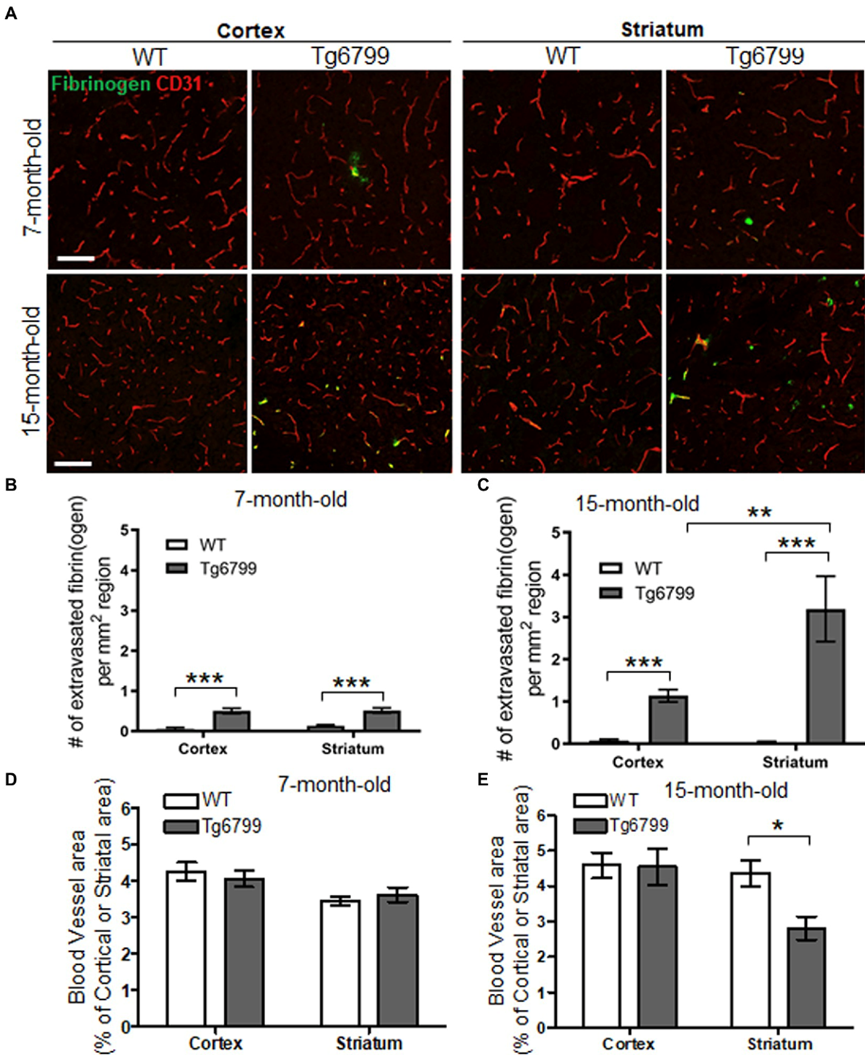
图1 7 个月和 15 个月阿尔茨海默病 (AD) 小鼠模型中
外渗的纤维蛋白原和血管密度
作者测量了 15 个月小鼠中纹状体和大脑皮层中 Aβ 沉积物的面积。与WT相比,AD小鼠的大脑皮层和纹状体中的 Aβ 沉积物水平明显较高(图2A - D),许多CD11b 阳性激活的小胶质细胞聚集在 Aβ 斑块周围或附近(图 2B、C)。我们发现在 15 个月的 AD 小鼠中,纹状体和皮质中活化的小胶质细胞或巨噬细胞水平显着增加(图 2E). 因此,这些结果表明,Aβ 沉积和小胶质细胞增生与 15 个月 AD 小鼠纹状体中外渗纤维蛋白(原)和血管变性水平增加有关。

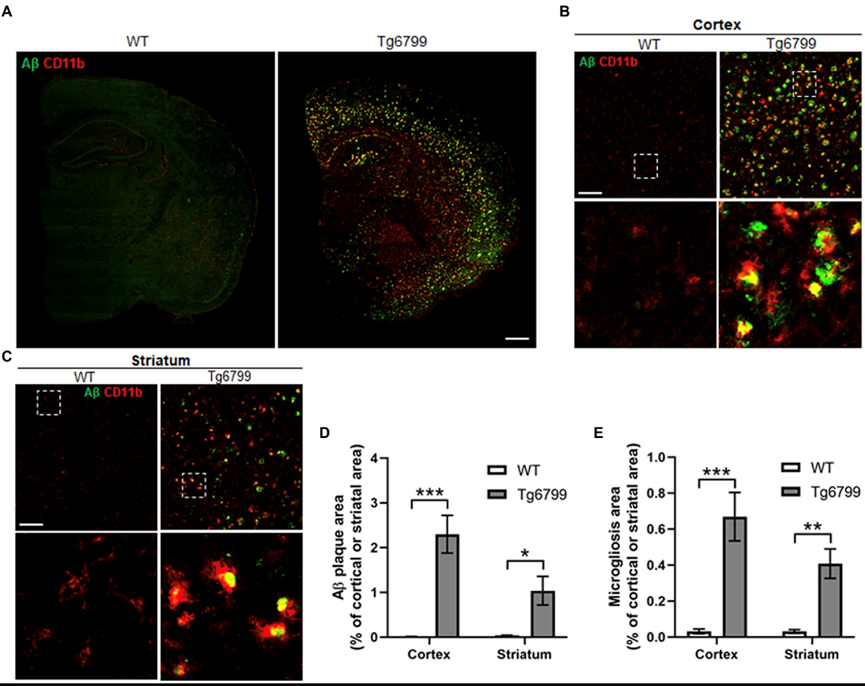
图2 (Aβ) 沉积和小胶质细胞增生
与 WT 同窝仔相比,Tg6799 纹状体白质中的髓鞘染色区域显着减少,MBP 染色的纹状体和基质区域显着减少,. MBP和神经丝共定位信号在 AD小鼠中也减少了,表明纹状体中潜在的轴突脱髓鞘。并且纹状体中的轴突神经丝染色显着减少,这似乎是区域特异性的,因为在同一小鼠的皮质中没有观察到显着差异。总之,这些结果表明脱髓鞘和轴突损伤发生在 AD 小鼠纹状体中与纤维蛋白原外渗和血管变性非常接近。
最后,作者发现衰老的 AD 小鼠表现出运动功能下降,丧失运动和平衡功能,总之行为分析表明,纹状体中的血管变性、纤维蛋白(原)外渗和脱髓鞘可能导致老年阿尔茨海默病小鼠模型中的异常焦虑和运动功能障碍。
在这项研究中,作者发现纤维蛋白原相关的血管损伤和轴突脱髓鞘发生在衰老 AD 小鼠大脑纹状体的同一区域,并且具有区域特异性。作者的研究在这些小鼠运动功能下降的时期内,提供了运动功能受损与AD中的血管异常之间的相关性,证明了随时间增加,AD小鼠纹状体中纤维蛋白原外渗的大量增加会导致脱髓鞘、轴突变性,并最终导致运动功能障碍。
参考文献:
Berk-Rauch HE, Choudhury A, Richards AT,Singh PK, Chen Z-L, Norris EH, Strickland S and Ahn HJ (2023) Striatal fibrinogen extravasation and vascular degeneration correlate with motor dysfunction in an aging mouse model of Alzheimer’s disease. Front. Aging Neurosci. 15:1064178.doi: 10.3389/fnagi.2023.1064178


