JAK抑制剂
时间:2023-01-24 18:02:22 热度:37.1℃ 作者:网络
 2021年9月,Theravance包括JAK抑制剂在内的两款药物临床失败,宣布裁员75%,公司股价一夜之间下跌超30%。
2021年9月,Theravance包括JAK抑制剂在内的两款药物临床失败,宣布裁员75%,公司股价一夜之间下跌超30%。
然而,往前再倒三年,强生却向Theravance支付了高达10亿美元的对价,获得后者的JAK抑制剂。某种程度上说,Theravance的裁员转折,正是“JAK”两面性的另类写照。
作为发展近30年的重要药物类型,JAK抑制剂有过一段颇具故事性公案。生物学家发现这类激酶之初,将其命名为“JAK”的全称是Just Another Kinase(只是另一种激酶)。直到后来,或许有人基于JAK两个结构域——一个正常的激酶结构域,一个伪激酶结构域——从罗马神话中借用拥有前后两副面孔的神祗Janus(雅努斯)的叫法,才形成了当下主流的Janus Kinase。
Janus掌握开始和结束两扇门,而对于药企而言,Theravance的受挫,暗示了JAK抑制剂也可能掌握公司的繁荣与衰败。
过去的2022年,FDA等监管机构对JAK抑制剂的担忧和限制,就连辉瑞等巨头也深有体会。可是,这并没有阻止更多竞争者的跃跃欲试。同样是去年,GSK豪掷19亿美元,买下了一款五易其主的JAK抑制剂;武田制药也在上个月出手,就JAK亚型之一TYK2抑制剂达成60亿美元的合作。
2023年,JAK抑制剂赛道会迎来新的变化吗?如果有,这些躬身入局的药企中,又会是哪些脱颖而出的黑马,成功将“魔鬼”驯化为“天使”?理解这一切,还得回到JAK抑制剂的突破起点。
1JAK进击:从骨髓、自免到新冠
JAK家族共包含四种亚型,JAK1、JAK2、JAK3和TYK2(酪氨酸激酶2),它们都在上个世纪被业界发现。
早在1989年,就有科学家确定了酪氨酸激酶具有可识别的激酶结构域和假激酶结构域。1991年,他们发现了第二个具有这种特征的酪氨酸激酶,并称之为JAK1和JAK2。而酪氨酸激酶2(TYK2)和JAK3则分别于1990年和1994年被识别。
基础研究的突破,带动一大批药企进场,最终饮下“头啖汤”的,是开发出芦可替尼(ruxolitinib)的诺华和Incyte。2011年,全球首款JAK抑制剂芦可替尼获FDA批准,用于治疗中危或高危骨髓纤维化患者。
随后,两家公司对芦可替尼开展多个领域的开发,至今已成功将其应用到特应性皮炎、移植物抗宿主病、真性红细胞增多症、原发性骨髓纤维化等多达几十种疾病。根据分工,Incyte负责芦可替尼(Jakafi)在美国市场,剩下的则交由诺华(商品名Jakavi)。2017年3月,芦克替尼在中国获批上市。
根据诺华2021年的财报,报告期内,芦可替尼为其带来了15.95亿美元,同比增速19.1%。
当然,分食这块蛋糕的不只是诺华和Incyte。就在芦可替尼首次上市的第二年,辉瑞带着它的JAK1/3抑制剂托法替布(tofacitinib)杀入。
辉瑞是最早将JAK视为多种疾病的潜在药物靶点进行研究的药企之一。2009年,ORAL Start研究首次证实,托法替布可单独用于治疗甲氨蝶呤治疗无效的类风湿关节炎患者。经过三年的酝酿和准备,2012年托法替布“粉墨登场”,获FDA批准用于治疗类风湿性关节炎,成为自身免疫疾病领域的首款JAK抑制剂。
目前,托法替布的适应症也实现扩展,覆盖了强直性脊柱炎、幼年特发性关节炎、溃疡性结肠炎、银屑病关节炎、类风湿性关节炎等疾病。
商业化市场方面,辉瑞已将托法替尼推向全球50个国家。2021年财报显示,尽管0.7%的增速一般,托法替布仍以24.55亿美元的销售额,领跑JAK抑制剂赛道。
有意思的是,JAK抑制剂还一度成为新冠药物瑞德西韦的搭档,在抗病毒市场发光发热。2020年11月,礼来与Incyte联合开发的巴瑞替尼(baricitinib)获得FDA紧急使用授权(EUA),与瑞德西韦联合用于需要辅助供氧、有创机械通气或ECMO的疑似或确诊COVID-19成人和儿童(2岁或2岁以上)住院患者。
2021年,巴瑞替尼虽刚跨过“重磅炸弹”的门槛,却以75%的销售额增速惊艳同行。去年6月,巴瑞替尼取得了治疗严重斑秃的重大突破,这是FDA批准的首个斑秃全身性疗法。因为临床试验效果显著,该药一度引起热议。
2黑框警告与崛起的JAK二代药物
JAK抑制剂之所以摘得“双面神”称号,自然是除了疗效优越之外,还存在致命的弱点:安全性问题。
领跑JAK市场的托法替布首当其冲。2019年2月和7月,FDA就曾警告称,托法替布可能会增加患者血栓和死亡的风险,因此对其说明书加上黑框警告。两年后,辉瑞一项长达六年的研究失败,FDA又一次强调了该药“出现严重心脏相关问题和癌症的风险增加”。
但“被针对”的不单单是托法替布,FDA质疑其安全性时,就埋下了JAK抑制剂的声誉下滑和使用受限的伏笔。很快,2021年9月,FDA给所有JAK关节炎药物作出严重的黑框警告。
欧洲监管机构也有同样的担忧。去年10月,药物警戒风险评估委员会(PRAC)建议,只有在没有合适的替代治疗方法的情况下,才应将这些JAK抑制剂用于65岁或以上的患者、患重大心血管疾病(如心脏病发作或中风)风险增加的患者、吸烟或长期吸烟的患者以及癌症风险增加的人群。
一个月后,EMA人类药物委员会(CHMP)批准了上述建议的措施,以最大限度地降低用于治疗几种慢性炎症疾病的JAK抑制剂的严重副作用风险。
从机制上来看,这或许是第一代泛JAK抑制剂情理之中的命运。但JAK选择性抑制剂具体是否优于非选择性药物,目前还有待更多数据验证。公平地说,抗癌药物和自身免疫药物的安全障碍是截然不同的,对于JAK这一类型的抑制剂也是如此。
令人欣慰的是,已有第二代JAK抑制剂顺势而生,它们拥有更高的选择性、安全性和耐受性。艾伯维的乌帕替尼(upadacitinib)无疑是二代中的翘楚。
2022年10月,FDA批准该药用于治疗对肿瘤坏死因子(TNF)阻滞剂治疗反应不足或不耐受的具有客观炎症迹象的活动性非放射轴性脊柱关节炎(nr-axSpA)成人。从数量上而言,这是乌帕替尼第六次获得FDA批准,也使其成为首个也是唯一一个在反应不足与不耐受两种条件下都获得批准的药物。
乌帕替尼首次获批于2019年,后有四项新适应症在五个月内接连获得FDA的首肯。2022年上半年,乌帕替尼销售额达到10.57亿美元,同比增长55.1%;第三季度,该药销售额达到6.95亿美元,同比增速为59.3%。俨然有扛起修美乐大旗的气势。
截至目前,全球范围内共有10款JAK抑制剂获FDA批准上市,其中5款为第一代JAK抑制剂,5款为第二代JAK抑制剂。
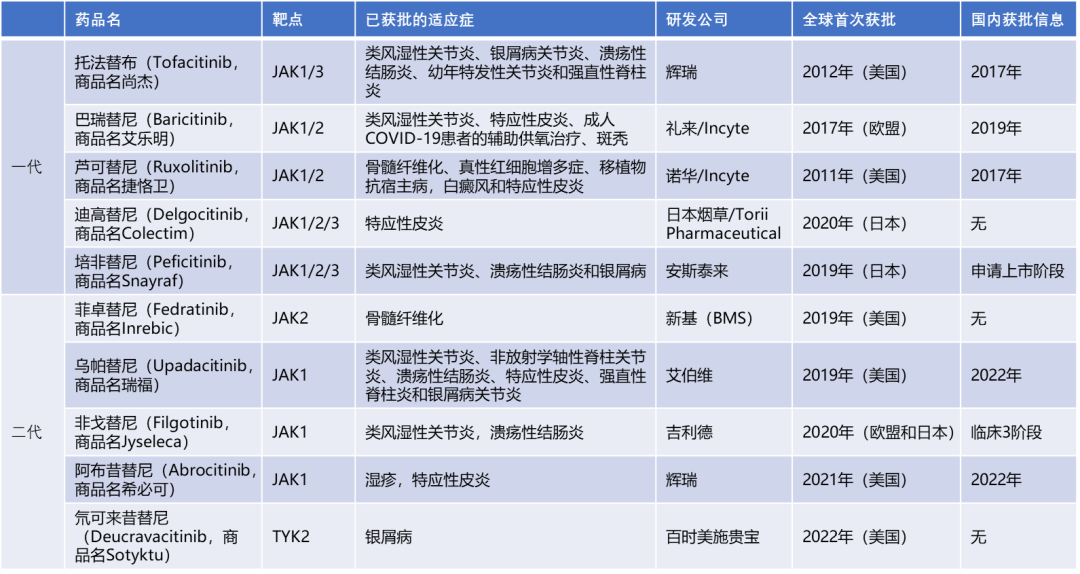 目前获批JAK抑制剂
目前获批JAK抑制剂
尽管第二代JAK抑制剂能够进一步降低风险,但它们要打消FDA对于这类药物安全性问题的担忧,仍需要很多有力的临床证据。
3
本土创新,谁能实现“零”突破?
JAK抑制剂不只在国外市场如火如荼,也有不少产品在国内获批。
截至目前,我国已获批的JAK抑制剂共有5款,分别为诺华的芦可替尼、礼来的巴瑞替尼、辉瑞的托法替布、艾伯维乌帕替尼、辉瑞阿布昔替尼,适应症主要覆盖类风湿关节炎、骨髓纤维化、特应性皮炎等方面。
虽暂未有国产JAK抑制剂获批,但国内诸多企业也参与了布局,而且突破在望。据不完全统计,我国布局JAK抑制剂药企有10余家,在研项目多为第二代选择性抑制剂,适应症主要围绕自免领域疾病展开。
在众多研发者中,恒瑞医药SHR0302、泽璟制药杰克替尼目前已进入III期临床。
恒瑞医药SHR0302以JAK1为作用靶点,开发了片剂和软膏剂两种剂型,已开展包括类风湿性关节炎、溃疡性结肠炎、特异性皮炎、斑秃、银屑病关节炎等多项适应症。2022年11月,艾玛昔替尼片治疗特应性皮炎的II期临床研究也获得成功,成为首个在自免领域获得关键III期研究成功的国内自研JAK1抑制剂。
一个月后的ASH大会上,恒瑞医药公布艾玛昔替尼联合泼尼松一线治疗AIIo-HSCT后慢性移植物抗宿主病的I期研究数据。该研究共纳入18例患者,首次给药后,第四周ORR已达到94.4%,4例患者(22.2%)达到完全缓解,13例患者(72.2%) 部分缓解。
至于泽璟制药的杰克替尼,则正在开展多个炎症性疾病及纤维化疾病的临床研究,且已于2022年获批进行治疗重型新型冠状病毒肺炎的临床试验。
此外,信达生物、迪哲医药、科伦制药、微芯生物、石药集团等实力药企均参与到JAK抑制剂市场中,在各自的研究方向取得不错的成效。但从研发进度看,恒瑞医药的SHR0302或将凭借先发优势,成为首款国产创新JAK抑制剂。
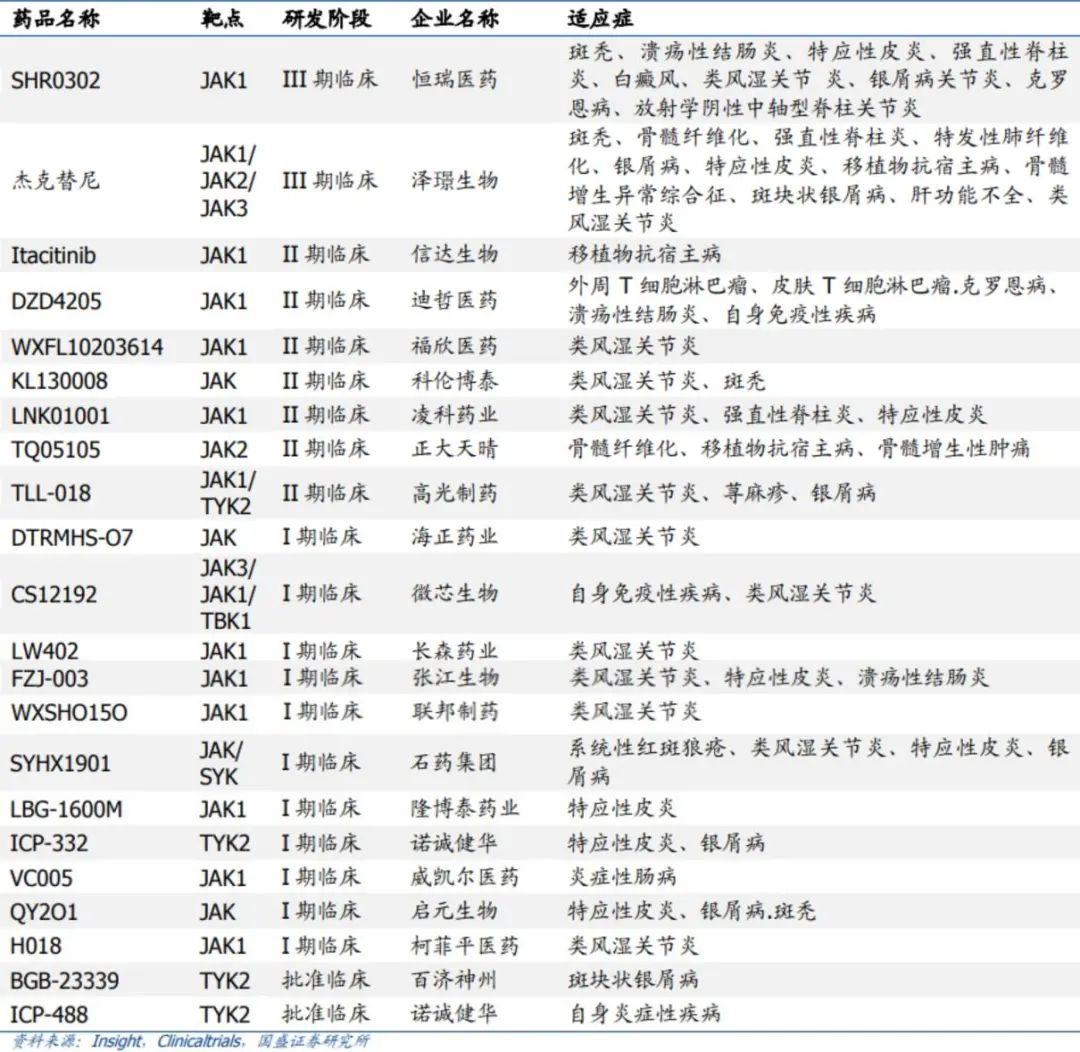 国内部分在研JAK抑制剂情况
国内部分在研JAK抑制剂情况
JAK/STAT通路可以调节与多种疾病发展相关的多种细胞机制,适应症较多,未来发展前景广阔。2021年,全球已上市的JAK抑制剂市场规模就已达到近90亿美元,市场也很可期。
随着更多本土药企入局,国内竞争也会逐渐加大。2023年,JAK抑制剂的战火将更加激烈。能否在这诱人的巨大蛋糕中吃个饱,各家药企还要拿出真本事。


