AM | 北京大学吴水林等团队合作开发新的治疗策略,实现细菌感染骨髓炎的快速根治
时间:2023-01-22 00:00:03 热度:37.1℃ 作者:网络
因细菌感染导致的骨髓炎危及生命,但尚缺乏有效的临床治疗方法。
2023年1月10日,北京大学,湖北大学及天津大学多单位合作,吴水林及刘想梅共同通讯在Advanced Materials 在线发表题为“Achieving Fast Charge Separation by Ferroelectric Ultrasonic Interfacial Engineering for Rapid Sonotherapy of Bacteria-Infected Osteomyelitis”的研究论文,该研究报道了一种超声触发BiFeO3/MXene (Ti3C2)铁电极化界面工程实现快速有效治疗骨髓炎的策略。超声触发下铁电极化诱导压电场的形成,而超声空化效应诱导的声致发光刺激BiFeO3/ Ti3C2产生光生载流子。
在极化电场和肖特基结的协同作用下,BiFeO3/ Ti3C2加速了电子和空穴的分离,同时抑制电子回流,提高极化电荷和光生电荷的利用率,继而提高了超声触发下活性氧(ROS)的产量。结果表明,在超声波加热的辅助下,99.87±0.05%的金黄色葡萄球菌在20分钟内被有效杀死。该研究提出了铁电超声界面工程理论,为开发用于深部组织感染诊断和治疗的铁电超声响应材料和其他声电器件提供了新的思路。

骨髓炎等深部组织发生的病原菌感染严重威胁患者的生命健康。无创疗法因其独特的治疗优势而广受关注。近年来,光动力疗法(PDT)作为一种代表性的无创治疗手段,通过光敏材料产生的光触发活性氧(ROS)快速杀灭细菌,对一些由细菌引起的疾病起到了理想的治疗效果。然而,生物组织中,即使是近红外光的穿透深度也很差,限制了其在治疗深部组织感染中的应用。与PDT相比,声动力疗法(SDT)可以利用超声波(>20 kHz)刺激声敏剂产生ROS并诱导氧化损伤来杀死细菌。SDT具有高组织穿透能力(在软组织中超过10 cm)、高远程时空选择性、低成本和可忽略的全身毒性,应用前景广阔。然而,因缺乏声动力敏化剂,SDT仍难以用于临床应用。因此,开发合适的声敏剂对SDT的应用至关重要。
截至目前,声敏剂主要包括有机小分子(卟啉化合物、二氢卟吩e6和玫瑰红)和无机声敏剂(二氧化钛、二硫化钼)。但有机声敏剂可能会使皮肤长期敏感、稳定性低且在生理环境中药代动力学较差,无机声敏剂较差的SDT效率也限制了其进一步应用。因此,开发具有高ROS产量和生物相容性的新型声敏剂意义重大。压电材料起源于非中心对称的晶体结构,当受到外部机械应力(如超声)时,其独特的压电效应可以产生内置电场和表面压电电势,从而诱导催化行为。与来自p-n结和肖特基结的电场相比,压电势可以提供强大的驱动力来分离界面载流子。此外,空化效应可以在超声过程中发生,其中空化气泡的破裂可以释放局部高温、高压和强冲击波。与PDT类似的是,塌陷气泡的声致发光可以激发压电材料产生光生电子和空穴。因此,压电材料是潜在的高效声敏剂。
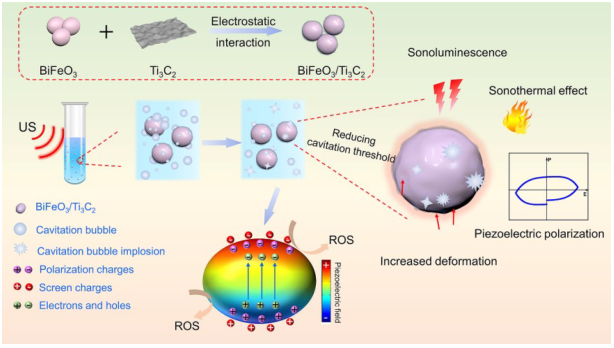
BiFeO3/ Ti3C2超声机理示意图(摘自Advanced Materials )
铁酸铋(BiFeO3)的自发极化强、压电系数高(d33),是众所周知的压电催化铁电材料。由于内建电场的形成,其铁电势可用于电子和空穴的分离。然而,低电荷分离效率使自发压电场得到的ROS量较少,导致SDT效率差。BiFeO3和具有优异导电性材料的界面工程构建可用作SDT的有效声敏剂,是打破现有瓶颈的潜在策略。二维(2D)MXene(Ti3C2)因其优异的导电性和化学稳定性而备受关注,这些特性均有利于电子转移。
因此,作者尝试通过结合Ti3C2和BiFeO3形成铁电极化和肖特基结来加速界面处的电荷转移,从而构建界面电荷转移通道。该研究中,带正电荷的BiFeO3纳米颗粒通过静电相互作用被带负电荷2D Ti3C2纳米片包裹。超声振动驱动BiFeO3/ Ti3C2产生空化气泡和铁电极化,前者的内爆将导致局部声热效应和声致发光,声致发光可以触发材料电子跃迁产生光生电子和空穴。同时,后者促使界面处压电场的形成,驱动极化电荷和光生电荷在界面间转移,实现空穴和电子的有效分离。
由于表面上不平衡的电荷状态,BiFeO3/ Ti3C2的超声应变增加产生更多的空间电荷。铁电超声界面工程为分离电子和空穴提供了更大的驱动力,使表面电荷状态不平衡性增加。因此,在超声作用下,更多的电荷参与ROS的产生,可以在20分钟内快速有效地根治细菌引起的骨髓炎。该策略有望使压电材料成为细菌特异性SDT的有效声敏化剂。
参考消息:
https://onlinelibrary.wiley.com/doi/10.1002/adma.202210296


