特别关注|肝切除术前肝储备功能的评估方法
时间:2023-08-03 15:26:20 热度:37.1℃ 作者:网络
肝脏是人体维持生命活动的重要器官之一,是人体最大的消化腺体,是新陈代谢最旺盛的器官,担负着极其重要而复杂的功能,如:合成与贮存、分泌胆汁、解毒、防御、造血功能等。肝脏储备功能是评估肝脏潜力大小的指标,反映了肝脏对机体内外环境失衡时的代偿能力。肝脏区别于其他器官,最突出的特点是其强大的再生能力,正常肝脏可耐受切除70%,而不出现明显的生理功能紊乱,这为部分肝切除术治疗肝脏疾病提供了无限的可能性。
对于不同肝功能分级的患者,能否行肝切除手术及手术方式的选择各有不同[1],手术前对患者肝脏储备功能及肝癌可切除性进行正确评估,有助于术中准确把握切肝量,降低肝切除术后肝功能衰竭(PHLF)的发生率。当前,肝脏手术的术前评估方法种类繁多,包含了常规生化检查、临床评分系统、影像学检查结合三维重建技术、动态肝功能等,本文将综述现有临床常用的术前评估方法的优缺点。
1常规生化检查
常规血清学生化检查,是认知肝功能最简单、常用、经济的评估手段。不同的血清学指标可从不同角度反映肝脏功能。目前,在精准医学理念的影响下,联合血清学指标评估肝功能的应用显得更为重要。
1.1 白蛋白(Alb)与血清前白蛋白(PA)
二者主要由肝脏合成,均可一定程度反映肝脏的合成功能,但又各有差异。Alb半衰期较长,3~4周,这就意味着临床血清学测得的Alb水平所反映的肝功能具有滞后性,Alb的减少还与众多其他因素相关,如:肝细胞本身病变、氨基酸供应缺乏、蛋白消耗增加、胃肠道丢失等,这些因素降低了Alb对肝功能储备反映的敏感性。相比较而言,PA半衰期短,仅约1.9天[2],对于反映肝合成功能,具有更高的敏感性,且有研究[3]提出,动态观察PA对肝病预后的判断有重要价值,但仍存在许多影响PA的因素,如创伤、感染、胆道疾患、肝脓肿等。
1.2 胆红素
胆红素反映了肝细胞的摄取、结合、转化和排泄功能,既是肝细胞损伤也是肝功能的指标,分为结合胆红素与非结合胆红素,单纯前者升高多见于胆道梗阻性疾病,单纯后者升高多见于溶血性疾病,二者均明显高于正常值则提示肝细胞性黄疸。可见,胆红素反映肝功能的准确性受到溶血、胆道梗阻等因素的影响。
1.3 透明质酸
透明质酸本质是由肝组织间质细胞产生的黏多糖,在肝窦内皮细胞可降解为乙酸和乳酸,有肝脏疾患尤其是肝硬化的患者,血清透明质酸明显升高,与肝损伤的程度具有明显的相关性。因此,血清中透明质酸的水平,反映了肝内皮细胞的功能,尤其对诊断肝纤维化程度和肝硬化程度有较高的临床意义。血清透明质酸的正常值<120.0 ng/mL[4],有学者提出血清透明质酸水平值大于400 ng/mL作为肝损伤的标准。Wang等[5]研究中将透明质酸与磁共振相结合的成像技术HA-Target-Cy5.5-DOTA-Gd (HTCDGd),可用于肝纤维化的准确分期。
1.4 Ⅳ型胶原7S
Ⅳ型胶原是一种基底膜蛋白,位于肝窦周围,是基底膜的免疫组织化学标志。在正常肝脏中,窦没有基底膜,然而,当肝脏发生纤维化时,出现毛细血管化,基底膜出现,基底膜中Ⅳ型胶原7S在血液中开始升高。Ishii等[6]对其的研究发现,对于术后肝功能的长期恢复,术前Ⅳ型胶原7S≤6 ng/mL组的恢复时间明显短于术前Ⅳ型胶原7S>6 ng/mL组,术前Ⅳ型胶原7S是预测术后早期发生PHLF及影响术后肝功能恢复的独立危险因素。因此,术前Ⅳ型胶原可用于预测不同亚群肝切除术患者的早期肝衰竭和术后肝功能的长期恢复。
1.5 其他血清学指标
ALT和AST是肝损伤的标志,与肝细胞坏死相关,肝损伤程度越高,肝酶可随之升高,但肝酶的升高水平并不能准确的反映肝功能。肝脏可合成多种凝血因子,如Ⅴ、Ⅶ、Ⅷ、Ⅸ、Ⅹ、Ⅺ和Ⅻ,因此血液中凝血因子的高低可一定程度反映肝脏功能。凝血酶原时间(PT)、国际标准化比值(INR)是目前常用的肝功能指标,多与其他指标联用或作为评分系统中的项目使用。抗凝血酶Ⅲ是一种由肝脏产生的糖蛋白,可灭活凝血系统中的部分酶,Mizuguchi等[7]对158例接受肝切除术的肝细胞癌患者的研究发现,抗凝血酶Ⅲ与Alb、胆红素、PT、吲哚菁绿15 min滞留率(ICG-R15)等肝功指标存在一定的相关性。此外有报道,Mac-2结合蛋白糖基化异构体、Ⅰ型胶原、基质金属蛋白酶组织抑制剂等血清学指标对于预测术后PHLF的发生具有一定的临床意义。
2影像学评估方法
2.1 超声扫描技术
超声是肝脏疾病的初筛手段之一,临床常用的超声技术见表1。
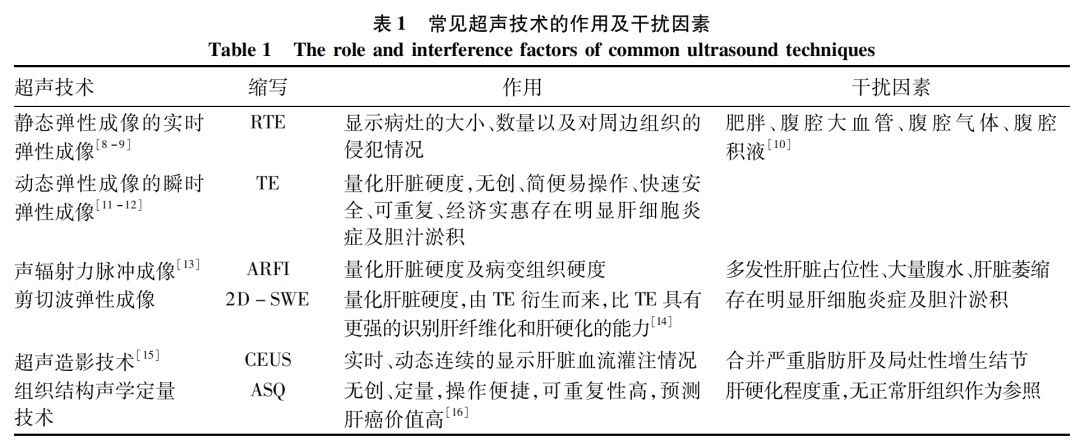
2.2 CT及三维重建技术
术前肝功能和残肝体积对术后肝功能恢复影响很大,术前测定残肝体积有助于预测PHLF的发生。通过CT灌注成像技术以及三维重建技术可以测量肝脏总体积及肿瘤体积,并相对准确地计算出残肝体积,达到术前评估肝癌可切除性的目的[17]。三维重建技术的广泛应用也得益于目前“精准肝切除术”理念的发展,近年来,研究[18]显示CT三维重建技术可直观、清晰显示肝脏解剖结构及肿瘤情况,判断肿瘤与肝内血管、胆管等其他复杂管道的侵犯情况,从而获得更为精确地术前评估。郭智辈等[19]对120例接受腹腔镜肝切除手术治疗患者的研究显示,术前对肿瘤体积采用CT三维重建技术评估,可显著减少术中出血、缩短患者住院时间,观察组预切除肝体积、实际切除肝体积显著低于对照组,剩余肝体积显著大于对照组,而预估病灶体积、实际病灶体积与对照组无明显差异。Lamadé等[20]研究表明,与二维图像相比,医生利用三维图像进行肿瘤的术前评估,对肿瘤定位的准确性可提高37%,手术切除范围的准确性提高了31%,提示三维重建技术对提高手术成功率及改善患者预后具有重要的临床意义。李连海等[21]对20例患者进行术前三维重建、制订手术方案的研究中,也有成功通过术前三维重建达到增加术后功能性肝体积及残肝分数的案例。
总之,三维重建在肝切除术中具有重要的临床应用价值,尤其是以下情况:(1)肿瘤部位特殊,可能侵犯重要血管及胆管者;(2)肝硬化程度重,肿瘤体积较大,预计切肝分数大者;(3)可能术中行血管重建者。而对于肝脏边缘性、小体积肿瘤,三维重建意义不大,对于肝脏密度严重不均或肝硬化程度较重者,还要结合ICG残留率、血清学检查、Child-Pugh评分及ALBI评分等其他评估手段。
2.3 钆塞酸二钠(Gd-EOB-DTPA)增强的MRI
Gd-EOB-DTPA是一种肝胆特异性MRI对比剂,肝功能正常者,Gd-EOB-DTPA约50%由胆道排泄,50%由肾脏排泄。最早在1993年,Yokoyama等利用Gd-EOB-DTPA动态增强的MRI尝试评估肝功能,并在动物模型中得以验证,其较高的软组织分辨能力,为节段性肝脏体积的测定提供了可能,实现对肝脏局部和整体功能的评估,从而提高肝切除手术的安全性[22-24]。Yamada等[25]对Gd-EOB-DTPA的研究提出,肝切除安全范围的公式为“70×(SLF-962)/1 076(%)”;有研究[26]表明,Gd-EOB-DTPA增强的MRI可以准确预测肝大部分切除术的PHLF。Barth等[27]报道,Gd-EOB-DTPA增强的MRI还可以用于预测门静脉栓塞术后残肝生长情况。在肝硬化患者中,肝细胞吸收Gd-EOB-DTPA减少,胆道排泄减少,导致肾脏代偿性增加,因此对比剂滞留在血液中的时间延长,肝胆期门静脉信号强度增高,提示其在肝硬化程度评估中的作用。Sourbron等[28]研究提出,Gd-EOB-DTPA增强的MRI较CT检查在鉴别病变良恶性中具有更高的准确性。肝细胞摄取及胆道排泄过程中胆红素与Gd-EOB-DTPA相互竞争,高胆红素血症导致Gd-EOB-DTPA滞留在血液中的时间延长[29],提示对于高胆红素血症患者,Gd-EOB-DTPA的应用具有一定的局限性。
总之,该方法可提供同时进行结构和功能评估的双重服务,且无辐射,具有良好的临床应用价值,但其扫描时间长且价格昂贵,以及缺少标准化测量方法的问题仍需进一步解决。
3临床评分系统
3.1 Child-Pugh评分系统及其改良
Child-Pugh评分系统是最常用的临床评分系统,是1964年由Child和Turcotte提出,1974年由Pugh改进,包括血清胆红素、Alb水平、血浆PT、肝性脑病及腹水,前三者为血清学定量指标,后两者由人为判断而得。一般来说,对于评分A级患者,行肝癌肝切除术比较安全,对于B级患者,需综合评估患者的其他手术影响因素后选择手术方式,对于C级患者,不建议行手术治疗或需先行降级保守治疗。近年来,不乏有研究[30]表明,对于评分A级患者,也有发生PHLF的可能,而对于评分B、C级患者,也有术后实际肝功能恢复良好的案例,表明该评分系统仍具有一定的局限性:(1)对于无肝硬化者,分级效果差,实际肝功能反映度低;(2)评分系统中存在两项主观性指标,易造成评估误差。有研究者[31]提出纳入血清PA而去除肝性脑病及腹水的改良Child-Pugh评分系统(MCP)(表2),其客观性可一定程度弥补原评分系统的缺点。
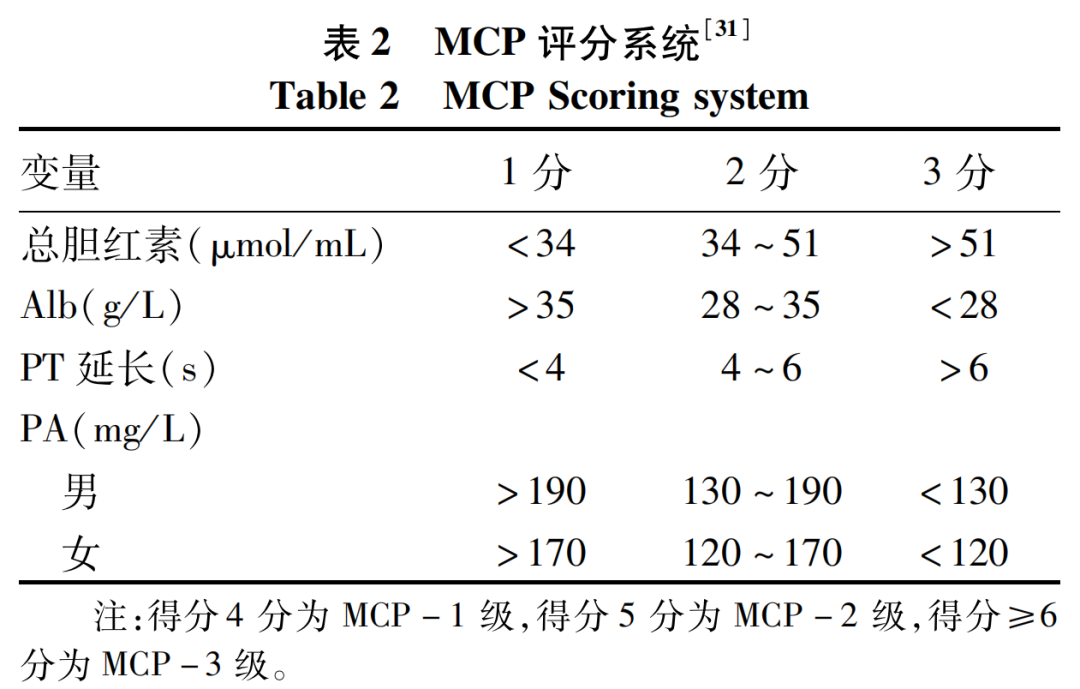
3.2 白蛋白-胆红素评分(ALBI)
考虑到Child-Pugh评分系统存在一定缺陷,Johnson等[32]于2015年用统计学方法对1 313例肝细胞癌患者生存资料分析后建立了新型的肝功能评价模型——ALBI评分,ALBI评分=0.66×lg[总胆红素(μmol/L)]-0.085×[(Alb(g/L)], 将肝功能分为3个等级,ALBI评分≤-2.60分为1级,-2.60分<ALBI评分≤-1.39分为2级,ALBI评分>-1.39分为3级。ALBI评分被广泛用于预测病毒性肝炎、肝硬化、胆管炎、肝衰竭、原发性肝癌患者术后的预后。Tsilimigras等[33]对706例肝内胆管癌(ICC)患者切除术后的预后研究发现,术前ALBI评分对于预测ICC患者术后90天病死率、总生存期具有很高的预测价值。Zou等[34]研究证明ALBI分级可预测PHLF的发生, 且随着ALBI分级增加而增加。Ma等[35]研究表明术前、术后ALBI评分可用于预测早期肝癌患者的总生存期。ALBI评分较Child-Pugh评分系统分级更为详细,避免主观性的指标,且指标便捷易得,其劣势在于Alb、胆红素指标一定程度受到患者营养状态、胆道阻塞的影响,且无法反映终末期肝病患者多器官衰竭的严重程度,因此有研究者[36]提出该评分需与早期肾功能损害的相关指标相结合。越来越多的研究表明ALBI评分比Child-Pugh评分具有更高的临床预测价值,术前、术后利用ALBI评分评估患者肝功能情况,对于提高肝切除术临床疗效有重要意义。
4动态肝功能测量
4.1 ICG清除试验及其他临床常用定量试验
动态肝脏功能定量试验,是借助一些无害的外源性物质,通过静脉注射的方法,测定肝脏对其的清除和代谢能力,以量化肝脏功能储备。临床常用的有ICG清除试验、利多卡因代谢试验和呼气试验等。ICG清除率试验是一种广泛使用的动态肝功能测试,ICG是一种荧光染料,被肝脏选择性摄取并通过胆汁排出,经静脉注射0.5 mg/kg后,健康肝脏约20 min内排出97%的染料。ICG清除率可以通过使用光学经皮传感器的血清取样或脉冲染料密度测定法在围手术期或术中确定[37]。ICG清除率常用指标为15 min后保留的ICG百分比(ICG-R15),或ICG血浆消失率(ICG-PDR)。ICG-R15≤15%和15 min后ICG-PDR≥ 18%/min通常见于健康肝脏。ICG-R15值越高或ICG-PDR值越低则表明PHLF的风险更高,这与肝切除的程度有关,一般认为正常肝功能ICGR15≤10%,可耐受两个或更多的肝段切除术,随着ICG-R15的升高,需慎重考虑肝切除的可行性及切肝体积[38]。ICG在预测PHLF、肝功能失代偿(即术后3个月腹水,生活质量和生存率受损)和病死率方面的准确性已在肝硬化、肝细胞癌以及肝门周围胆管癌患者中得到证实[39-40]。然而,ICG预测非肝硬化患者PHLF的准确性较低[41],因此,该试验应更广泛的应用于肝硬化患者。此外,剩余肝脏体积的ICG清除率比肝脏体积更加能够预测术前门静脉栓塞(PVE)后PHLF的发生率[42]。该试验优点为对人体不会产生刺激,不良反应及过敏现象少,且操作简便。然而,ICG清除试验还受到肝血流量、肝内分流情况、血清胆红素水平、胆道梗阻情况等的影响,这些情况会降低ICG清除试验的可信度[43],此外,ICG清除试验反映的是整体肝功能,若考虑到肝脏各区域功能的不均一性,ICG-R15对肝功能的评估也有所差异。白蛋白-吲哚菁绿评估系统(ALICE)是肝硬化和肝细胞癌患者的分级系统,它结合了血清Alb水平和ICG-R15值,公式为:0.663×log10(ICG-R15[%])-0.071 8×Alb(g/L)。有研究[44]证实,ALICE能够预测肝细胞癌肝切除患者的PHLF和病死率,这也在胆道癌患者中得到验证。
4.2 核素肝功能检查
4.2.1 99锝m标记的半乳糖基人血清白蛋白(99Tcm-GSA)显像
GSA是一种去唾液酸糖蛋白类似物,可与肝细胞中的特异性受体相结合,在肝脏中滞留约30 min,静脉注射后,利用γ相机并通过平面动态核素显像计算该物质在肝脏中的摄取和血液清除率,从而对肝脏储备功能做出评估。有研究者[45]将99Tcm-GSA显像与SPECT/CT相结合用于评估剩余肝脏体积的储备功能,可以很好地预测PHLF等术后并发症的发生及ALPPS的术后评估[46]。Tokorodani等[47]利用该方法计算出肝脏的平均摄取率(SUVmean), 并提出SUVmean>6.7能准确预测严重肝纤维化。此外,有研究[48]发现,由于GSA仅可被肝细胞吸收而不受血清胆红素水平的影响,因此GSA可用于合并胆管病变或胆汁淤积患者的肝功能评估及PHLF预测,可惜的是,GSA的获取困难限制了该技术的发展。
4.2.2 99Tcm-甲溴苯宁肝胆显像(HBS)
亚氨基二乙酸(IDA)的吸收、排泄、不经肝脏转化的特性与ICG类似。甲溴苯宁是最具有肝脏特异性的IDA衍生物, 可被肝脏特异性蛋白所摄取[49],且具有较高的肝脏摄取率,受胆红素影响小、经肾脏排泄少,这决定了它可以成为一种理想的肝功能评估方法[50]。静脉注射99Tcm-甲溴苯宁后, 通过动态闪烁成像计算出肝脏的相对摄取比率并以体表面积进行校正,结合SPECT/CT可对肝脏各节段功能进行精准评估。HBS优势在于可行肝脏整体及局部功能评估、可结合SPECT/CT行体积评估,考虑到了肝功能的不均匀性。然而Gupta等[51]提出,高胆红素血症与低Alb血症对HBS准确性的影响仍需更多的临床研究去探讨。
5人工智能评估
近年来,人工智能在医学影像学领域飞速发展,契合精准外科发展理念,智能影像组学、机器学习与深度学习是目前研究热点。
5.1 智能影像组学
2012年荷兰学者Lambin[52]第一次提出影像组学的概念,即从大量的影像学图像中采集相关影像学特征,利用自动化特征数据提取算法,将其与临床数据、基因数据相对比,挖掘出高度代表性的影像组学特征,从而对肝癌的病理分级及分型、分化程度、预后预测等作出定量评估,其评估流程主要包括图像采集、图像分割、特征提取、数据分析、模型构建等步骤。传统的影像学诊断依靠影像医师的临床经验及鉴别能力,智能影像组学可提高临床医师的工作效率,其诊断准确性甚至可优于影像医师[53]。Chen等[54]基于影像组学构建的肝细胞癌分化程度预测模型具有较高的预测价值。Yang等[55]利用影像组学对肝细胞癌患者微血管侵犯的风险进行了准确的术前评估,人工智能可识别图像中人肉眼无法识别的多种信息,因此对于患者的预后有更高精度的预测[56]。然而,图像采集、数据处理及分享等方面尚无统一的标准,限制了该技术的发展,未来仍需更多的多中心实验去加以探索。
5.2 机器学习与深度学习
基于人工智能的机器学习是将人体大脑的思考能力赋予计算机,并利用其庞大的数据处理能力,发掘疾病与临床数据的内在联系,从而帮助临床医师提高工作效率[57]。深度学习是当前最热的机器学习分支之一[58],卷积神经网络是深度学习模型最重要的算法之一[59],近年来不乏有研究者利用3D卷积神经网络方法对肝脏及肝脏肿瘤成功进行了精准分割,对于肝癌的诊断和治疗具有重要的指导作用。除此之外,深度学习还被广范用于肝纤维化分期、优化影像学诊断、肿瘤分级、肝癌早期诊断等研究中。未来,随着人工智能的发展,期待可以出现人工智能主导的“一站式”肝癌诊疗系统。
6总结与展望
如何准确、全面的评估肝脏整体及局部的储备功能,是肝脏手术术前准备的重中之重。在精准医学理念的影响下,对肝脏细致入微的评估,关乎患者手术的成功与否及生存获益,而降低PHLF的发生率,是肝脏手术治疗的直接目标。肝功能评价方法百花齐放,各有利弊,将多种检查方法相结合,取长补短,是目前肝功能评估最行之有效的策略。目前临床常用Child-Pugh评分来选择手术患者,结合动态肝功能测量、影像学分析、常规生化检查来进行手术决策,随着新兴人工智能的引入,肝功能评价体系将朝着更加精准化、智能化、个性化的方向发展。
参考资料
http://www.lcgdbzz.org/cn/article/doi/10.3969/j.issn.1001-5256.2023.05.034
裴俊鹏, 丁佑铭. 肝切除术前肝储备功能的评估方法[J]. 临床肝胆病杂志, 2023, 39(5): 1219-1226


