工程化靶向性抗体融合蛋白的研究进展
时间:2023-01-05 12:02:05 热度:37.1℃ 作者:网络
前言
自从35年前FDA批准首个治疗性抗体以来,抗体产品在医药市场上获得了迅猛发展。在单克隆抗体成功的基础上,最近的研究利用了抗体良好的特异性和药代动力学特性来创造新的抗体融合蛋白,能够靶向传递治疗有效载荷。
目前,已有几种抗体融合蛋白被批准作为治疗药物。早在1998年,依那西普(TNFR2与Fc结构域的融合)就被批准用于治疗类风湿关节炎。自该批准以来,抗体融合蛋白通过将各种有效载荷,如细胞因子、毒素、酶、神经保护剂和可溶性细胞因子陷阱等连接到不同的抗体成分,包括全长抗体、Fc结构域、单链片段(scFvs)、单域抗体(sdAbs)和抗原结合片段(Fabs)。本文我们一起来关注这些抗体融合蛋白最新的临床前和临床研究进展。
肿瘤靶向的细胞因子抗体融合蛋白
免疫细胞因子作为癌症治疗药物已得到广泛地研究。最近,细胞因子抗体融合蛋白成为研究的热门领域,包括IL-4、IL-15、TNFα、IL-2、IL-12、IL-21、IFN-α和IFN-β等。这些细胞因子在体内稳态中具有免疫刺激、免疫抑制或多效性作用。

为了将细胞因子有效载荷传递到肿瘤微环境(TME),最近开发的免疫细胞因子结合了靶向细胞外基质(ECM)成分的抗体,特别是与疾病相关的纤维连接蛋白亚型。其中一种抗体名为F8,识别纤维连接蛋白的额外结构域A,它在炎症部位的新生血管中高表达,但在大多数健康组织中检测不到。F8的几种细胞因子融合蛋白已在癌症的临床前和临床上取得了成功。
另一种ECM靶向抗体称为L19,它与纤维连接蛋白的额外结构域B结合,从而能够选择性定位到肿瘤相关血管。最近,包含TNFα、IL-12或IL-2的L19单链抗体融合蛋白已证明具有抗肿瘤功效。目前,L19-TNFα、L19-IL12和L19-IL2正在临床试验的各个阶段进行探索,作为单一疗法或与其他癌症疗法联合。
另一种肿瘤靶向策略是利用坏死肿瘤区域中发现的游离DNA片段。例如,结合组蛋白的人lgG1抗体NHS76与IL-12融合,以增强肿瘤定位。NHS-IL12与放疗、化疗、癌症疫苗或免疫检查点抑制具有协同作用,显示了其在联合治疗方法中的治疗潜力。在第一阶段临床试验中,发现NHS-IL12具有良好的耐受性和免疫刺激性。目前,集中于将NHS-IL12与其他癌症治疗相结合的联合疗法。
其他免疫细胞因子融合方式也被用于向TME靶向输送促炎细胞因子。对于其中许多方法,降低了细胞因子的亲和力来确保抗体靶向而不是细胞因子指导融合蛋白的定位。例如,PD-1抗体与亲和力受损的IL-21变体融合,以将IL-21传递给PD-1表达的T细胞,同时最小化对局部抗原提呈细胞的非靶向影响。
炎症靶向的细胞因子抗体融合蛋白
由于其固有的炎症部位定位,ECM靶向抗体也被用于将抗炎细胞因子活性导向慢性炎症和自身免疫性疾病的炎症部位。
在最近的进展中,包含IL-4、IL-9、IFN-α和IL-10的新型免疫细胞因子已在临床前用于治疗慢性炎症和自身免疫性疾病。在胶原蛋白诱导的关节炎小鼠模型中,F8-IL4与地塞米松联合使用,可完全治愈该疾病。在实验性肺动脉高压小鼠模型中,F8-IL9-F8降低了右心室收缩压并改善了超声心动图参数。
作为基于ECM靶向的替代方法,以Clec9A为靶向的单域抗体成功地将IFN-α活性定位到Clec9A+DC,从而改善多发性硬化症小鼠模型的症状,而没有与可溶性IFN-α相关的毒性。在另一项研究中,融合到Fc结构域的抗CD86单链抗体与IL-10的融合蛋白诱导了CD86+耐受性DC的分化,可用于治疗移植物抗宿主病(GVHD)。
信号偏向性细胞因子抗体融合蛋白
结构导向分子工程的发展促进了有偏向性的细胞因子设计,这些免疫细胞因子可以调节整合细胞因子的活性。其中IL-2是目前研究最活跃和最领先的免疫细胞因子。
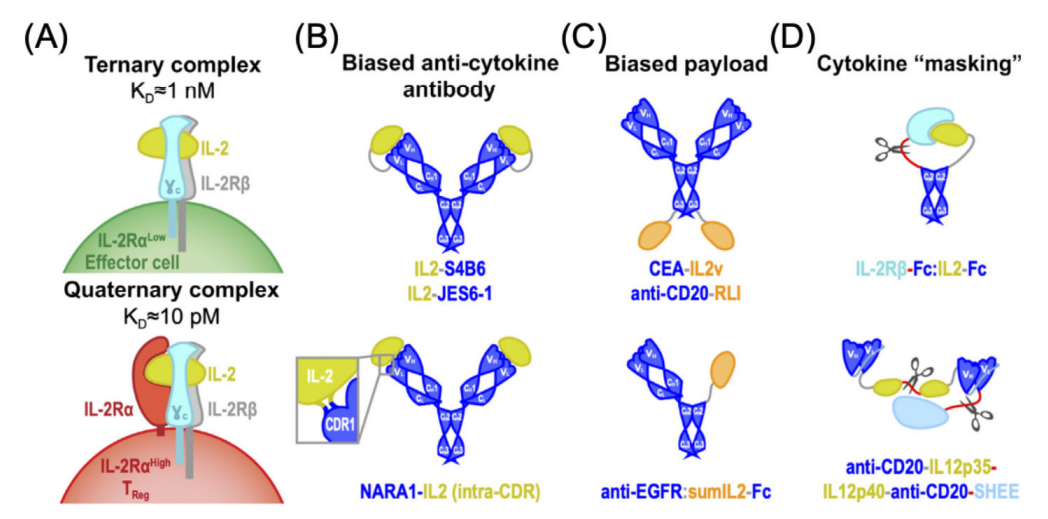
由于IL-2在协调免疫反应中的重要作用,它已被用于治疗癌症和自身免疫性疾病。IL-2可以通过IL-2Rβ和γC链的异二聚体受体或IL-2Rα、IL-2Rβ和γC链的更高亲和力的三聚体受体传递信号。与效应T细胞相比,Tregs高表达IL-2Rα,因此对IL-2具有极高的敏感性。Boyman等人开发了一种抗IL-2的抗体(S4B6),选择性地将IL-2活性导向效应细胞。S4B6抗体使IL-2活性偏向于效应细胞的扩增,IL-2/S4B6复合物在小鼠中具有强大的抗肿瘤活性,而不会引起全身毒性。另一种IL-2的抗体JES6-1诱导小鼠优先Treg的扩增,IL-2/JES6-2复合物用于治疗I型糖尿病和其他自身免疫性疾病。
IL-2的突变也可以产生偏向性,可与针对疾病抗原的抗体融合。例如,将IL-2突变后去除了与IL-2Rα的结合能力,然后融合到抗癌胚抗原(CEA)抗体,CEA-IL-2v抑制了肿瘤生长并提高CEA+荷瘤小鼠的存活率。此外,在CEA+结肠癌小鼠模型中,发现CEA-IL2v与CEA靶向嵌合抗原受体(CAR)T细胞协同诱导肿瘤完全根除,并产生保护性免疫。另一融合蛋白用突变IL-2取代抗EGFR抗体的一个Fab臂,突变IL-2降低了IL-2Rα结合活性,由此产生的分子抑制了黑色素瘤小鼠模型中的肿瘤生长。
细胞因子的结构阻滞或“掩蔽”也可以改善偏向性。例如,效应细胞偏向的IL-2变体和IL-2Rβ细胞外结构域(ECD)分别融合到Fc结构域,使得IL-2Rβ链结合并“遮蔽”融合的IL-2,其通过可切割连接子连接到各自的Fc结构区。因此,在肿瘤相关基质金属蛋白酶存在的情况下,选择性地释放掩蔽的IL-2,使该分子表现出优于IL-2的疗效,并与检查点阻断疗法产生强大的协同作用。
免疫毒素(RIT)抗体融合蛋白
RIT是免疫毒素与抗体片段的融合,RIT的抗体部分发挥导向作用,将毒性有效载荷靶向患病细胞。毒性成分可按其细胞毒性机制分类:穿孔毒素(PFTs);核糖体失活蛋白(RIPs)和微管破坏蛋白(MDPs),它们阻止有丝分裂和囊泡转运,从而促进细胞凋亡。

RIPs是RITs中使用的最多样化和最广泛的毒素类别,而MDPs是最少的。这两种类型都需要RIT的抗体部分,以促进内吞作用,从而实现细胞杀伤。相比之下,大多数PFT直接与细胞膜结合,因此不需要抗体介导的内吞作用来发挥细胞溶解功能。
目前正在临床试验或经FDA批准的RIT都是RIPs,包括铜绿假单胞菌外毒素A(PE)、白喉毒素(DT)和志贺毒素1(Stx1)。两种临床上最领先的RIT,moxetumomab pasudotox(LUMOXITI:registered:)和oportuzumab monatox,均含有优化后的PE。在临床试验中有几个分子使用DT作为有效载荷,被优化用于RIT。此外,只有一个Stx1有效载荷RIT正在临床试验中。RIT面临的一个重大挑战是,许多患者产生了针对毒性部分的抗抗体,从而严重阻碍治疗效果。此外,由于大多数RIT无法充分穿透实体肿瘤,许多免疫毒素的大小限制了其在肿瘤学中的临床应用。
到目前为止,绝大多数研发和优化工作都集中在外源毒素上,但颗粒酶B和颗粒溶素等内源性RIP毒素最近已经在临床前开发,并且由于它们没有免疫原性,因此极具吸引力。另一种RIT方法是针对肿瘤的改良超抗原(SAg)。与其他直接破坏细胞功能的毒素不同,SAgs招募并激活T细胞以杀死靶细胞。总的来说,RIT在有针对性地消除癌细胞方面显示出巨大的前景。
抗体酶融合蛋白及其他新型方法
抗体导向酶前体药物治疗(ADEPT)是另一种新型策略,在该策略中,连续给予以癌症为靶点的抗体酶融合蛋白和酶激活前体药物。与大多数RIT相比,ADEPT融合蛋白中的抗体不触发受体介导的内吞作用,因为酶必须留在细胞外才能获得前体药物。由CEA特异性抗体片段和细菌羧肽酶G2(CPG2)组成的融合蛋白MFECP1,在早期临床试验中显示出良好的安全性并局限于患者肿瘤,但免疫原性是一个问题。ADEPTS的临床前开发仍在继续,但临床转化需要克服免疫原性挑战。
抗体酶融合蛋白是另一类已进入临床试验的新型分子,这些融合蛋白中的抗体有助于将酶有效载荷运输到溶酶体,在溶酶体中,它们取代已突变的酶来治疗遗传疾病,如庞贝病和粘多糖病。一种抗体融合蛋白VAL-1221将抗体介导递送技术与重组人类酸性α-葡萄糖苷酶(rhGAA)相结合,促进将rhGAA递送至肌肉,降解从溶酶体泄漏的糖原。目前,VAL-1221正在进行临床开发用于治疗晚发性庞贝氏症患者。
其他抗体酶融合蛋白,例如HIRMAb酶融合蛋白,除了促进通过人类胰岛素受体(HIR)的内吞作用外,还促进跨血脑屏障的转运。这些分子在临床前研究以及早期临床试验中均显示出良好的前景。
小结
基于抗体的融合蛋白已显示出非凡的临床价值,创新的分子修饰、融合形式和临床前开发中蛋白质有效载荷的爆炸性增长都预示着抗体融合蛋白的进一步迅猛进展。基于抗体的靶向性可以显著提高有效载荷的效力,并防止不良副作用。与抗体融合的蛋白质有效载荷也表现出肾清除率降低和循环半衰期延长,减少了重复给药的需要。
目前,临床上研究最领先的分子主要专注于肿瘤学应用,但基于免疫细胞因子和RIT的感染性、慢性炎症和自身免疫性疾病的治疗肯定很快就会出现。用于治疗神经系统疾病和遗传性退行性疾病的抗体融合蛋白相信也即将出现。抗体融合蛋白治疗的前景广阔。
参考文献:
1.Engineered antibody fusion proteins for targeted disease therapy. Trends Pharmacol Sci. 2021 Dec; 42(12): 1064–1081.
: , 。 视频 小程序 赞 ,轻点两下取消赞 在看 ,轻点两下取消在看


