Nat Biotechnol:IL-2开发前沿:一种条件性激活减毒的IL-2模拟物
时间:2022-12-08 14:59:27 热度:37.1℃ 作者:网络
免疫刺激性细胞因子是免疫系统的中枢调节因子,具有作为免疫治疗药物的巨大潜力。然而,其临床应用受到全身免疫激活产生的严重毒性的限制。IL-2是一种被批准用于治疗黑色素瘤和肾细胞癌的强效多效细胞因子,然而受到CD25+细胞的优先激活和全身性剂量限制毒性的影响,限制了其临床应用。
最近,计算机蛋白质设计的最新进展使得能够产生高度稳定的功能性蛋白质,其完全具有天然细胞因子的活性,而且改善了生化和治疗特性。一种新设计的IL-2模拟物(Neo-2/15)通过激活IL-2Rβ和IL-2Rγ来复制IL-2和IL-15的免疫刺激功能,但完全独立于CD25和CD215受体。与天然IL-2相比,这种模拟物通过避免CD25+免疫细胞的优先激活,诱导了毒性降低的有效免疫治疗。其聚乙二醇化的版本(NL-201)已在多个临床前模型中显示出改善的治疗效果,目前正在临床试验中进行测试。
在Neo-2/15蛋白中,有4个螺旋结构,其中螺旋H3与IL-2Rβ相互作用,H4与IL-2γ相互作用,H1与两种受体相互作用。研究人员测试了Neo-2/15的几种分裂版本:(1)H1和H3–H2–H4,(2)H1–H3和H2–H3,以及(3)H1–H3–H2和H4。在所有三种情况下,当两个片段组合时,观察到比单独两个片段更强的IL-2受体结合和信号传导。而对于分离对H1和H3-2-4,即使在高浓度下,两个片段都没有单独显示任何活性。
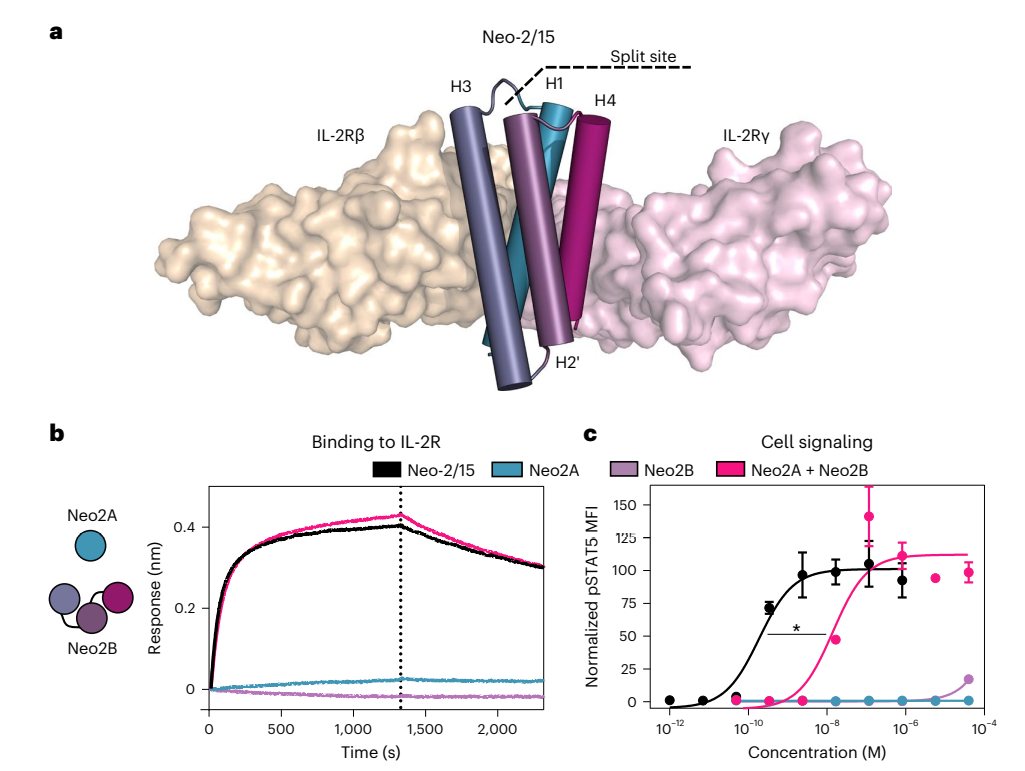
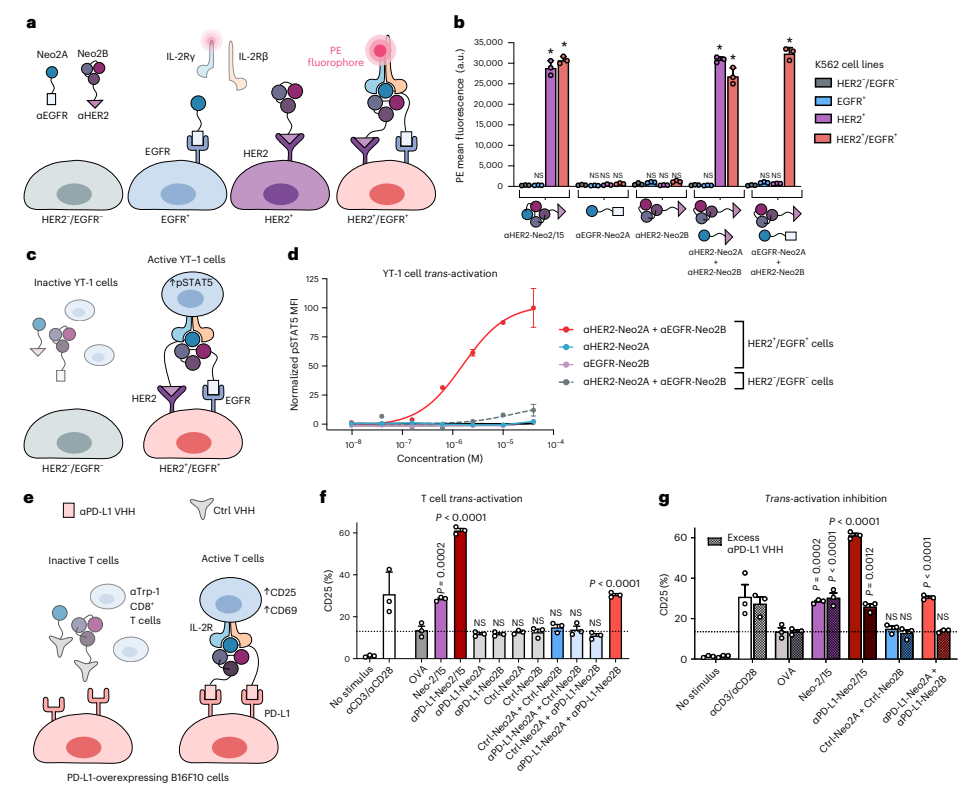
接下来研究人员这些片段分别融合到设计的锚蛋白中,该蛋白靶向HER2和EGFR这两种肿瘤相关抗原的细胞外结构域。通过选择性靶向细胞表面受体来评估Neo-2/15的重组活性。结果显示,当Neo2A和Neo2B都靶向HER2(αHER2-Neo2A + αHER2-Neo2B)时,具有与HER2靶向的完整Neo-2/15(αHER2-Neo2/15)相似的活性,显示共定位依赖性IL-2受体激活。当一个片段靶向HER2而另一个靶向EGFR时,也显示了相似的定位依赖性激活,证明了该方法靶向同一细胞表面上的两种不同抗原的可行性。
接下来,研究人员评估了分裂的Neo-2/15的安全性和治疗活性。IL-2通常在小鼠中显示诱导毒性,如肺水肿和体重减轻。通过给予健康的C57BL/6 J小鼠以等摩尔剂量的Neo-2/15、靶向和非靶向的Neo-2/15融合蛋白(PD-L1-Neo2/15和Ctrl-Neo2/15)以及靶向和未靶向的分裂Neo-2/15融合蛋白,正如预期的那样,完整的Neo-2/15融合蛋白在治疗后几天就被发现有毒性,而分裂的Neo-2/15片段组合在同等剂量下均未显示任何毒性迹象。
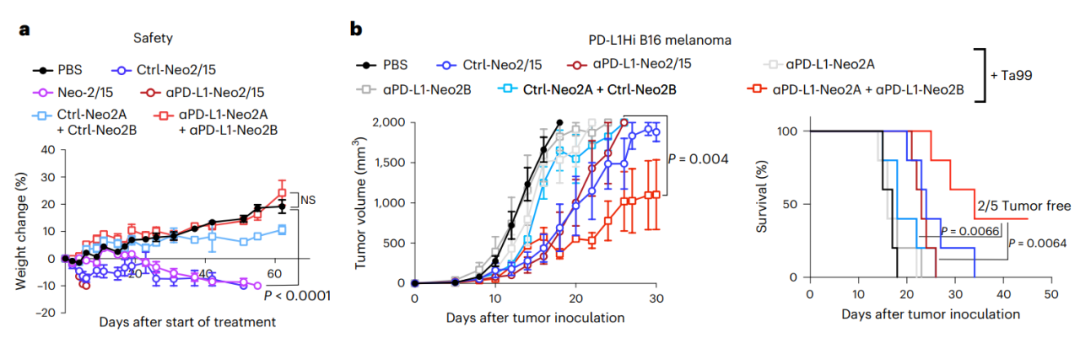
此外,在PD-L1过表达B16黑色素瘤的同基因小鼠模型中,单个片段没有显示出任何抗肿瘤治疗活性。而PD-L1靶向的分裂片段(αPD-L1-Neo2A + αPD-L1-Neo2B)的抗肿瘤作用优于非靶向分裂片段(Ctrl-Neo2A + Ctrl-Neo2B)以及靶向和未靶向的完整Neo-2/15融合蛋白。
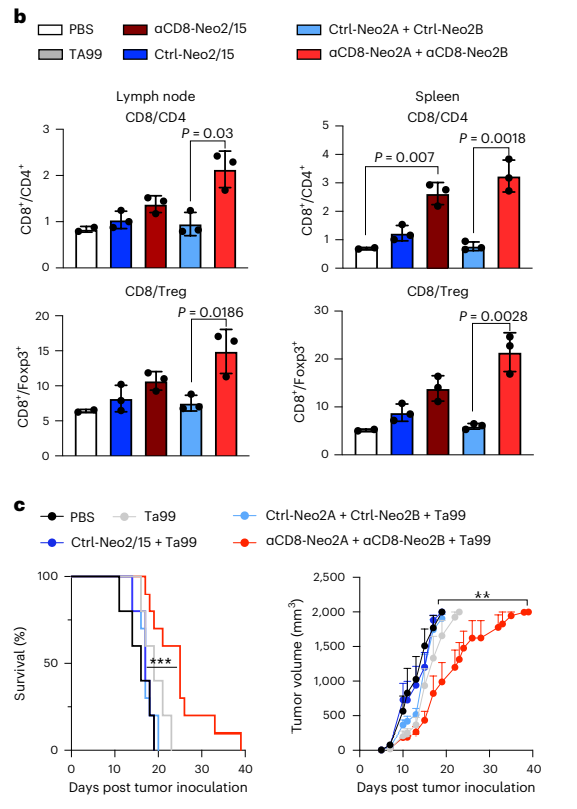
一些免疫治疗策略受益于细胞因子介导的特定免疫细胞亚型的全身扩增,以促进抗肿瘤作,而Tregs限制了许多基于IL-2的免疫疗法。Neo-2/15是CD25非依赖的,因此不偏向于优先激活CD25+细胞。研究人员将分裂的Neo-2/15蛋白融合到一个αCD8纳米体靶向结构域,在健康的Foxp3-GFP小鼠中评估分裂的Neo-2/15、完整的Neo-2-15和非靶向对照的CD8+T细胞选择性扩增的程度。结果显示,与完整的Neo-2/15相比,分类的Neo-2/15融合蛋白显著增加了CD8+细胞的比例。 同时,研究人员评估了CD8靶向分裂Neo-2/15在B16小鼠黑色素瘤模型中的抗肿瘤效果,与未靶向的完整和分裂的Neo-2/15相比,CD8靶向分裂的Neo-2/15导致小鼠肿瘤生长延迟,生存率提高。
总之,上述的分离式Neo-2/15的开发解决了目前IL-2治疗方面的两个主要挑战,即CD25的偏倚和系统毒性。这项研究也显示了计算机从头设计蛋白质的强大功能,同时,这种方法也为新的应用打开了大门。在新的应用中,可以利用从头设计的蛋白质来开发高度特异性的治疗药物,这些药物可以被设计的靶蛋白条件性激活。
参考文献:
1.A split, conditionally active mimetic of IL-2 reduces the toxicity of systemic cytokine therapy. Nat Biotechnol.2022 Oct 31.
: , 。 视频 小程序 赞 ,轻点两下取消赞 在看 ,轻点两下取消在看


