Br J Dermatol:Bimekizumab治疗中重度斑块型银屑病的研究
时间:2022-12-05 08:59:48 热度:37.1℃ 作者:网络

靶向肿瘤坏死因子(TNF)或白介素12/23的生物制剂的引入使大多数斑块型银屑病患者的银屑病面积和严重程度指数(PASI 75)比基线改善了75%。最近,靶向IL-23和IL-17A的生物制剂进一步提高了治疗预期,PASI 90成为一个现实的目标,许多患者也达到了PASI 100(皮肤完全清除)。IL-17A,T辅助细胞(Th)17细胞的标志性细胞因子,IL-17A是一种在银屑病组织中过度表达的促炎细胞因子。有显著的临床证据表明,抑制IL-17A可以迅速缓解银屑病的临床、组织学和分子水平。IL-17F是IL-17A的近亲家族成员,尽管它在诱导促炎症细胞因子如CXCL1(C-X-C基序趋化因子配体1)、IL-8(由CXCL8基因编码)和IL-6方面比IL-17A弱约100倍,但在银屑病皮肤中要丰富得多。越来越多的证据表明,IL-17A和IL-17F通过驱动异常的角质形成细胞生物学,在银屑病的潜在疾病病理生物学中发挥核心作用。角质形成细胞的增殖和IL-36c和IL-17c等因子的释放都会放大炎症和斑块的慢性化。
Bimekizumab是一种有选择性地抑制IL-17A和IL-17F的单抗。体外临床前研究表明,用Bimekizumab双重抑制IL17A和IL-17F的抑制效果比单独阻断任一种细胞因子的抑制效果更大。中重度斑块型银屑病患者的II期研究表明,Bimekizumab的皮肤清除率很高,Q4W维持剂量可以很好地维持这一点。
在这里,我们介绍了一项II期探索性试验的结果,该试验旨在研究延长Bimekizumab维持剂量间隔是否可以获得高的皮肤清除率。以及比马珠单抗治疗是否与银屑病等炎症标志物的分子消退有关。
方法:49例中、重度斑块型银屑病患者在0/4周时服用比卡珠单抗320 mg,16周后给予比卡珠单抗320 mg(n=17)或安慰剂(n=32)治疗。疗效、安全性、药代动力学、免疫原性和活检转录本分析评估至第28周。
结果:治疗8周时,47%的患者银屑病面积和严重程度指数(PASI 100)较治疗前100%改善,12周(第二次治疗后8周)上升至57%,然后下降。在那些在第16周接受Bimekizumab的患者中,PASI100率在第20周增加到类似的峰值水平,但在第28周到41%(第三次注射后12周)下降。在皮损银屑病皮肤中观察到的第8周转录特征迅速正常化到与非皮损皮肤一致的水平,导致分子缓解。角质形成细胞相关基因产物如CXCL1(C-X-C基序趋化因子配体1)、IL-8(由CXCL8基因编码)、CCL20(C-C基序趋化因子20)、IL-36c和IL-17C被深度标准化到与非皮损皮肤相关的水平。
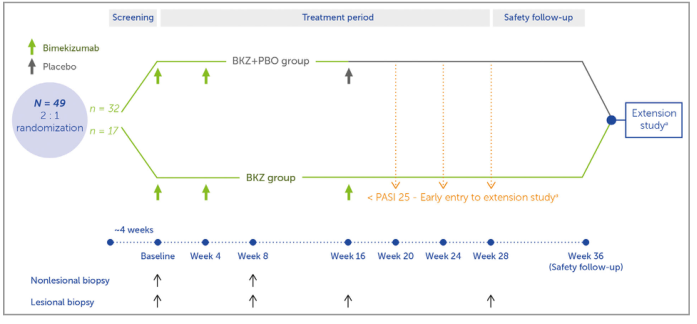
图1 研究设计。研究访问发生在0周(基线)、2周、4周、8周、12周、16周、20周、28周和36周(安全随访)。BKZ+安慰剂(BKZ+PBO)组在0周和4周接受两剂Bimekizumab 320 mg治疗,在16周接受安慰剂治疗;BKZ组在0、4和16周接受三剂Bimekizumab 320 mg治疗。只有在前16周银屑病面积和严重程度指数(PASI 25)较基线改善25%的患者在安全随访后有资格进入扩展研究(NCT03230292);如果这些患者在20、24或28周未能达到PASI 25,他们被允许提前进入扩展研究,并在访问时接受第一剂药物研究。
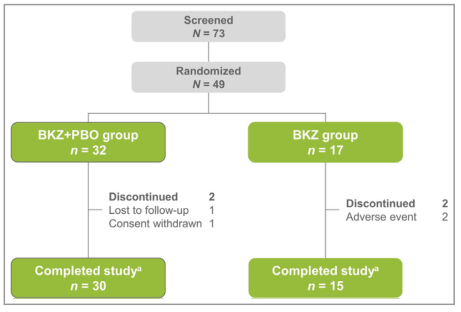
图2 病人的性格。BKZ+安慰剂(BKZ+PBO)组在0周和4周接受两剂Bimekizumab 320 mg,在16周接受安慰剂;BKZ组在0、4和16周接受三剂Bimekizumab 320 mg。研究完成被定义为在第28周结束或在第20、24或28周完成访问并提前进入扩展研究。
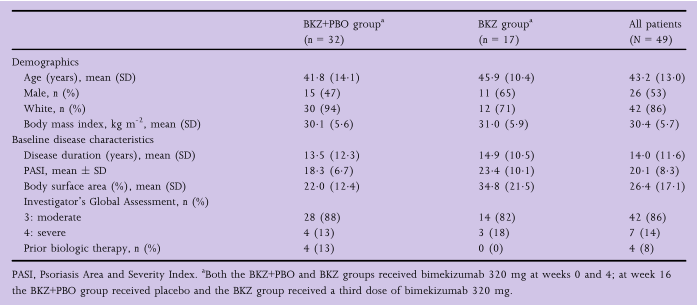
表1 人口统计和基线特征
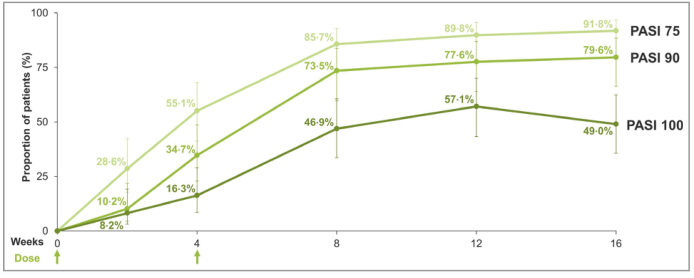
图3 联合治疗组对第16周的银屑病面积和严重程度指数(PASI)反应(无思考插补)。PASI 75\/90/100,≥ 与基线PASI相比,改善75%\/90%\/100%。
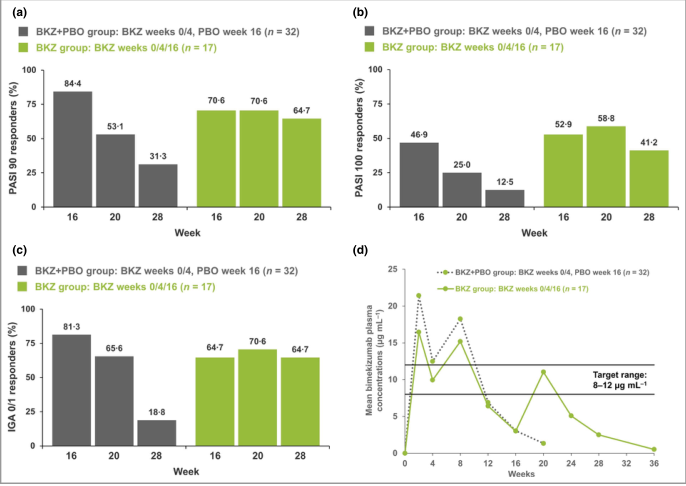
图4 银屑病面积和严重程度指数(PASI)评分和研究者全球评估(IGA)第16、20和28周的0/1反应(无思考插补);bimekizumab加安慰剂(BKZ+PBO)组在第0周和第4周接受两次剂量的BKZ 320 mg,第16周接受安慰剂;BKZ组在第0周、第4周和第16周接受了三剂320 mg bimekizumab。(a)PASI(PASI 90)反应改善了90%。(b) PASI 100响应(总清除率)。(c) IGA 0\/1应答:0分(清晰)或1分(几乎清晰)≥ 相对于基线IGA的2类改善,以5分制评分。(d) Bimekizumab血浆浓度。关于比美基单抗血浆浓度目标范围的基本原理,见图S1(支持信息)。
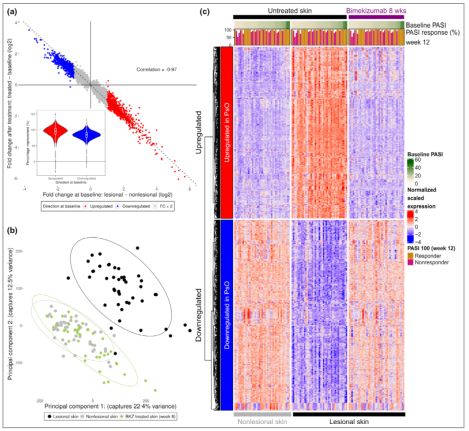
图5 比美基单抗(BKZ)对银屑病(PsO)转录组的分子解析。(a) 散点图比较了基线时和治疗后每个问题的折叠变化(FC),在基线时明显失调。探针在基线处按其方向着色。银屑病问题改善百分比的Violin图插入。(b) 用于将样本转录组投影到两个维度的主成分分析结果(一起解释了数据中35%的全局方差)。(c) 基线和治疗后银屑病转录组中探针表达谱的热图。表达式值按行缩放,首先按方向拆分问题集,然后使用分层聚类进行聚类。样本按基线时银屑病面积和严重程度指数(PASI)评分的升序排列。条形表示第12周的PASI应答百分比,PASI 100应答者(与基线PASI相比改善100%的应答者)进一步以橙色突出显示。
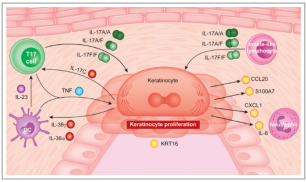
图6 银屑病斑块形成的驱动因素。促炎性趋化因子:CXCL1(C-X-C基序趋化因子配体1)、白介素(IL)-8(由CXCL8编码)和CCL20(C-C基序趋化因子20);上游细胞因子:IL-17A、IL-17F、IL-23A和IL-12B;上皮应激标志物:IL-19、IL-36c和IL-36a;增殖:KRT16;抗菌肽:S100A7.肿瘤坏死因子。T17细胞代表产生IL-17的T细胞(包括细胞毒性T细胞和T辅助细胞)。
结论:在抑制IL-17F和IL-17A的同时,抑制IL-17F可引起快速、深入的临床反应。此外,观察到角质形成细胞生物学和银屑病转录组的深刻正常化,包括8周前IL17和IL23基因表达的正常化。这些数据为在III期临床试验中评估每8周和每4周一次的Bimekizumab维持剂量提供了证据。
文献来源:Oliver R, Krueger JG, Glatt SBimekizumab for the treatment of moderate-to-severe plaque psoriasis: efficacy, safety, pharmacokinetics, pharmacodynamics and transcriptomics from a phase IIa, randomized, double-blind multicentre study.Br J Dermatol 2022 Apr;186(4)


