Nat Rev Bioeng:中山大学左涛团队发表改造肠道微生物群的综述
时间:2023-07-17 17:29:15 热度:37.1℃ 作者:网络
人类胃肠道含有数千种微生物,包括细菌、古细菌、真菌和病毒,它们共同构成了肠道微生物组。近十多年的大量研究已经充分证明了肠道菌群与人体健康和疾病之间的密切联系,其生态失调与许多疾病的发病机制有关,包括癌症、代谢性疾病、自身免疫病和传染病等等。对肠道微生物进行工程改造,以诊断和调节菌群失调,进而促进健康和治疗疾病,这是未来重要的研究和发展方向。肠道微生物组包含超过330万个基因,是人体基因组的150倍,这种遗传复杂性提供了人类基因之外的大量可操纵遗传模块。而也正因为肠道微生物组是一个庞大且复杂的生态系统,针对单一微生物菌株的策略往往是不够的。
为此,对肠道菌群中的一组关键微生物联合体进行生态集体编辑,从而建立一个相互支持和协作的肠道微生物网络可能是更有潜力的方案。
2023年6月16日,中山大学左涛研究员及团队于Nature Reviews Bioengineering在线发表题为“Engineering the gut microbiome”的综述,总结了工程改造肠道微生物组在人类健康和疾病中的应用,并系统深入地讨论了它们的转化潜力,同时也提到了其他改造肠道微生物组的多学科交叉策略,例如胶囊、联合电子设备、正交饮食工程和粪便微生物移植(FMT)等。

常用于基因改造的底盘微生物包括大肠杆菌 Nissle 1917、乳酸菌和双歧杆菌等传统益生菌菌株,其优点是研究相对完善,并可以支持各种 CRISPR/Cas 系统,使其适合异源生产白细胞介素-10,抑制病原体生长和生物传感目的。另外,肠道真菌布拉迪酵母也是常用的底盘菌,经过改造可在哺乳动物肠道中合成小分子。噬菌体也已被用于靶向人体中的有害微生物,并且已设计出不同的策略来提高其抗菌活性并扩大其应用范围。
然而,传统上单独使用单一微生物菌株或少数益生菌菌株对于治疗某些疾病是无效的,因此,从整体上改造肠道微生物群,特别是通过互利合作发挥某一系列特定功能的微生物群,可能是更具有潜力的策略。整体肠道微生物组的工程广泛包括重塑肠道微生物组的组成和生态的任何方法,从天然肠道细菌的大规模遗传改造到外源或合成微生物群落的大规模输入。这种方法比工程化单一微生物更强大,对肠道环境挑战具有更强的抵抗力,由于资源共享和分工而减少代谢负荷,并增强代谢能力。
在这篇综述中,作者重点介绍了对肠道微生物群中多个特定物种进行同时、精准的基因改造技术,包括通过引导 RNA 辅助靶向 (INTEGRATE)、CRISPR转座子介导的 DNA 编辑一体化 RNA 引导 CRISPR–Cas 转座酶 (DART)、CRISPR 干扰和基于接合质粒的 II 组内含子插入转座元件。更广泛的意义上,FMT 和饮食也可以被认为以整体方式“改造”人类肠道微生物组。FMT通过将健康供体的粪便转移到肠道微生物群受到干扰的接受者(例如患有艰难梭菌感染 (CDI)、IBD 和糖尿病的患者)的胃肠道来重建肠道微生物群平衡。正交饮食生态位工程(orthogonal dietary niche engineering,一种基于在饮食中间歇性添加独特营养素以动态调整肠道中感兴趣微生物的存在和丰度的方法)有助于识别能够精确、持久调节肠道的功能性饮食和饮食成分微生物组。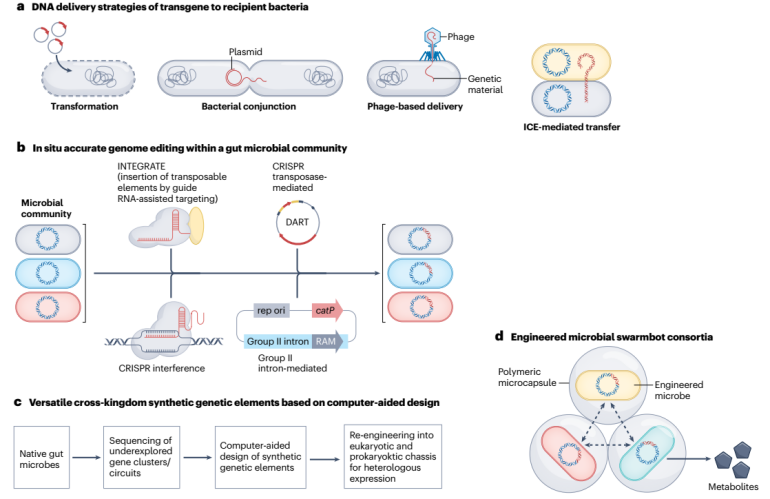
肠道微生物的整体改造策略(图源自Nature Reviews Bioengineering )
目前,工程微生物展现出应用于治疗炎症性肠病(IBD)、癌症、代谢性疾病和传染性疾病的潜力。例如口服分泌 IL-10 的工程细菌会刺激 Treg 细胞并抑制炎症性 TH17、TH1 和 TH2 细胞以及巨噬细胞,从而抑制促炎细胞因子(如IL-17、IL-6、IFNγ和TNF)的分泌。
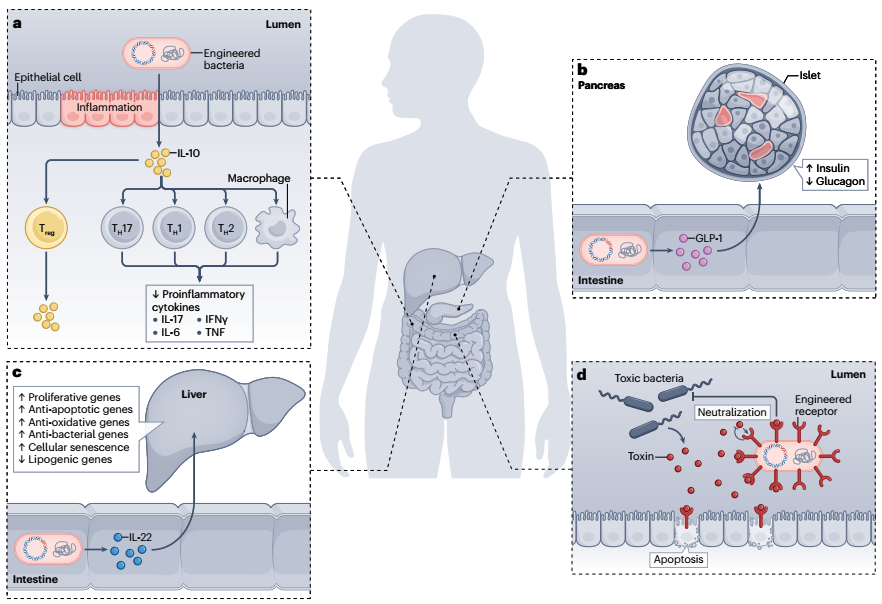
工程微生物治疗疾病的转化应用(图源自Nature Reviews Bioengineering)
在该文中,作者指出,尽管取得了诸多进展,肠道微生物组临床应用面临的挑战包括生物安全性、精确靶向、毒性弱化和稳定定植等。尽管有大量令人鼓舞的临床前研究,但只有少数研究进入人体临床试验。规模人体试验要求工程生物治疗药物在伦理上合理,具有令人信服的生物安全数据,才能获得公众的信任和支持。无法为临床目的生产足够大(且未受污染)的重组治疗微生物,特别是在没有抗生素或其他选择程序的情况下,是使用工程微生物进行人体试验的另一个障碍。大的适应性损失通常与工程微生物中异源蛋白质的产生有关,这可能会阻碍生物量的增加。在没有相当大的选择压力的情况下,引入的基因也可能很快消失或突变。消除这些障碍对于为临床应用铺平道路至关重要。
参考消息:
https://www.nature.com/articles/s44222-023-00072-2


