两大药企有关“超级流感药”之争,是原研药和仿制药之争吗?有的药便宜又救命,却再也没有药厂愿意生产……
时间:2022-10-20 12:00:48 热度:37.1℃ 作者:网络
石药集团流感仿制药获批,
其专利权人罗氏制药发文质疑侵权
就在前天下午,医药界发生了一件大事,引起了一阵热烈的讨论。
罗氏制药在其官方微信公众号发布了《针对石药集团欧意药业有限公司玛巴洛沙韦片仿制药获批事宜的声明》,声明直言石药欧意公司的行为已对罗氏制药就玛巴洛沙韦片的后续研发和商业化工作带来了极大干扰。

在罗氏制药的声明中,我们可以了解到,玛巴洛沙韦片(速福达)及其活性成分受第 ZL201180056716.8 号中国发明专利的保护。该专利涉及化合物专利,效力稳定,有效期直至2031年9月21日届满终止。
该声明表示,依据中国专利法的有关规定,未经专利权人的许可,任何个人或实体不得在中国大陆以生产经营为目的制造、使用、销售或许诺销售玛巴洛沙韦化合物和/或含有玛巴洛沙韦化合物的药品。而该专利的专利权人从未许可除罗氏制药及其关联公司以外的任何个人或实体在中国大陆展开上述行为。
罗氏制药在声明中还表示,速福达在国内获批不过三个月,石药欧意即递交了仿制药上市申请。自2021年7月以来,公司多次就知识产权问题和石药欧意沟通,但石药欧意一方面自认其获批仿制药落入第ZL201180056716.8号中国发明专利的保护范围,另一方面至今拒绝承诺在上述专利保护期内不实施侵犯专利权的行为。
上述声明也特别指出,石药欧意流感仿制药虽然获得了国家药品监督管理局的批准,但这并不意味着欧意公司可以以生产经营为目的制造、销售或许诺销售其仿制药玛巴洛沙韦片,否则将构成对上述专利的侵权。
事件发酵至此,石药欧意目前并未做出任何公开回复。
不明所以的人可能要问,既然玛巴洛沙韦的专利还处于保护期内,并且未得到罗氏制药的授权,那这种仿制药的注册申请是怎么通过的呢?
据相关律师介绍,去年7月4日,国家药监局和国家知识产权局发布了《药品专利纠纷早期解决机制实施办法(试行)》(简称《办法》),其中第六条规定:化学仿制药申请人提交药品上市许可申请时,应当对照已在中国上市药品专利信息登记平台公开的专利信息,针对被仿制药每一件相关的药品专利需作出声明。声明分为四类:

不过,国家药监局药品审评中心(CDE)受理石药欧意玛巴洛沙韦仿制药上市申请的时间为2021年7月1日,在上述办法发布之前,公开渠道也未检索到其相应声明,因此石药欧意对于上述专利的态度尚且不得而知。
一般而言,原研药企知晓仿制药公司的四类声明后,会在规定时间内提起诉讼、向国家知识产权局提起裁决,这一诉讼或裁决可能会持续9个月,此时药监局还在继续进行审批工作,直到诉讼或裁决产生结果。
但倘若9个月过后未产生结果,药监局可以给出批文。换而言之,正是诉讼在9个月内没有结果,导致CDE按照正常流程审批,进而促成该药的获批。
但最重要的问题来了,石药集团这款仿制药虽然获得了药监局的审批,但由于罗氏制药的专利还未到期,很显然,石药集团还不能将此款仿制药进行上市销售。倘若苦等十年等到专利过期,十年之后的情况又将会是怎样的呢?
原研药还是仿制药?
超6成患者对仿制药的药品质量和疗效持怀疑态度
以上是两家药企的争论,不做过多分析。但站在医生和患者的角度,我们还是得谈论一下原研药和仿制药的问题。
首先,梅斯先请你们投一个票:
我们曾做过一项面对全体医生和患者的调研,询问他们对仿制药和原研药的态度。
结果是,超过6成的患者对仿制药的药品质量和疗效持怀疑态度,这6成的人群中超过20%只对进口原研药青睐有加,是原研药的铁杆支持者。
而在医生方面,65%的医生表示给患者开国产仿制药还是进口原研药,都要视具体情况而定,倾向于国产仿制药的医生仅为23%。
但当问题中的国产仿制药前面加上一个定语“通过‘一致性评价’”时,处方视具体情况而定的医生比例下降至42%,而支持国产仿制药可替代同类进口原研药的比例攀升至41%,同比增加近1倍,而坚持开进口原研药的比例并没有改变,仍为17%。
怎么加了一个“一致性评价”,愿意开国产仿制药的医生比例竟然提高了那么多?那什么又是“一致性评价”呢?
药物一致性评价,是《国家药品安全“十二五”规划》中的一项药品质量要求,即国家要求仿制药品要与原研药品质量和疗效一致。具体来讲,就是仿制药必须和原研药“管理一致性、中间过程一致性、质量标准一致性等全过程一致”的高标准要求。
当前,很多县市级的医生,甚至是主任医师,还停留在国产药的纯度比进口药纯度低的认知程度上,对仿制药一致性评价没有什么概念。
医生对病情严重和经济条件好些的患者,开进口药处方,对病情较轻或经济条件不好的患者开国产药处方的情况十分严重,这是一一种需要特别注意的现象。

图源摄图网
有医生表示,对于既往使用原研药的患者,在得知必须或被建议改换成中标国产仿制药之后,的确有部分患者表示出质疑,比如不信任非原研药的疗效,怀疑医生有故意推广嫌疑,但当医生表示该改变是出于“国家政策”原因之后,大部分患者也能表示接受。
查查资料可知,我国有95%的药品在2007年前获批,其中90%以上为仿制药。然而当时,国家并没有对这些药物提出与原研药一致性评价的强制性要求,所以有些药品在疗效上与原研药存在一些差距。这也是超6成患者对仿制药提出质疑最重要的原因。
现如今,有了强制性要求,凡是通过了一致性评价的药物,其疗效至少是原研药的8折,但其价格却不到原研药的一半,甚至更低,这也是为什么所有国家都热衷于靠仿制药控制医疗费用增长的重要原因了。
事实上,很多国家在扶持原研药和仿制药的问题上都面临两难抉择,仿制药价格实惠、效果也不差,有利于减轻医保负担。但一味支持仿制药又会打击原研药的核心创新能力,导致后续创新不足,以后都没有人愿意花大量金钱和时间去搞原创研发了,那还提什么仿制呢?
下一步,仿制药只有比原研药做得更好,在巨人的肩膀上更有创新精神,或许才能得到更多患者和医生的认可!
一些药很救命又便宜,
但是药企却不生产了……
从玛巴洛沙韦片这种人人都想仿制的“网红流感神药”,笔者想到了那些不受药厂待见、待在角落里再无出头之日,却给患者带来了实实在在疗效的一些药物。
大家还记得二巯丙磺钠注射液吗?这种药俗称“排铜针”,是治疗“肝豆病”的特效药,但目前已经停产了。
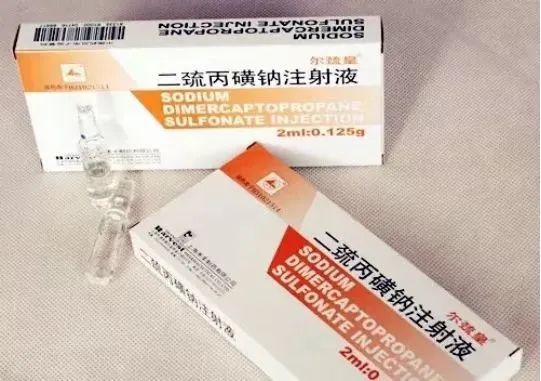
图源药健网
肝豆病属于罕见病,全世界已知的罕见病约有7000种,其中只有约6%的疾病有药可治,即便有特效药,也大多非常昂贵,一年费用几十万到几百万都有。而二巯丙磺钠,一支50元左右,假设一年治疗需要400支,那就是2万元的费用,和其它罕见病药物相比,堪称最便宜的罕见病特效药。
奈何,便宜也是一种罪过……
正因为二巯丙磺钠注射液价格便宜、需求量小,造成的结果就是药企没有动力生产,前段时间又因为全国唯一的原料厂搬迁,造成药品暂时停产,上万患者陷入困境。
大家是否又记得氨苯砜片呢?同样作为老药,作为国家基本药物目录中的药物,氨苯砜最初被广泛应用于麻风病的治疗,80年代又被用于线性IgA大疱性皮病的治疗,效果一直很好。

源自健康时报
可由于线性IgA大疱性皮病在中国发病较少,甚至没有流行病学的统计,导致这种药在中国停产,患者一度达到无药可用的地步。
据相关药厂质量部经理告诉记者,“这个药上市之后就是卖两三分钱一片,十年过去了,成本和员工的工资都涨了好几倍,药的定价还是几分钱一片。我还记得2016年时,这款药一瓶大概65元,摊下来6分钱/片,成本都赶不上”。
“卖矿泉水都比卖这个药赚钱,药企没法再做这个亏本生意。”药厂质量部经理透露,其所在的药厂曾是氨苯砜片的生产厂家之一,但氨苯砜片早已于2017年起就被划出生产目录。
当问及未来是否可能会恢复氨苯砜片的生产时,该质量部经理坦言:“应该很难了。”
过去几年,“药荒”轮番上演:2011年,心脏手术用药“鱼精蛋白”出现全国性紧缺;2012年,治疗心脏衰竭的抢救用药“西地兰注射液”短缺;2013年,治疗甲亢的“他巴唑”断货;2015年,心外科用药“地高辛片”、“放线菌素D”全国断供……
有网友不禁询问,这些药物利润不好,但可都是救命的药,药厂不生产了,相关政府部门能不能制定一些政策,给国企药厂一些财政兜底,督促他们肩负起民生职责,采取集中生产、集中管控的方法,重新把那些药物生产起来。

或者建立一种罕见病药物国家储备的制度,最起码能保证这些患者有药可购,不至于求药无门。

网友的建议一条条一列列给得很是中肯,不知你有什么见解呢?赶快评论区告诉我们吧!
撰文 | 阿拉斯加宝编辑 | 阿拉斯加宝


