Lancet oncol:3期| 达雷妥尤单抗+来那度胺一线治疗不适移植的多发性骨髓瘤的疗效可期!
时间:2021-10-14 15:01:23 热度:37.1℃ 作者:网络
在3期MAIA试验(中位随访28.0个月)的主要分析中,与采用来那度胺和地塞米松治疗的不符合移植条件的新确诊的多发性骨髓瘤患者相比,采用达雷妥尤单抗联合来那度胺和地塞米松治疗的患者的无进展生存期显著延长。
本文汇报了该试验预定的总生存期中期分析的最新疗效和安全性结果。
MAIA研究是一项正在进行的、多中心、随机的、开放标签的3期试验,从14个国家的176家医院招募年满18岁的、新确诊的、因年龄(>65岁)或合并症不能进行大剂量化疗+自体干细胞移植的多发性骨髓瘤患者。受试患者被1:1随机分成了两组,接受达雷妥尤单抗(16 mg/kg;前两个疗程,1/周;第3-6个疗程,1/2周;第7个疗程起,1/4周)+口服来那度胺(25 mg,第1-21天)+口服地塞米松(达雷妥尤单抗组)或来那度胺+地塞米松(对照组)治疗,28天为一疗程。重要终点是无进展生存期。次要终点是总生存期。
两组的无进展生存期
2015年3月18日至2017年1月15日,共952位患者接受了条件评估,其中737位被招募入组后随机分至达雷妥尤单抗组(n=368)或对照组(n=369)。中位随访了56.2个月后,达雷妥尤单抗组和对照组的中位无进展生存期分别是未达到 vs 34.4个月(风险比[HR] 0.53, 95% CI 0.43-0.66; p<0.0001)。两组的中位总生存期均未达到(HR 0.68, 95% CI 0.53-0.86; p=0.0013)。
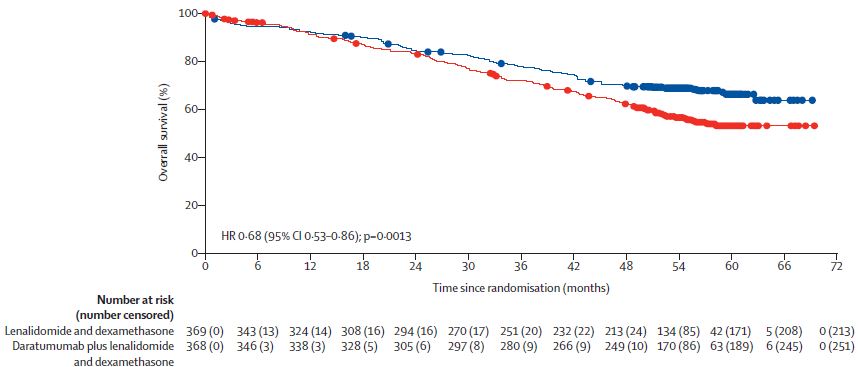
两组的总生存期
最常见的(>15%)3级及以上的治疗相关的不良事件有中性粒细胞减少(达雷妥尤单抗 vs 对照组:54% vs 37%)、肺炎(19% vs 11%)、贫血(17% vs 22%)和淋巴细胞减少(16% vs 11%)。达雷妥尤单抗组有281位(77%)患者、对照组有257位(70%)患者发生了严重不良事件;还分别发生了13例(4%)和10例(3%)治疗相关死亡。
总而言之,达雷妥尤单抗联合来那度胺和地塞米松相比单用来那度胺和地塞米松可延长不适合进行干细胞移植的新确诊的多发性骨髓瘤患者的总生存期和无进展生存期。无新的安全性事件发生。该研究结果支持在一线使用达雷妥尤单抗+来那度胺和地塞米松治疗不适合移植的多发性骨髓瘤患者。
原始出处:
Thierry Facon, et al. Daratumumab, lenalidomide, and dexamethasone versus lenalidomide and dexamethasone alone in newly diagnosed multiple myeloma (MAIA): overall survival results from a randomised, open-label, phase 3 trial. The Lancet Oncology. October 13, 2021. https://www.thelancet.com/journals/lanonc/article/PIIS1470-2045(21)00466-6/fulltext