晚期尿路上皮癌新疗法在 2 期临床试验中显示出前景
时间:2021-08-03 13:02:01 热度:37.1℃ 作者:网络
 enzolifesciences
enzolifesciences
在铂类化疗和免疫检查点抑制剂 (CPI) 联合治疗后疾病进展的转移性尿路上皮癌 (mUC) 患者的治疗选择有限。进展后,根据 NCCN 和 ESMO 指南,唯一可广泛使用的药物是紫杉烷和长春氟宁(欧盟批准)。这些药物的反应率约为 10%,中位总生存期 (OS) 为 7-8 个月。
近期,在一项国际多中心 2 期临床试验公布的结果中,一种治疗晚期尿路上皮癌的新疗法有效且副作用可耐受。试验结果促使美国食品和药物管理局 (FDA) 于4月13日加速批准该疗法,为患有这种侵袭性很强的癌症患者提供了一种新的治疗选择。
在这项于 4 月 30 日在线发表在《临床肿瘤学杂志》( Journal of Clinical Oncology)上的研究中,研究人员对 113 名晚期尿路上皮癌(最常见的膀胱癌类型)患者进行了治疗,研究治疗药物为sacituzumab govitecan (SG),以前称为 IMMU-132,现在商品名为 Trodelvy。
 TROPHY-U-01: A Phase II Open-Label Study of Sacituzumab Govitecan in Patients With Metastatic Urothelial Carcinoma Progressing After Platinum-Based Chemotherapy and Checkpoint Inhibitors. Journal of Clinical Oncology, 2021; 39 (22): 2474 DOI: 10.1200/JCO.20.03489
TROPHY-U-01: A Phase II Open-Label Study of Sacituzumab Govitecan in Patients With Metastatic Urothelial Carcinoma Progressing After Platinum-Based Chemotherapy and Checkpoint Inhibitors. Journal of Clinical Oncology, 2021; 39 (22): 2474 DOI: 10.1200/JCO.20.03489
总体而言,他们之前接受了3种治疗,尽管接受了以铂金为基础的化疗和免疫促进 "检查点抑制剂 "的治疗,试验人群的病情仍有进展。在接受 SG 治疗后,31 名患者 (27%) 的肿瘤大小持续缩小,包括 6 名患者的肿瘤完全消失。最常见的严重副作用包括 34% 的白细胞计数极低(10% 发烧)和 9% 的严重腹泻,这些副作用通过剂量调整和最佳支持治疗均可得到控制。
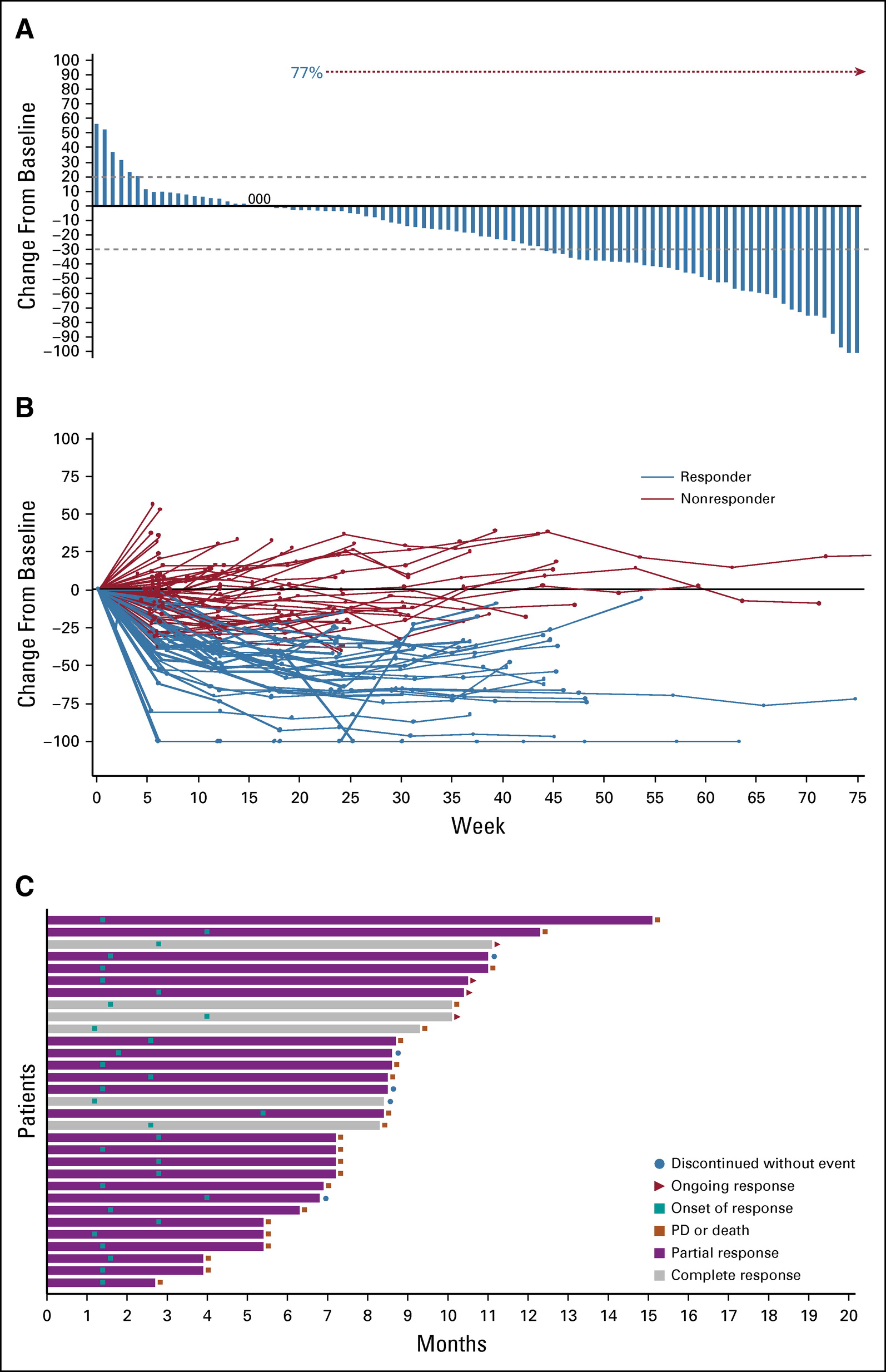 对 sacituzumab govitecan 的肿瘤反应
对 sacituzumab govitecan 的肿瘤反应
尿路上皮癌约占膀胱癌的 90%,在美国有每年约 70,000 例新病例和 17,000 例死亡的速度发生。这些病例中有四分之三以上是男性,吸烟会使患这种癌症的风险增加几倍。
晚期尿路上皮癌通常肿瘤无法手术或已经转移,通常用铂类化疗药物治疗(如顺铂或卡铂),和/或旨在释放免疫系统抗癌能力的免疫检查点抑制剂药物。但在大多数情况下,这些治疗仅在疾病再次进展之前的有限时间内有效。
SG 代表了患有这种侵袭性类型和阶段的癌症患者的新选择——与用于该适应症的其他药物相比,它具有不同的靶点与良好的作用机制。
Sacituzumab govitecan 是一种抗体药物偶联物。药物成分是一种名为 SN-38 的化疗药物,它附着在一种抗体上,该抗体位于一种名为 Trop-2 的受体上——在大多数尿路上皮癌细胞中发现。通过这种方式,该药物可以专门杀死肿瘤细胞,同时在很大程度上保护正常的健康细胞。
制造SG 的公司主要针对其他癌症对其进行测试,在 2015 年的一项试点试验中,招募了 45 名难治性尿路上皮癌患者(包括许多其他各种晚期癌症),结果显示在6名对铂类化疗无反应的晚期尿路上皮癌患者中,有3名肿瘤缩小了,该试验结果令人鼓舞。
此次,在由吉利德科学公司赞助的名为 TROPHY-U-01 的新 2 期试验中,他们在 113 名晚期尿路上皮癌患者中测试了 SG,这些患者在接受铂类和检查点抑制剂治疗后癌症仍进展。这些患者在全球 42 个中心接受治疗,每三周接受两次 SG 输注。如果肿瘤生长(进展)或副作用不可接受,则停止试验。
对肿瘤扫描进行的一项独立、盲法分析显示,有76% 的患者肿瘤缩小,27% 的患者出现“客观反应”,即显着、持续的肿瘤缩小——包括 6 名患者的肿瘤消失。中位反应持续时间为 7.2 个月,从治疗开始的中位总生存期为 10.9 个月。
相比之下,该类别中用于治疗耐药的晚期尿路上皮癌的标准细胞毒性化疗的客观缓解率约为 10%,中位总生存期约为 7 个月。
根据 TROPHY-U-01 研究,另一种名为 enfortumab vedotin (EV) 的抗体药物偶联物获得了 FDA 的加速批准,最近公布的 3 期试验数据可能会获得完全批准。TROPHY-U-01 试验中接受过 EV 治疗的患者数量很少,但与其他试验参与者相比表现出相似的反应。研究者表示,鉴于每种疗法都有不同的靶点和接头,并使用不同的毒素来破坏肿瘤,因此这一发现并不奇怪。
但专家仍强调,TROPHY-U-01 试验是一项初步试验,缺乏并行对照组——每位患者都接受了相关治疗,因此很难将其结果与其他药物的结果进行比较。不过,他指出,SG 的制造商于去年年底开始了一项随机、对照、3 期试验,将其与化疗进行比较(TROPiCS-04)。该研究的结果将在几年后到期,将决定 FDA 是否授予全面的监管批准。
原始出处:
TROPHY-U-01: A Phase II Open-Label Study of Sacituzumab Govitecan in Patients With Metastatic Urothelial Carcinoma Progressing After Platinum-Based Chemotherapy and Checkpoint Inhibitors. Journal of Clinical Oncology, 2021; 39 (22): 2474 DOI: 10.1200/JCO.20.03489


