JNNP:提高四级护理转诊中心外显子组测序的效率:罕见神经遗传疾病的新突变、临床表现和诊断挑战
时间:2021-06-20 23:02:52 热度:37.1℃ 作者:网络
遗传性神经肌肉疾病患者常表现为非特异性、复杂和非典型表型,仅凭临床资料难以做出准确诊断。疾病基因的鉴定能够对患者进行分子诊断,确定亲属的疾病风险,是更好地理解潜在蛋白质的生理作用和疾病途径的第一步,进而导致疾病治疗的发展。尽管靶向基因面板和候选基因检测可以识别已知突变,但这些检测可能成本高昂,而且对未知突变不敏感。全外显子组测序(WES)可以快速、低成本和无偏倚地鉴定疑似遗传病患者的致病性变体。但是,这种强大的基因发现工具提供的大量信息可能非常耗时,而且往往产生不确定的结果。使用基因列表可以通过将患者WES结果筛选到与致病突变相关的基因中确定的变体来提高诊断率。 然而,通过基因列表筛选确定的感兴趣的变体需要通过其他方法进一步验证。

国立卫生研究院(NIH)临床中心的神经遗传学诊所是一个四级护理中心,为从国家和国际三级医疗中心转诊的患者提供服务。转诊包括复杂和难以诊断的单胎或小的家庭病例,在这些病例中,标准护理评估没有确定诊断。在这项研究中,将基因筛选列表与详细的表型分析、生物学分析和家族分离分析相结合来诊断罕见的神经遗传疾病患者。这使得本文能够识别来自不同种族和种族背景的患者的突变,这些患者患有一系列神经遗传疾病,包括那些罕见的、复杂的和非典型的疾病。
NIH神经遗传学诊所(马里兰州贝塞斯达)对66名疑似遗传性神经疾病患者(年龄范围:13-75岁,中位数:48岁)进行外显子组分析,作为其诊断评估的一部分。这些病人由三级医疗中心转介,并由外部神经学家完成评估。其中单胎50例(76%),兄弟姐妹5对9例,多代家庭7例。17名患者(26%)的祖先来自欧洲以外,包括亚洲和南美洲。大多数患者(85%;n=56)以前进行过基因检测,包括单基因和群体基因检测。所有患者均进行了全面的体检,并进行了相关的临床检查,如MRI、电生理学检查和肌肉活检。WES是在一个研究实验室(NIH校内测序中心)对从全血中提取的DNA进行的。使用VarSifter(美国贝塞斯达国家人类基因组研究所)筛选外显子组变体。共有634个基因标识符根据其与人类疾病的关联性被分为以下几类:肌病(n=293)、神经病变(n=193)和运动神经元疾病(n=148)。首先用适合其表型的基因表筛选感兴趣的变异体,然后应用另外两个基因表来确保神经肌肉疾病基因组的诊断率。
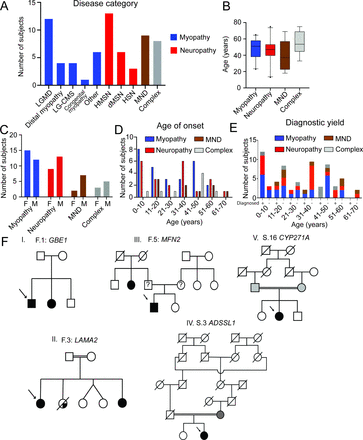
接受WES者的人口统计学和遗传模式
对从基因列表筛选中识别出的变异进行分类。具有良性影响、可能的良性影响或不确定意义的变异被排除在进一步分析之外。使用CADD、CDPred和ClinPred解释基因组聚集数据库(gnomAD)中等位基因频率<0.0001的致病性或可能致病性错义变体。全基因组寡核苷酸阵列比较基因组杂交(CGH)+SNP分析由GeneDx使用血液DNA样本上的18万个寡核苷酸探针进行。对S.2患者股外侧肌组织进行RNA序列分析。为了获得ADSSL1-cDNA克隆,从活体股外侧肌分离的细胞总RNA进行逆转录,然后用RNase H酶切合成cDNA。通过31个PCR周期,扩增出大多数ADSSL1剪接亚型共有的从外显子2到13的cdna。将5个PCR反应的产物合并,凝胶纯化并克隆到pBSK中进行Sanger测序(n=30个克隆)。从基因组DNA中扩增出ADSSL1两个主要亚型的交替5'UTR和外显子的编码序列,并进行Sanger测序分析。
39%(26/66)的受试患者进行了基因诊断,其中有受影响家庭成员的患者(88%,14/16)和有复杂表型的患者(63%,5/8)。在20岁以前发病的16个人(59%)接受了基因诊断,而在40岁以后发病的老年人中,这一比例相对较低(27%)。在有一个以上患者的家庭中,家系包括常染色体显性和隐性遗传模式。接受WES者的人口统计学和遗传模式(A) 肌病组(n=27)包括肢带型肌营养不良(n=12)、远端肌病(n=4)、肢带型先天性肌无力综合征(LG-CMS);先天性肌病(n=1)和其他(n=6)。神经病变组(n=22)包括遗传性运动和感觉神经病变(HMSN,n=13)、远端遗传性运动神经病变(dHMN,n=6)和遗传性感觉神经病变(HSN,n=3)。这些患者主要有轴突型(n=17)、脱髓鞘型(n=3)或混合型(n=2)神经损伤。运动神经元病组9例,复合组8例(B) 以平均值和5/95%可信区间显示初次出现时年龄分布的图表。肌病、神经病变、MND和复杂表型组的平均发病年龄分别为48岁、46岁、41岁和55岁(C) 每个疾病类别中女性(F)和男性(M)的数量(D) 各疾病类别的发病年龄分布。肌病组有11例青少年/成人发病(10-40岁),8例儿童发病(<10岁)和8例晚发(>40岁)疾病。在肌病(n=3)、神经病变(n=5)和MND(n=2)患者中发现了10种新的致病性变体。9个氨基酸替换在其他物种间保守的残基中。这些变异发生在被认为是疾病相关变异热点的蛋白质的重要功能域。远端肌病患者的MYH7 p.Leu1533Pro变异体(S.7)位于蛋白的远端杆区,在该区域已确定其他突变可引起Laing远端肌病和心肌病。
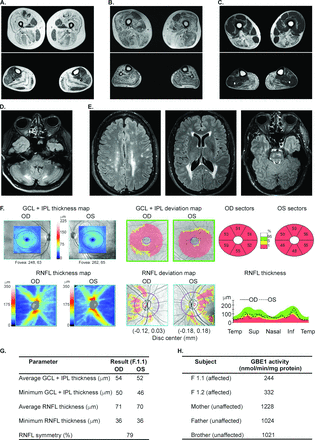
通过外显子组测序分析辅助遗传诊断的临床试验结果实例
鉴于WES在研究和诊断实验室中已经建立,需要更多的方法和途径来解释和确认这些数据,神经科医生和病人之间的接口需要更好的描述,以便更多的医生可以决定下一步哪些是合适的,在随后的评估和验证基因检测数据。本文方法使用了一系列在临床实践中可行的工具,包括预测算法、生物信息学、家族分离研究、临床诊断测试和生物分析,从而提高了WES测试的产量。我们在66个有不同罕见神经遗传疾病表现的连续、未经选择的个体中获得了39%的分子诊断率(n=26),这高于其他研究的阳性率(13%–30%)。尽管对这些患者的病情进行了广泛的评估,包括单基因和群体基因检测,但这些患者多年没有诊断。先前的研究表明,在儿童期接受WES治疗的人群中,诊断成功率分别为46%和39%。本文在20岁以下患者中的诊断率为59%,突出了本文方法的新颖性和实用性。在本文的队列中,晚期发病年龄是一个诊断挑战,三分之一的患者发病年龄超过40岁。在这组患者中,本文的诊断成功率为27%。
这种方法使能重新定义本文的实践,识别新的疾病相关变体,扩大罕见疾病的表型谱,并为本文的患者和高危家庭成员提供更好的护理。
Grunseich C, Sarkar N, Lu J, et al Improving the efficacy of exome sequencing at a quaternary care referral centre: novel mutations, clinical presentations and diagnostic challenges in rare neurogenetic diseases Journal of Neurology, Neurosurgery & Psychiatry Published Online First: 08 June 2021. doi: 10.1136/jnnp-2020-325437

