南开大学郭东升/王蔚ACS Nano: 多功能纳米材料的超分子策略协同治疗类风湿性关节炎
时间:2023-12-18 15:01:36 热度:37.1℃ 作者:网络
疾病的复杂性和渐进性要求开发更加多功能的材料。然而,引入功能不可避免地会增加材料的复杂性,从而使制备复杂化并降低可重现性。
在本研究中,南开大学郭东升教授/王蔚副教授和河北大学Ke-Rang Wang等人报道了基于甘露糖修饰的偶氮杯[4]芳烃(ManAC4A)和人参皂苷Rb1(Rb1)的多功能纳米材料及其超分子集成策略。ManAC4A具有清除活性氧(ROS)的能力和缺氧反应性,以及巨噬细胞靶向和诱导功能。因此,Rb1@ManAC4A具有三重靶向(ELVIS靶向、巨噬细胞靶向和缺氧靶向释放)和三重治疗(ROS清除、巨噬细胞极化和Rb1抗炎作用)的能力。作者指出,ManAC4A具有精确的结构和分子量,其自发组装和识别有助于简单直接地制备Rb1@ManAC4A,从而获得优异的批次一致性,有助于促进多功能材料的临床转化。相关工作以“Supramolecular Integration of Multifunctional Nanomaterial by Mannose-Decorated Azocalixarene with Ginsenoside Rb1 for Synergistic Therapy of Rheumatoid Arthritis”为题发表在ACS Nano。

【文章要点】
类风湿性关节炎(RA)是一种病因复杂的系统性自身免疫性疾病。在RA微环境中,迁移的循环单核细胞分化为炎症性M1亚型巨噬细胞,并且伴随着活性氧(ROS)通过多种促炎信号通路的上调。一方面,人参是一种受欢迎的草药化合物,具有多种治疗和药理应用。人参糖苷是人参的关键成分,已鉴定出约40种化合物。在这其中,Rb1表现出了特别突出的抗记忆、抗氧化、抗炎和抗癌活性。另一方面,杯芳烃由于其固有的活性氧清除能力而被作者选为核心骨架。通过接枝偶氮基团,具有加深空腔的偶氮杯芳烃能够提供有效的药物负载并实现缺氧控制释放。此外,甘露聚糖作为巨噬细胞靶向和诱导巨噬细胞表型的官能团,被修饰在偶氮杯芳烃的上边缘。因此,精心设计的ManAC4A构成了多功能生物材料的化学基础(图1)。通过自组装,两亲性ManAC4A形成了具有ELVIS效应(通过渗漏血管和炎症细胞介导的隔离而实现外渗)的被动靶向性和由于自组装多价性而具有巨噬细胞的主动靶向性以及表型诱导能力的纳米材料。
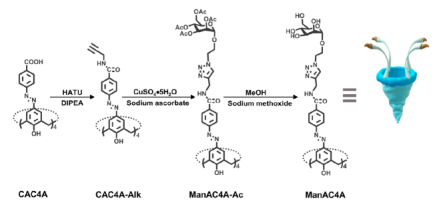
图1 ManAC4A的制备
进一步地,通过大环宿主的功能化设计以及宿主和客体药物之间的有效识别,ManAC4A纳米组装体可负载Rb1,即将大环治疗剂和大环递送系统整合到一起。所形成的Rb1@ManAC4A虽然只有两种成分,但整合了三重靶向功能,包括ELVIS靶向、巨噬细胞靶向和缺氧靶向释放,以及三重治疗功能,包括ROS清除、巨噬细胞极化和Rb1的抗炎作用,最终可应用于RA大鼠的协同抗炎治疗(图2)。
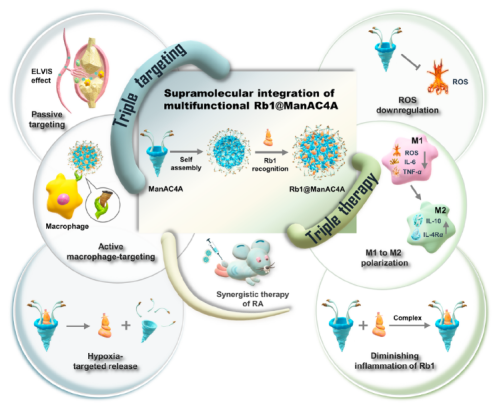
图2治疗RA示意图
原文链接:
https://pubs.acs.org/doi/10.1021/acsnano.3c09140


