Nature子刊:浙江大学朱依敏团队发现女性不育的发病新机制
时间:2023-10-22 23:34:43 热度:37.1℃ 作者:网络
N6-甲基腺苷(m6A)维持母体RNA在卵母细胞中的稳定性。ALKBH5是m6A的一个调节因子,可逆转m6A沉积,并且在RNA代谢中是必需的。然而,ALKBH5在卵母细胞成熟中的具体作用仍不清楚。
2023年10月17日,浙江大学朱依敏团队在Nature Communications 发表题为“ALKBH5 controls the meiosis-coupled mRNA clearance in oocytes by removing the N 6-methyladenosine methylation”的研究论文,该研究发现Alkbh5缺失会导致卵母细胞减数分裂的广泛缺陷,从而导致女性不育。母体转录组的时间序列分析显示在减数分裂成熟过程中,Alkbh5-/-卵母细胞中有显著的RNA积累。
m6A动力学分析表明,Alkbh5介导的m6A去甲基化确保了母源RNA的及时降解,而这一降解在Alkbh5-/-缺失后被严重破坏。具有持续m6A峰的独特转录子子集被m6A读取器IGF2BP2识别,因此保持稳定,导致RNA清除受损。此外,在Alkbh5缺失的卵母细胞中降低IGF2BP2可以部分修复这些缺陷。总之,该研究确定了ALKBH5是卵母细胞质量的关键决定因素,并揭示了ALKBH5介导的m6A去除在母体RNA衰变中的促进作用。

从卵母细胞到胚胎的复杂协调过渡伴随着母体转录本的动态变化。在生长中的卵母细胞中,母体RNA被稳健地转录和储存,以支持卵母细胞的进一步成熟和胚胎发育。一旦卵母细胞发育到完全生长的生发囊泡(GV)阶段,促性腺激素就会触发广泛但靶向选择性的母体RNA衰减,并且停止从头转录。受精后直到合子基因组激活(ZGA)才恢复转录。因此,在2-细胞阶段,小鼠胚胎中约90%的细胞RNA被降解。因此,母源性转录本的维持和及时衰变是卵母细胞获得完整发育能力的先决条件。事实上,RNA衰减延迟的卵母细胞表现出极体挤出(PBE)率降低、纺锤体扭曲和胚胎发育停滞。这些观察结果提出了关于mRNA衰减在减数分裂成熟过程中如何调节的有趣问题。
转录后修饰已被证明在调节母体转录本中发挥重要作用,从而决定RNA的命运。在这些修改中值得注意的是N6-甲基腺苷(m6A),这是真核RNA上最丰富的修饰之一,存在于多种物种中。它在RNA上的沉积由METTL3-METTL14-WTAP甲基转移酶复合物和其他调节因子催化,而它可以通过两种去甲基化酶FTO和ALKBH5(称为“橡皮擦”)去除。越来越多的m6A结合蛋白(也称为“读取器”),可识别m6A修饰的RNA,从而实现其在调节细胞生理学方面的功能。这一表观遗传标记几乎影响了RNA代谢的每个方面,并对从器官发育到癌症的广泛生物学过程产生深远影响。
之前的研究已经强调了m6A的读者和作者在卵子发生中不可或缺的功能。转录组和m6A甲基化组的综合分析表明,m6A是一个保护因素,以确保母源RNA在卵母细胞中的稳定性。这些发现共同表明m6A沉积在母体RNA上并决定其命运,从而影响卵母细胞的活性。然而,尽管大多数研究都集中在书写蛋白和阅读蛋白分别诱导和介导的RNA m6A甲基化的功能和后果,但对于由擦写蛋白催化的m6A去除在卵母细胞成熟中的作用却知之甚少。
作为已知的m6A去甲基化酶之一,α -酮戊二酸依赖性双加氧酶alkB同源物5 (ALKBH5)可清除RNA中的m6A修饰,并已被证明在哺乳动物发育和人类疾病中发挥作用。Alkbh5缺陷的雄性小鼠生育力低下,精子发生受损。对精子发生细胞的转录组和m6A谱的进一步分析表明,ALKBH5适当的m6A去甲基化是控制精子发生过程中mRNA的剪接和稳定性所必需的。除了在雄性生育力中发挥作用外,ALKBH5似乎还参与卵母细胞发育的调节,因为雌性Alkbh5-/-小鼠也表现出生育力受损。然而,ALKBH5如何影响女性生育力以及是否涉及ALKBH5的去甲基化功能尚不清楚。
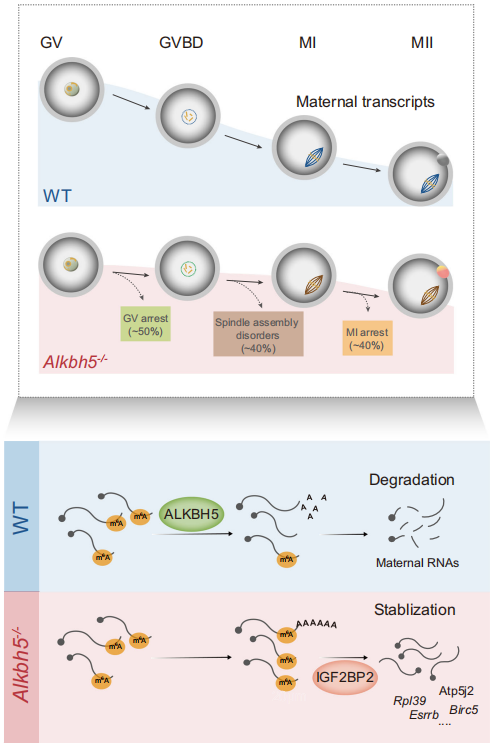
ALKBH5通过调控m6A去甲基化来调控GV-MII转化过程中的母源RNA清除(图源自Nature Communications)
为了解决这些问题,研究构建了Alkbh5全敲除(Alkbh5-/-)小鼠品系,并研究了Alkbh5在女性生育力和卵母细胞发育能力中的潜在作用。结果表明,Alkbh5-/-雌性小鼠是不育的,这些小鼠的卵母细胞成熟过程受到影响。机制上,研究发现alkbh5介导的m6A去除确保了RNA在卵母细胞减数分裂成熟过程中的及时衰减。相反,Alkbh5缺失导致的m6A修饰被m6A阅读蛋白IGF2BP2基因特异性识别。综上所述,这些发现表明,在Alkbh5-/-卵母细胞中,IGF2BP2的整体降低部分克服了母体及时降解的需要,并逆转了细胞周期缺陷。
参考消息:
https://doi.org/10.1038/s41467-023-42302-6


