Blood:Tafasitamab联合来那度胺治疗复发难治大B细胞淋巴瘤的回顾性研究
时间:2023-10-16 17:30:22 热度:37.1℃ 作者:网络
II期L-MIND研究证实Tafasitamab联合来那度胺(TL)治疗复发难治大B细胞淋巴瘤(R/R LBCL)的完全缓解率(CR)为43%,中位无进展生存期(PFS)为12.1个月。但该研究排除了≥4线治疗、原发难治、高危细胞遗传学、既往CD19靶向治疗和ECOG PS≥3分的LBCL患者,因此在真实世界环境中评估上述患者,以确认TL治疗的普遍性。
纪念斯隆·凯特琳癌症中心Gilles Salles教授牵头一项多中心回顾性研究,纳入连续的TL治疗的R/R LBCL患者178例,研究结果近日发表于《Blood》。
研究结果
共纳入178例接受Tafasitamab联合来那度胺治疗的复发难治大B细胞淋巴瘤,基线特征见表1,并与L-MIND研究进行对比。在149例可评估患者中,多数不符合L-MIND研究入组标准:如果考虑实验室指标,131例(89%)不适合;如果不考虑实验室指标,仍有116例(78%)不适合。
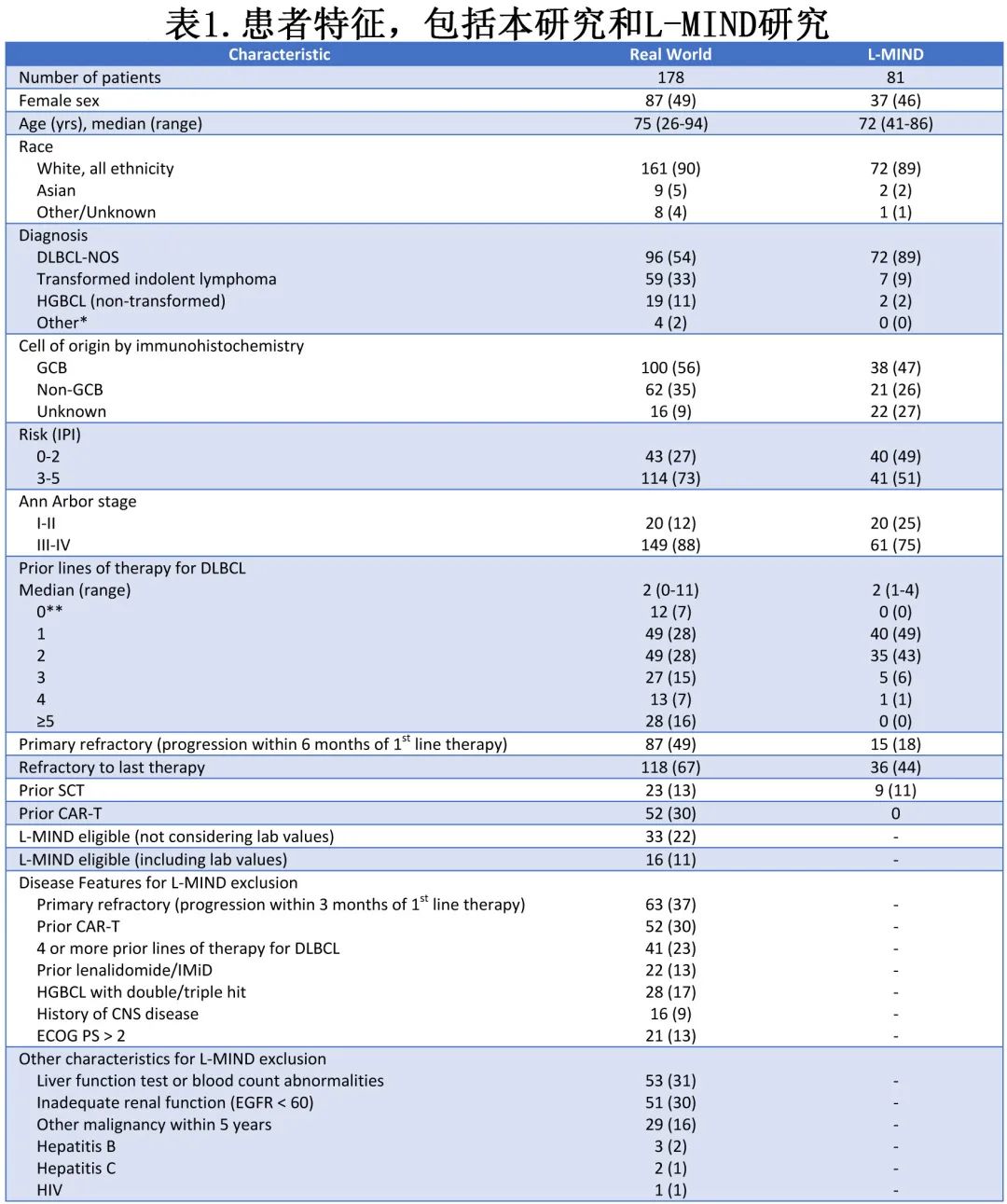
在中位至删失时间12个月时,主要终点(中位PFS)为1.9个月(图1),中位 OS 为6.5个月。最佳总缓解率为31%,CR为19%。省略实验室标准后,L-MIND研究合格患者 (n=33) 的PFS(HR=0.51) 和OS(HR=0.50) 均显著改善。
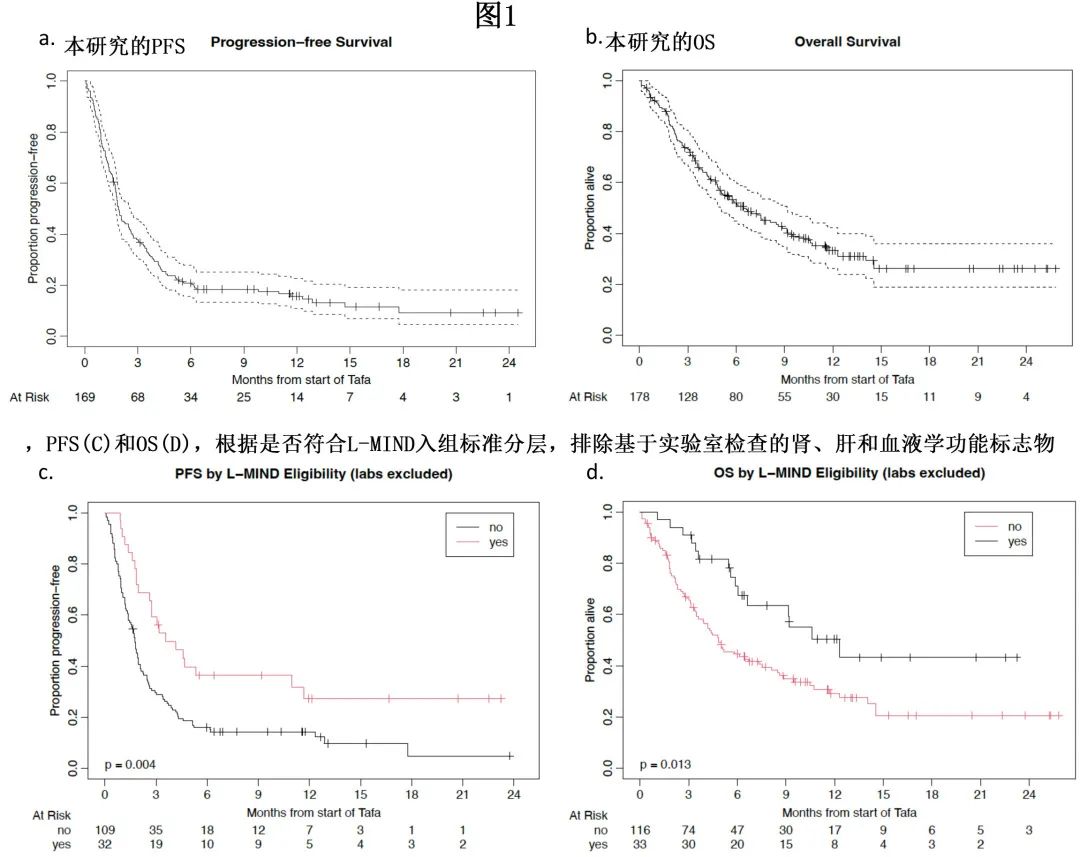
PFS的亚组分析显示,年龄<70岁、ECOG PS更差、LDH升高、国际预后指数 (IPI) 更高、既往 LBCL 治疗线数超过2线、既往 CAR-T 治疗、原发难治和末次治疗难治患者的进展风险更高。在多变量分析中,与 PFS 较差显著相关的因素包括 ECOG PS 较高 (PS 2 vs 0-1,HR=1.76,P=0.014;PS 3-4 vs 0-1,HR=2.79,P<0.001)、LDH升高 (HR=1.58,P=0.034) 和末次治疗难治(定义为<CR或6个月内复发 (HR=1.78,P=0.017)。患者年龄≥70岁与进展风险降低独立相关 (HR=0.56,p=0.019)。单变量分析显示既往 CAR-T 暴露与进展风险增加相关 (HR=1.46,p=0.043),但多变量分析显示不影响 (HR=1.04,p=0.89)。
48%的患者发生来那度胺启动延迟;在延迟的患者中,首次 tafasitamab 和首次来那度胺给药之间的中位时间为7天。来那度胺延迟与较差的 PFS 无关 (HR=1.05,p=0.78)。169例患者中的107例 (63%) 在开始时降低来那度胺剂量,与较差的 PFS 无关 (HR=1.09,p=0.63)。在减量的患者中,中位起始剂量为 15 mg/天。初始剂量降低的原因包括体能状态较差 (38%)、肾功能不全 (30%) 和血细胞减少 (6%)。
156例有安全性数据,其中54%在治疗期间发生至少1起临床显著AE。最常见的具有临床意义的 AE 为血液学事件,包括中性粒细胞减少症 (26%)、血小板减少症 (15%) 和贫血 (14%)。7%的患者发生发热性中性粒细胞减少。14%的患者因毒性而中止TL。
随访时,178例患者中有162例中止治疗,最常见的原因为疾病进展 (75%)、毒性 (14%) 和死亡 (3%)。共报告了108例死亡;淋巴瘤进展是最常见的死亡原因 (80%),其次是未知原因 (10%) 和不相关原因 (10%)。
该真实世界研究表明,TL治疗后的 PFS 和 OS 低于关键 L-MIND 研究的结果,但该人群中存在更多的高危疾病特征和合并症。这些数据表明,对于符合 L-MIND 研究合格标准的患者,TL是合理的;但不符合标准的患者,尤其是具有高危特征(如初始治疗或末次治疗难治)的患者,是 TL 的不良候选者,应考虑替代方案。
本研究强调,将具有限制性合格标准的非随机研究结果外推具有相关风险,研究疗效数据的普遍性可能有限。此外还应更加强调开发具有更多包容性标准(反映关注人群)的淋巴瘤 II 期研究。
参考文献
Qualls DA,et al. Tafasitamab and lenalidomide in large B cell lymphoma: real-world outcomes in a multicenter retrospective study.Blood . 2023 Sep 22;blood.2023021274. doi: 10.1182/blood.2023021274


