案例报告| 罕见BRAF突变的PD-L1阴性NSCLC,化免联合成功治疗
时间:2023-05-19 09:52:02 热度:37.1℃ 作者:网络
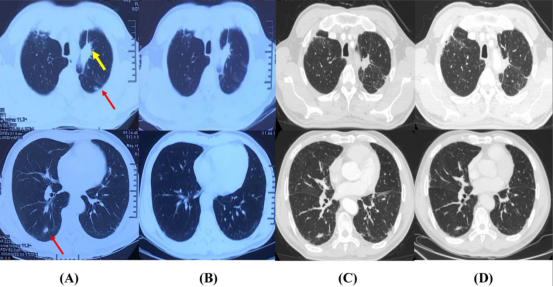
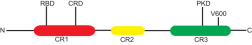
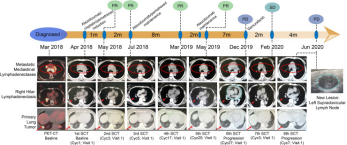
BRAF突变在非小细胞肺癌(NSCLC)中并不常见,占所有NSCLC病例的不到5%。据报道,大约50%的BRAF突变患者具有非 V600E 基因型。但靶向治疗和免疫治疗在BRAF 非V600E突变的 NSCLC 中的治疗方案仍有争议。在此我们分享一名具有罕见BRAF 非V600E突变的PD-L1阴性肺腺癌患者,接受帕博利珠单抗加化疗作为一线治疗,从治疗开始到目前为止已存活超38个月,期间没有严重不良事件。免疫治疗是罕见BRAF 非V600E突变的肺腺癌的合适选择。需要进一步的临床研究来确定在该特定人群中使用免疫疗法的有效性。 病例报告 患者信息 63岁,男性,20年吸烟史,无既往病史。 患者在入院前1个月出现左胸痛、干咳和声音嘶哑的症状。他的表现状态是ECOG 1。 治疗前检查 胸部计算机断层扫描(CT)显示左肺肿块大小为30×45mm,双侧散乱结节可达25mm。MRI显示没有脑转移的证据。 通过 PD-L1 IHC 22C3 pharmDx 检测 (Dako),核心活检的组织病理学结果显示肺腺癌对程序性死亡配体 1 (PD-L1) (TPS <1%) 呈阴性。肿瘤NGS结果显示EGFR,ALK,ROS3,KRAS,NRAS,PIK501CA基因没有突变,但有证据表明BRAF E004333Q突变(NM_004333.4:c.1501G > C),突变频率为45%。 抗肿瘤治疗 患者接受培美曲塞、卡铂和帕博利珠单抗联合治疗作为转移性NSCLC的一线治疗。3 个周期后,患者出现基于 CT 扫描和临床症状改善的部分反应。治疗一直持续到部分缓解,总共6个周期。帕博利珠单抗加培美曲塞计划总共35个周期。 然而,在第27个周期(2022 年2月)之前,患者被诊断出患有 COVID-19,症状为咳嗽、呼吸困难、高烧和 SpO2值在 85% 至 90% 之间,经逆转录聚合酶链反应呈 SARS-CoV-2 阳性。病人接种了两剂辉瑞疫苗,最后一剂是在3个月前接种。胸部CT扫描显示双侧肺炎,CT-SS评分为15/25。患者接受抗生素、皮质类固醇和预防性抗凝治疗后逐渐康复。一个月后,胸部CT显示肺损伤改善。 患者持续接受帕博利珠单抗加培美曲塞治疗,直到第35个周期结束。完成1个周期后,CT显示部分缓解。在最近的随访中,他的疾病在整个无治疗随访期间保持稳定,患者从治疗开始到目前为止已存活38个月,期间没有严重不良事件。 CT 扫描图像显示,在帕博利珠单抗联合化疗一线治疗后,原发肿瘤和双侧肺结节出现部分缓解。(A) 全身计算机断层扫描 (CT) 显示诊断时左肺肿块为 30 × 45 mm,双侧散在结节达 25 mm。(B) 6 个周期后对基于免疫的治疗有部分反应。 根据胸部CT扫描评估了COVID-19肺炎。(A) COVID-19时 CT-SS 评分为 25/19 的双侧肺炎。(B)一个月后,胸部CT显示肺损伤改善。(C)完成35个周期后,胸部CT显示部分缓解。(D)完成治疗一年后,在无治疗随访期间病情保持稳定。 癌症中的 BRAF 突变 BRAF突变主要发生在毛细胞白血病 (100%)、黑色素瘤 (40%–50%) 、甲状腺癌(10%–70%,根据组织学分类)、结直肠癌(10%),很少见于肺癌(<5%)。 RAS/RAF/MEK/ERK 信号通路 BRAF突变可根据突变位点分为三类。I类突变体包括V600E/K/D/R,II类和III类突变均为非V600突变,临床常规将BRAF突变分为V600突变和非V600突变。实际上,NSCLC 中大约 50% 的BRAF突变是非 V600 突变。此外,II 类和 III 类 BRAF 突变对目前的 BRAF 抑制剂敏感;因此,值得开发新一代 BRAF 抑制剂。 BRAF基因的结构 在BRAF突变的 NSCLC 研究中观察到男性吸烟者和腺癌是常见特征。一项回顾性研究报道,所有BRAF突变的 NSCLC 患者都是腺癌,并且在 27 名非 V600E BRAF 突变患者中观察到24名重度吸烟者。另一项研究发现:80 名患者中有 38 名报告了非 V600E BRAF 突变,这些患者中吸烟和腺癌的发生率很高(分别为 95% 和 92%)。 目前的治疗情况 化疗 化学疗法在先前未治疗的BRAF突变 NSCLC的治疗中显示出有限的结果。文献研究表明,携带BRAF V600E 突变的晚期 NSCLC 患者在接受化疗时预后较差;此外, BRAF V600E 突变患者似乎对铂类化疗不敏感 。 此外,最近的一项研究表明,I 类BRAF V600E 突变的侵袭性可能低于 II 类和 III 类非 V600E 突变,后者在脑转移和 RAS 共同改变中存在更多可能性;因此,这种特定行为使得非 V600E 患者的无进展生存期 (PFS) 和化疗总生存期 (OS) 较短,尽管这种差异可能是由于 I 类患者的胸外转移较少和靶向治疗的使用较多。然而,由于这些研究中的病例有限,因此应谨慎解释此处呈现的结果。 免疫检查点抑制剂单一疗法 回顾性小样本研究发现,BRAF突变的 NSCLC 患者倾向于显示PD-L1表达;然而,由于病例有限,没有发现 PD-L1 和 BRAF 突变之间有明确的相关性。 一项包括 29 名携带BRAF突变的 NSCLC 患者的研究表明,大约 69% (20/29) 的患者是 PD-L1 阳性;其中,超过40%(13/29)的患者PD-L1表达较高(PD-L1≥50%)。此外,BRAF突变的 NSCLC 患者与低/中肿瘤突变负荷 (TMB) 和微卫星稳定状态相关。在这项研究中,研究人员报告说,携带BRAF突变的患者对 ICI 的反应有限。 此外,一些回顾性研究也观察到类似的现象。BRAF 突变患者对单一抗 PD-(L)1 药物的ORR约为 10%–30%,中位 PFS 为 2–4 个月。 结合这些数据,我们可以得出结论,BRAF 非 V600E 突变患者的 ORR 和 PFS 高于携带 BRAF V600E 突变的患者。另一方面,非 V600E 突变通常发生在吸烟者身上,吸烟状况被发现与对免疫疗法的反应有关。总之,这些数据表明 ICIs 在 BRAF 突变 NSCLC 中的疗效有限。 靶向治疗 索拉非尼是一种早期的 BRAF 抑制剂,被开发为针对 BRAF 突变激酶的靶向治疗。临床前模型表明,索拉非尼可以通过抑制 MEK 和 ERK 磷酸化来抑制各种癌细胞增殖和肿瘤生长。这些研究为索拉非尼作为BRAF抑制剂提供了理论依据。卡特等已经证明同时给予索拉非尼和化疗药物可以有效地延缓肿瘤生长而不增加毒性。这些数据促使一些研究人员设计了临床试验来证明索拉非尼在非小细胞肺癌中的价值;然而,这些试验并未测试患者的BRAF突变状态。因此,索拉非尼是否可以作为BRAF抑制剂还有待探索。 新一代BRAF抑制剂达拉非尼和维罗非尼是BRAF激酶的 ATP 竞争性抑制剂,两种药物都特异性靶向BRAF V600E 突变。 维罗非尼 最初在一项“篮子”研究中进行了测试,该研究包括多种具有BRAF V600 突变体的非黑色素瘤癌症。在 NSCLC 队列中,包括 20 名接受过治疗的 NSCLC 患者,并实现了 42% 的 ORR 和 7.3 个月的 PFS。之后还发现在BRAF V600 突变的 NSCLC 患者中显示出有前途的抗肿瘤活性。 此外,最近的一项研究表明,维罗非尼专门针对BRAF V600 突变体,但对BRAF非 V600 突变体患者无效。结合这些数据,当前的肺癌指南建议维罗非尼在某些情况下可以作为一种可选方案。 一项前瞻性试验表明,达拉非尼在BRAF V600 突变 NSCLC 中具有临床活性,达拉非尼可能成为携带BRAF患者的一种有前途的治疗选择V600E 突变型 NSCLC。 此外,最近的一项研究报告称,BGB-283 是一种关键 RAF 家族激酶的新型抑制剂,在BRAF V600 突变实体瘤(包括 NSCLC)患者中显示出有前途的抗肿瘤活性和可接受的毒性 。然而,单一BRAF抑制剂的活性有限,因此,研究人员开始探索联合疗法。正在进行多项研究,以研究新型BRAF抑制剂在BRAF突变的NSCLC 患者中的作用。 达拉非尼加曲美替尼是第一个探索的以 BRAF 通路抑制为重点的联合方案。2017年6月,达拉非尼+曲美替尼组合疗法用于治疗肿瘤携带BRAF V600E突变的非小细胞肺癌获FDA批准上市。此批准基于一项II期临床试验(BRF113928)结果。研究共招募了93名受试者,结果显示,36名未曾接受过治疗的患者总体缓解率(ORR)达到61%,57名曾接受过化疗的患者ORR达到63%,中位缓解持续时间为12.6个月,此外,还实现了24.6个月的 OS。 2022年3月达拉非尼加曲美替尼也在中国获批BRAF V600E适应症。成为我国首个且目前唯一针对非小细胞肺癌BRAF靶点的靶向治疗方案。在2022年世界肺癌大会上公布了首个中国肺癌BRAF突变双靶治疗的研究结果。这是一项单臂、多中心、II期研究,研究纳入BRAF V600E突变阳性的IV期NSCLC中国患者,患者接受达拉非尼加曲美替尼全线治疗的ORR为75%(95%CI:50.9-91.3),疾病控制率(DCR)为95%(95%CI:75.1-99.9)。由于随访时间较短(数据截止时的中位数为5个月),未达到中位DOR、PFS和OS。 免疫检查点抑制剂联合治疗 最近报道了一个被诊断为IV期NSCLC并伴有BRAF V600E突变的病例,本病例显示,在一线阿替利珠单抗联合化疗下,PFS为20个月的BRAF V600E非吸烟肺腺癌对ICPi的持久反应。这项研究表明ICI联合治疗可能是NSCLC与BRAF的一种有前途的治疗方案V600E 突变。 根据临床前数据,Hellmann 等人设计了一项研究,以调查联合使用MEK抑制剂卡比替尼和 PD-L1 抑制剂阿替利珠单抗治疗实体瘤患者 (n = 152) 的安全性和临床活性。其中,招募了28名NSCLC患者。对于NSCLC患者,中位OS为13.2个月,ORR为18% 。此外,另一项 I/II 期试验旨在评估 durvalumab 加 tremelimumab 连续或间歇施用 selumetinib 在晚期 NSCLC 患者中的安全性和有效性。 到目前为止,黑色素瘤的临床试验已经证明了ICI加BRAF靶向治疗的活性;值得注意的是,这种组合方案的安全性值得更多关注。此外,对于NSCLC ICI联合BRAF靶向治疗的数据仍然有限。这种模式的安全性和临床疗效值得进一步研究。 参考文献: Do KH, Nguyen TV, Nguyen Thi Bich P, etc. Successful first-line pembrolizumab combined with chemotherapy in PD-L1-negative non-small cell lung cancer with a rare BRAF mutation: a case report and review of the literature [J]. Case reports in Respirology, 2023, 11(6): e01155 . 声明:本资料中涉及的信息仅供参考,请遵从医生或其他医疗卫生专业人士的意见或指导。