检测指标不适合免疫治疗的多处转移癌症患者,用PD-1后全部病灶消失,生存8年多了
时间:2023-08-22 11:39:59 热度:37.1℃ 作者:网络
今天的文章是关于一个微卫星稳定型(MSS)、PD-L1表达阴性的肝转移肠癌病人,通过使用PD-1抑制剂免疫治疗后,所有可见肿瘤病灶消失,我们一起看看究竟是怎么回事?这里先做个小剧透——基因损伤修复(DRR)途径的基因突变、较高的肿瘤浸润淋巴细胞是关键。
一、肠癌病人的治疗困境
最近一段时间,我们在与肠癌的患者或家属沟通的时候。经常会拿一些案例文章供大家参考,比如BRAF基因V600E突变的肠癌,通过药物组合实现5年期间的长生存。这些都是实打实发生的治疗案例,对大家的治疗具有非常好的参考。
一般来说肠癌患者基因检测首先看KRAS基因、BRAF基因等突变情况,此外检测微卫星不稳定性MSI的情况,有时还需要加测PD-L1蛋白表达。这些将会来指导患者能否从靶向药或免疫治疗药物里获益。但是晚期肠癌的微卫星高度不稳定性的比例仅为5%,剩下95%的晚期肠癌对PD-1的治疗应答有限。微卫星稳定型肠癌的免疫微环境以免疫豁免和免疫荒漠型为主,肿瘤淋巴细胞浸润和肿瘤突变负荷(TMB)水平较低,被认为是典型的“冷肿瘤”。目前主要是通过将免疫治疗和化疗、放疗、靶向药联合,调节这种肠癌患者的肿瘤微环境,将“冷肿瘤”变为“热肿瘤”,以提升免疫治疗的疗效。
那究竟什么样的情况下,肠癌患者使用免疫治疗会有效,下面的案例我们看看能获得什么样的启发。
二、一个幸运的晚期肠癌患者
2019年1月,一名50岁男性患者因为直肠癌肝转移而入院治疗,CT影像学检查显示右肝左叶和尾叶有主要的转移瘤,对肝转移病灶的穿刺也证实了是转移性直肠腺癌,第二代基因测序结果发现KRAS基因野生型(没有突变),微卫星稳定型(MSS),PD-L1阴性表达,肿瘤突变负荷TMB数值较高为11.7突变/Mb。
这个患者2014年3月初确诊为IV期直肠腺癌伴随左肝转移,接受8个周期的转换治疗(贝伐单抗联合化疗),随后对直肠和肝转移病灶进行了根治性手术。手术之后患者又接受了5个周期的辅助化疗和1年的维持治疗。
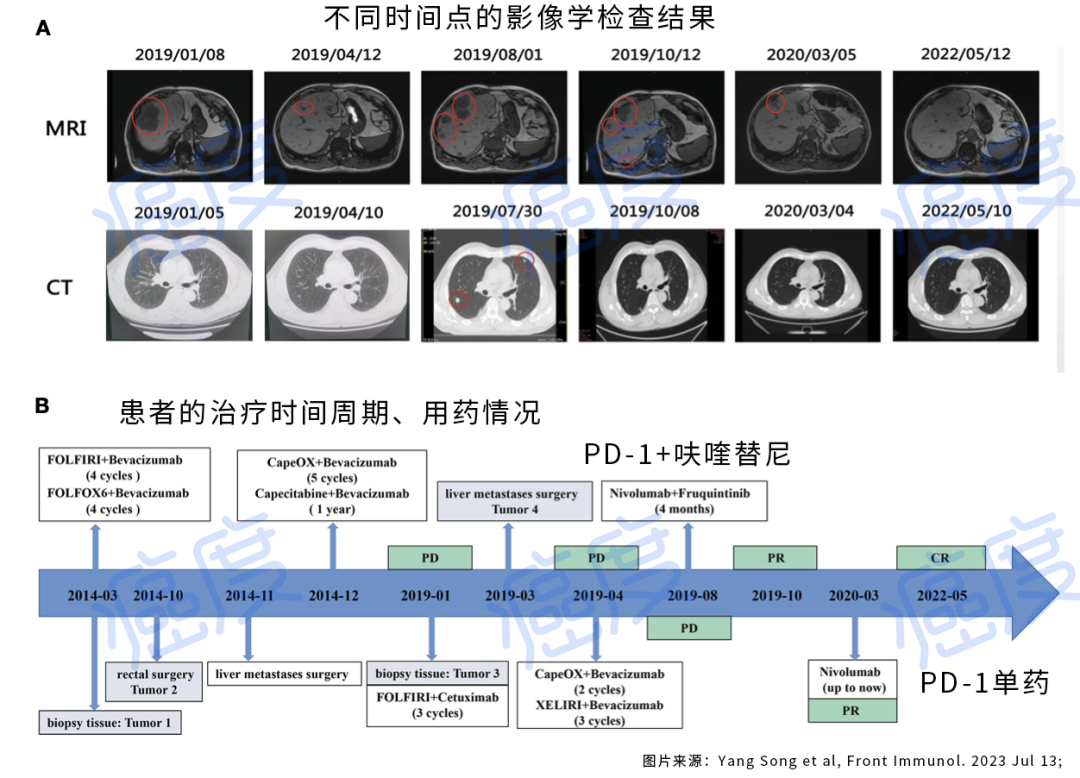
患者的治疗时间周期和用药、影像学检查结果
2019年患者再次复发后,先后使用了西妥昔单抗联合化疗、肝部手术治疗等,但是7个月后的检查显示肿瘤已经转移至肺部。在这个时候医生也没什么更好的办法了,他们跟患者和家属沟通后,给予患者使用PD-1抑制剂纳武利尤单抗,联合抗血管生成靶向药呋喹替尼。2个月之后胸部CT显示双肺肿瘤几乎消失,腹部增强核磁显示肝脏病灶也缩小。迄今为止,患者仅仅进行PD-1抑制剂纳武利尤单抗的单药治疗,在2022年5月最后一次复查的时候,肝脏和肺部肿瘤完全消失,达到了完全缓解。目前患者身体状况良好,已经无病生存41个月了。总生存期已经达到了106个月(8.8年)。
三、为何患者会有效果?
后面研究者仔细分析了患者的肿瘤组织样本,希望探索出来为何患者的治疗效果会这么好。最后分析出来是基因修复途径DDR有相应的基因突变,此外患者的肿瘤有比较多的肿瘤浸润淋巴细胞。当然我们不能由此判断其他的患者也可以达到这样的疗效。但是大家可以作为一个治疗的参考思路。
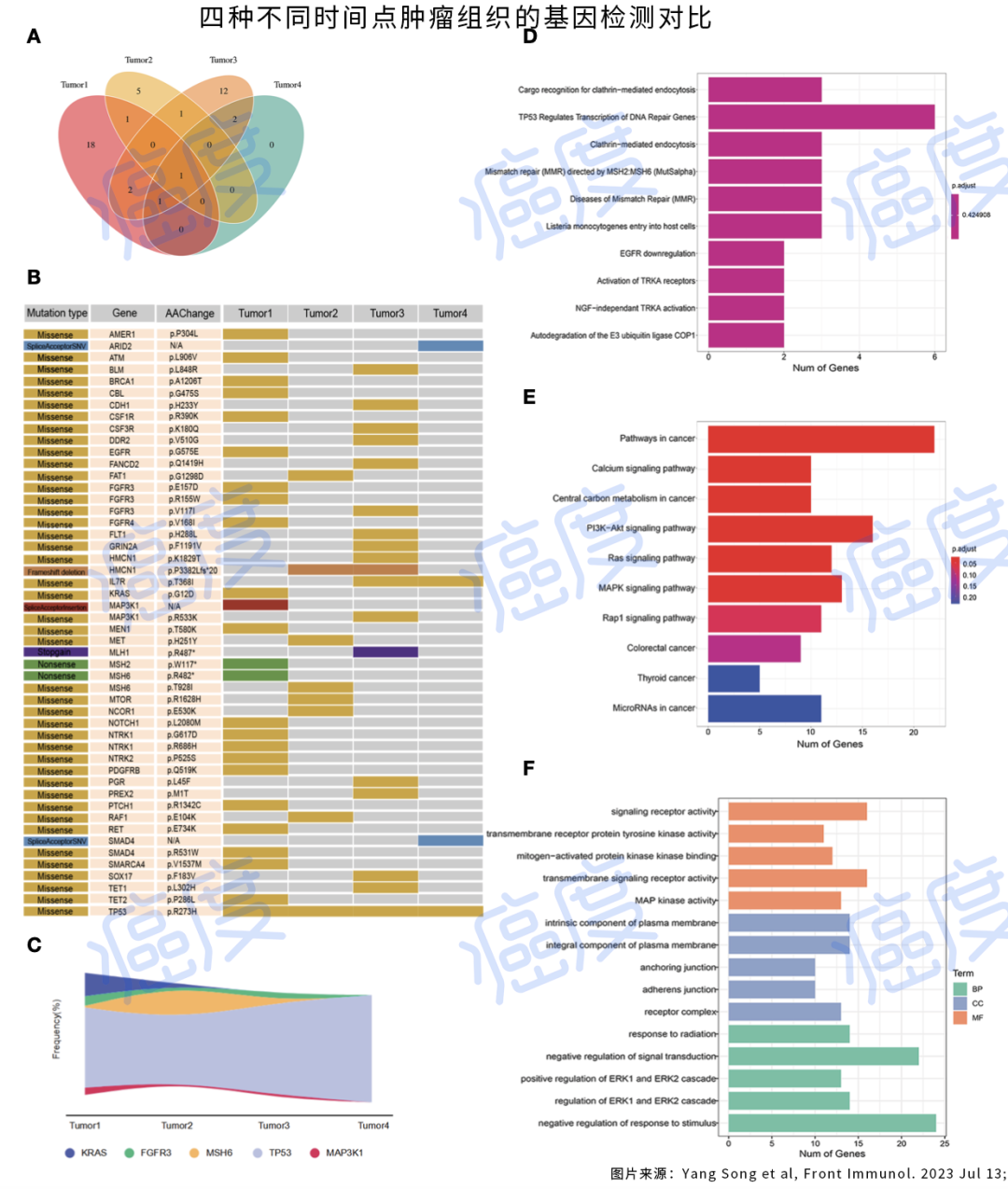
韦恩图显示四种肿瘤组织中体细胞突变的分布
我们癌度这篇稿件更多的是希望鼓励大家不要放弃。比如这个患者在最后使用PD-1和呋喹替尼的时候,医院的医生是问询并且获得他们知情同意的。但是没有人能确定就一定有很好的效果。因为按照基因检测报告的说法,这个患者不大可能从PD-1抑制剂里获益,也就是不属于免疫治疗的天选之人。但是奇迹真的发生了。
对于微卫星稳定型肠癌患者,有研究探索PD-1联合抗血管生成靶向药组合,在三线治疗的总体缓解率大概为7%到27%。此外还有在这种药物组合基础上用放疗、化疗的办法的。总之想办法去捣鼓让免疫治疗起效。
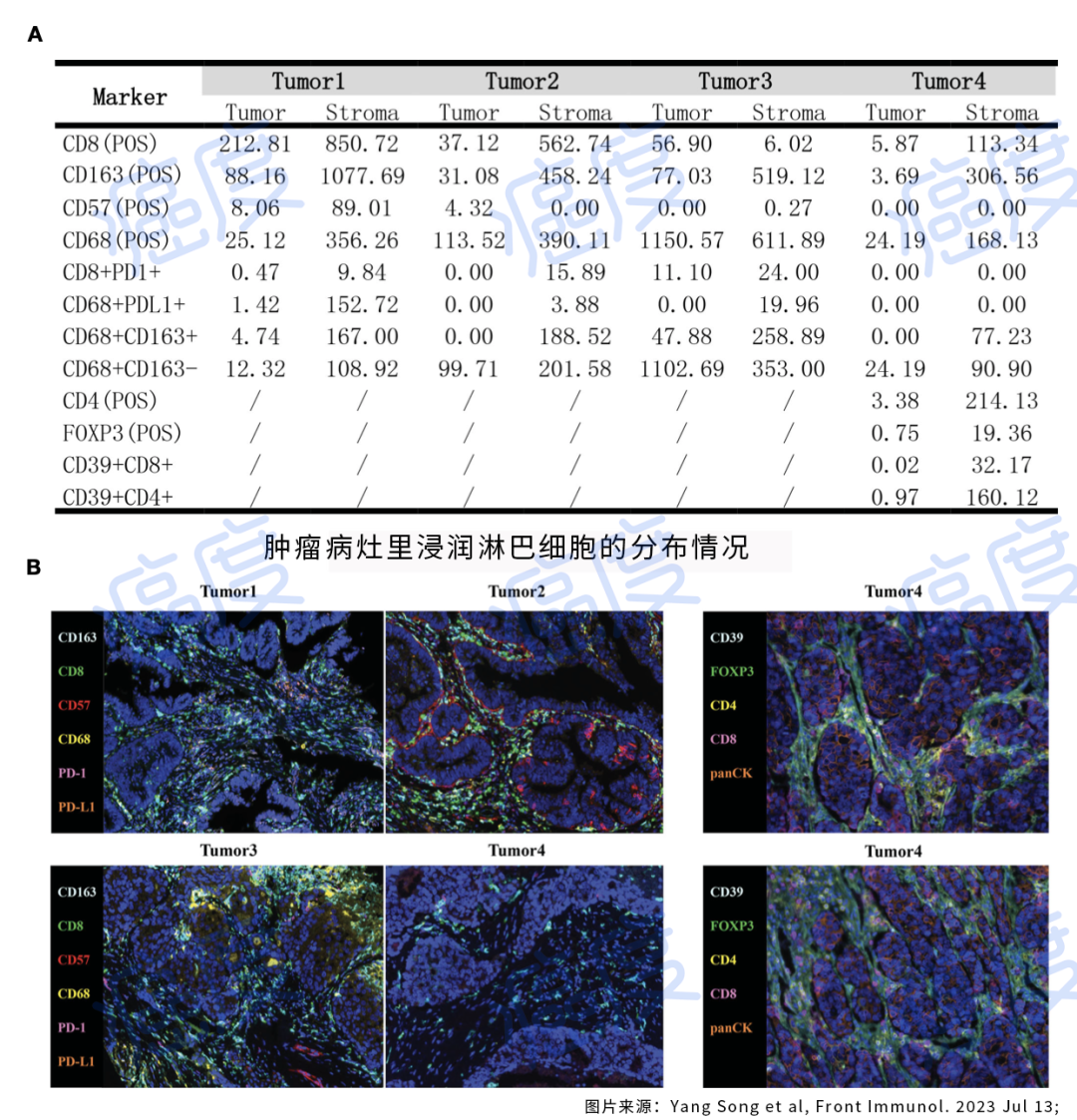
测定的肿瘤免疫微环境中肿瘤浸润免疫细胞的密度
如上面的图示,如果这个患者是最后阶段才想起用免疫治疗,比如躺在病床上已经失去行走能力。体质极度的差,这个时候免疫力已经很低了。这个时候同样使用相应的药物,也不见得会出现治疗的奇迹。
对抗癌症从来不是一件容易的事情,但既然已经发生了,便只能咬牙努力前行。也许奇迹会在下一个转角处。最后希望本文可以给到大家一些启发和参考。
参考文献:
Yang Song et al, Case Report: Genetic and immune microenvironmental characteristics of a rectal cancer patient with MSS/PD-L1-negative recurrent hepatopulmonary metastasis who achieved complete remission after treatment with PD-1 inhibitor, Front Immunol. 2023 Jul 13;


