Eur.Urol:通过 PD-L1 联合阳性评分和肿瘤细胞评分对高危肌层浸润性尿路上皮癌患者的无病生存分析( CheckMate 274 研究)
时间:2023-08-21 11:39:28 热度:37.1℃ 作者:网络
PD-L1免疫组织化学检测在评估免疫检查点抑制剂的临床试验中很常见,但PD-L1表达作为对这些治疗反应的预测性生物标志物的效用受到限制。用于评估临床试验中使用的PD-L1表达的方法的异质性,包括不同的诊断测定,组织制备方法,活检样品的部位和评分技术(肿瘤细胞与免疫细胞),以及定义PD-L1阳性的染色阈值的变化,进一步混淆了PD-L1检测缺乏既定的临床实用性。先前的研究已经使用联合阳性评分(CPS)测量了PD-L1的表达,该评分测量了肿瘤细胞和浸润性免疫细胞(包括淋巴细胞和巨噬细胞)上的PD-L1表达,仅肿瘤浸润性免疫细胞的免疫组织化学和肿瘤细胞(TC)评分。
根据CheckMate 274的原发性无病生存(DFS)结果,美国食品药品监督管理局(FDA)于2021年8月批准纳武利尤单抗用于治疗尿路上皮癌(UC)患者,无论PD-L1表达如何,这些患者在接受根治性切除UC后复发风险很高。在CheckMate 274中,与安慰剂相比,辅助纳武利尤单抗改善了根治性手术后高危肌层浸润性尿路上皮癌(MIUC)患者的DFS。在意向治疗(ITT)人群(危险比[HR]0.70,98.22%置信区间[CI]0.55-0.90;p<0.001)和肿瘤PD-L1表达≥1%的患者中观察到了这种益处。除了在ITT人群中观察到接受纳武利尤单抗治疗的益处之外,一项探索性亚组分析表明,TC<1%的患者使用纳武利尤单抗获得了DFS益处(HR 0.82,95%CI 0.63-1.06),尽管这种益处不符合常规的统计学显著性水平。

方法:通过基于PD-L1在肿瘤和免疫细胞中的表达的联合阳性评分(CPS)来分析DFS。该研究将709名患者按1:1随机分组,每2周静脉注射240 mg 纳武利尤单抗或安慰剂,辅助治疗≤1年。主要终点是使用肿瘤细胞(TC)评分的意向治疗人群和肿瘤PD-L1表达≥1%的患者的DFS。
研究结果:在629名可评估CPS和TC的患者中,557名(89%)CPS≥1,72名(11%)CPS<1,249名(40%)TC≥1%,380名(60%)TC<1%。TC<1%的患者中,81%(n=309)的CPS≥1。与安慰剂相比,对于TC≥1%的患者(危险比[HR]0.50,95%置信区间[CI]0.35–0.71)、CPS≥1的患者(HR 0.62,95%CI 0.49–0.78)以及TC<1%且CPS≥1(HR 0.73,95%CI 0.54–0.99),纳武利尤单抗可改善DFS。

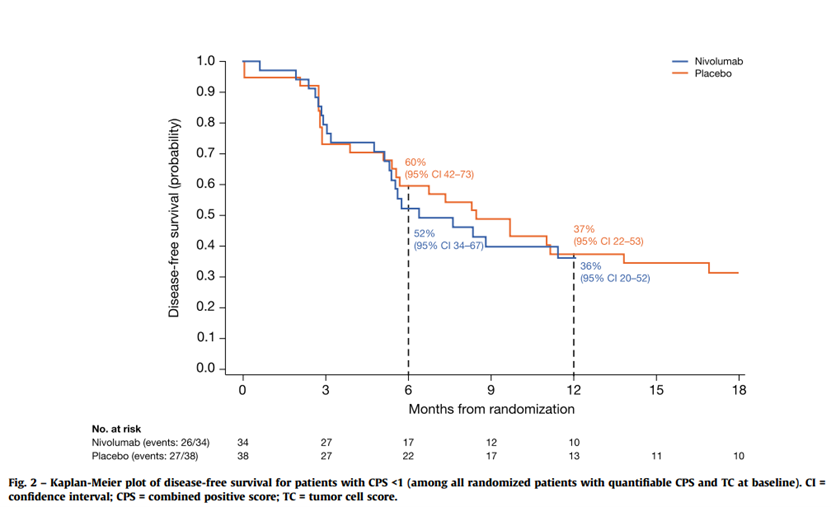

结论:总之,这项事后分析表明,CheckMate 274中的大多数患者的CPS≥1,而TC<1%的大多数患者的CPS≥1。对于TC≥1%或CPS≥1的患者,以及TC<1%和CPS≥1的患者,纳武利尤单抗与安慰剂相比,DFS有所改善。这项事后分析的结果表明,大多数TC<1%的患者在根治性切除术后也可能受益于纳武利尤单抗对高危MIUC的辅助治疗,只要他们的CPS≥1。这些结果为CPS和TC之间的差异提供了额外的见解,作为PD-L1表达的量度,需要进一步的前瞻性研究来评估这些PD-L1表达测量对临床决策的影响。
原始出处:
Galsky MD, et al. 2023. Disease-free Survival Analysis for Patients with High-risk Muscle-invasive Urothelial Carcinoma from the Randomized CheckMate 274 Trial by PD-L1 Combined Positive Score and Tumor Cell Score. European Urology 83:432-440. DOI: 10.1016/j.eururo.2023.01.016.


