Nature Cancer:顾伟团队发现,p53的这种点突变,可同时抑制铁死亡和促肿瘤转移
时间:2023-03-31 14:31:36 热度:37.1℃ 作者:网络
肿瘤转移是导致癌症患者死亡的主要原因,占癌症死亡原因的90%以上。深入研究肿瘤转移机制及药物标靶对干预肿瘤转移具有重要的意义。p53基因是重要的抑癌基因,p53基因的突变是多种肿瘤发生的关键环节之一,40-50%的肿瘤患者存在p53基因的突变。相比于单纯删除p53基因,p53基因错义突变可产生新的表型,其中重要一方面即促进肿瘤的转移,其主要原因可能为突变型p53蛋白不仅丧失了野生型p53蛋白的抑癌功能,还可通过gain-of-function(功能增益)机制干预其他信号通路,从而获得促转移功能。
针对突变型p53蛋白的干预一直是药物开发领域的热点,然而不同的突变型p53蛋白的生物学调控及其特异性靶向干预一直不清楚。
近日,美国哥伦比亚大学顾伟教授团队(苏振毅博士为第一作者)在 Nature Cancer 期刊在线发表了题为:Specific regulation of BACH1 by the hotspot mutant p53R175H reveals a distinct gain-of-function mechanism 的研究论文。
该研究发现,p53热点突变蛋白p53R175H可特异性与转录因子BACH1结合,发挥双重作用:一方面,解除BACH1对SLC7A11下调作用,从而抑制铁死亡,促进肿瘤生长;另一方面,通过上调促转移靶点的表达,促进BACH1依赖的肿瘤转移。
在机制上,p53R175H介导的BACH1功能的双向调控,依赖于它招募组蛋白去甲基酶LSD2靶向启动子和差异调节转录的能力。
这些研究数据表明,BACH1作为p53R175H执行其特定gain-of-function(功能增益)的独特的伙伴,还表明了不同的p53突变体可通过不同的机制发挥功能增益作用。这也为针对携有不同类型p53突变的癌症患者的个体化治疗提供了治疗靶标。

研究团队通过蛋白质组学筛选发现,p53热点突变蛋白p53R175H体内可以特异性与转录因子BACH1结合,从而干预BACH1的生物学功能,而其他p53热点突变蛋白(如p53R248W、p53R273H等)不与BACH1结合,也不影响其功能。
BACH1是一个具有双向调控功能的转录因子,一方面可转录抑制一批与氧化应激调节相关的基因,促进铁死亡(ferroptosis)的发生,另一方面,BACH1可转录激活另一批与肿瘤转移相关的基因,从而促进肿瘤的转移。
p53R175H与BACH1特异性结合,一方面解除BACH1对SLC7A11等铁死亡相关基因的转录抑制,从而拮抗铁死亡,促进肿瘤生长;另一方面,增强BACH1对CEMIP(细胞迁移诱导透明质酸酶-1)等促转移分子的转录激活,从而加速肿瘤的转移。
该研究进一步发现,p53热点突变蛋白p53R175H之所以可以同时调控BACH1抑制性与激活性靶点,机制上在于p53R175H可招募一个组蛋白H3K4me1/2去甲基化酶LSD2,形成p53R175H-BACH1-LSD2三元调控复合体,通过影响靶基因组蛋白的甲基化状态,实现对BACH1转录靶点的选择性调控。

p53R175H通过BACH1发挥抑制铁死亡、促进肿瘤转移的功能和机制
该研究揭示了BACH1、LSD2是介导p53热点突变蛋白p53R175H促转移作用的关键蛋白,失活BACH1或LSD2可以有效阻断p53R175H介导的肿瘤转移。
该研究首次提出并证明了不同突变型p53发挥的gain-of-function机制是可以不同的,这为针对携有不同类型p53突变的癌症患者的个体化治疗提供了可能。未来可以以BACH1或LSD2为药物靶标,设计和开发出针对p53R175H突变患者特异性的抗转移药物。
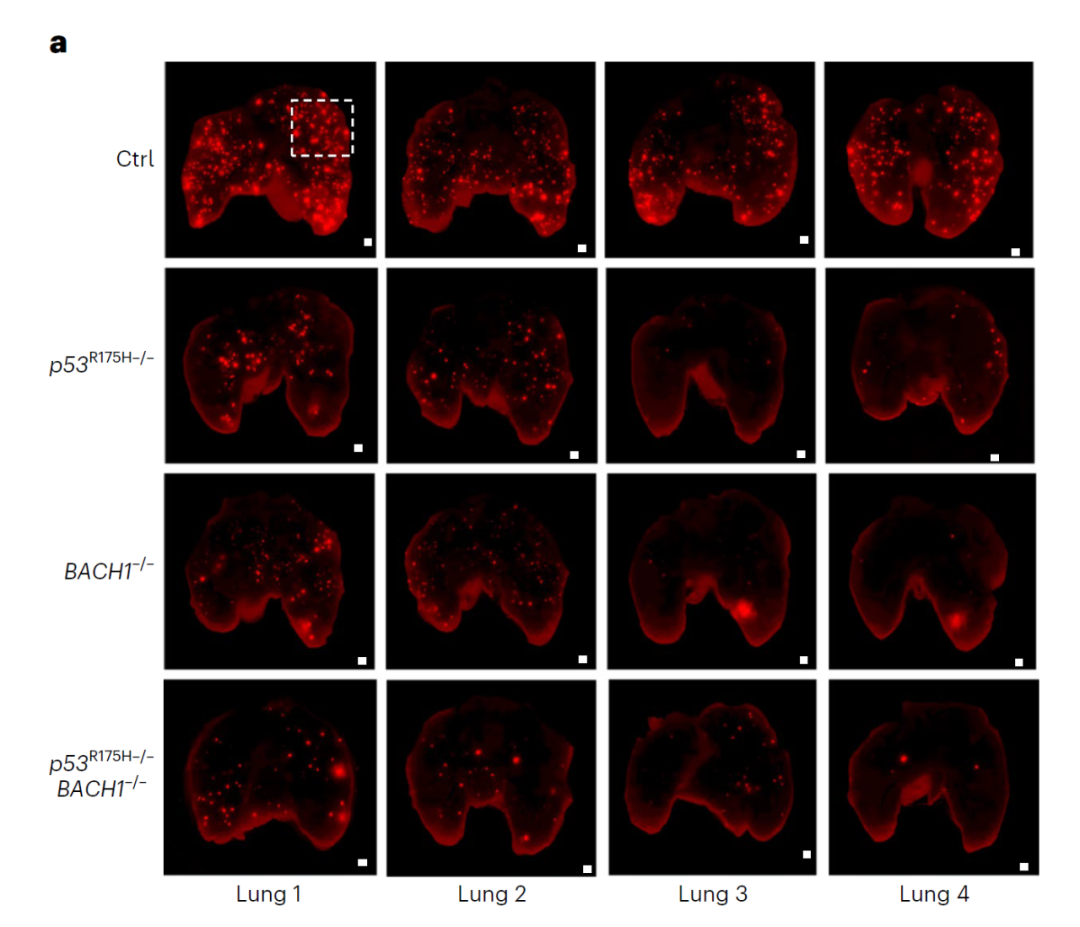
敲除p53R175H或BACH1可有效抑制肿瘤向肺部的转移
原始出处:
Su, Z., Kon, N., Yi, J. et al. Specific regulation of BACH1 by the hotspot mutant p53R175H reveals a distinct gain-of-function mechanism. Nat Cancer (2023). https://doi.org/10.1038/s43018-023-00532-z.


