硬核抗肿瘤新星——放射性核素偶联药物
时间:2023-05-04 11:46:16 热度:37.1℃ 作者:网络
放射性核素是指不稳定的原子核,能自发地放出射线( 如α,β 射线等),通过衰变形成稳定的核素。放射性核素是高效和普遍的细胞毒剂,能够通过电离辐射的方式破坏细胞,这是任何细胞手段都无法避免或消除的。所以当核素未能定向到目标细胞时,将会对周围的健康细胞造成不同程度的伤害,因此治疗剂量下的放射性核素将引起或多或少的不良反应。 而近几年不断发展至今甚至有大火趋势的放射性核素偶联药物(RDC)可以很大程度地降低核素对健康组织的损害。 RDC结构:各司其职,团体协作 RDC在结构上由靶向配体、连接臂和放射性核素组成: RDC结构示意图 1.放射性核素:作为药物的主要活性成分,放射性核素通过其α、β或Auger射线的照射作用实现治疗目的。常用的放射性核素包括碘-131、镭-223、铊-201、砷-211等。这些核素具有不同的半衰期、射程和照射方式,可以用于不同的治疗应用。 2.靶向配体:用于将放射性核素特异性运送至疾病部位的分子载体,如抗体、肽类、小分子等。这些靶向分子可以与肿瘤表面特异性配体或其他生物学靶点高度结合,实现对放射性核素的靶向递送。 3.连接臂和螯合物:放射性核素与靶向配体之间由连接臂和螯合物连接,两者可看成一个整体。常用的连接基团有螯合配合物基团、生物可降解连接基团等。这些基团应稳定、特异性地连接放射性核素与靶向分子,在靶向递送至肿瘤部位后,放射性核素可以稳定释放,发挥治疗作用。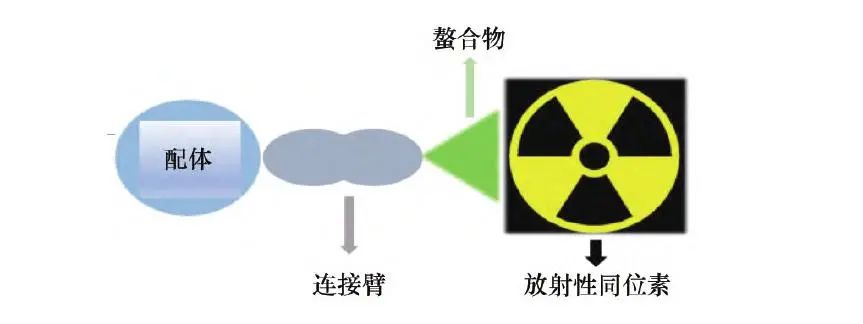
RDC疗法将放射性核素与特异性单克隆抗体相结合,实现了精准靶向和强效杀伤肿瘤细胞的双重优势。它可以将放射性核素释放的能量高度聚集在癌细胞直径的几倍范围内,从而最大限度地减少对周围正常组织的损害。这使其可以有效杀死癌细胞的同时保护正常组织,因此具有良好的疗效和低的不良反应,能够延长晚期癌症患者的生存期,这对晚期肿瘤的治疗意义重大。
RDC的强大在于种类多样且灵活组合
按照功能RDC可以分为诊断用RDC和治疗用RDC,而其功能分类与核素类型关系密切。
放射性核素分类

目前临床应用最广泛的诊断用核素是99mTc,治疗用核素则是131I、90Y和223Ra等。放射性核素技术为肿瘤的早期诊断和靶向治疗提供了独特的优势,但放射性核素的获取与制备技术仍然限制其更广阔的临床应用,需要进一步研发。
RDC根据靶向配体的不同又可细分为:抗体偶联核素药物(ARC)和小分子偶联核素药物(包括多肽偶联核素药物-PRC)。
抗体偶联核素药物
将放射性核素直接或间接偶联到肿瘤相关抗原的单克隆抗体上,利用抗体与抗原特异性结合将核素运载至肿瘤部位,这类药物疗效高但免疫原性强。
全球范围内部分获批的ARC

多肽偶联核素药物
利用肿瘤相关受体的多肽配体与放射性核素偶联,通过配体与受体的高亲和性结合将核素运载至肿瘤。主要用于神经内分泌肿瘤和前列腺癌的诊断治疗,多次给药且低免疫原性。
近五年FDA批准的PRC
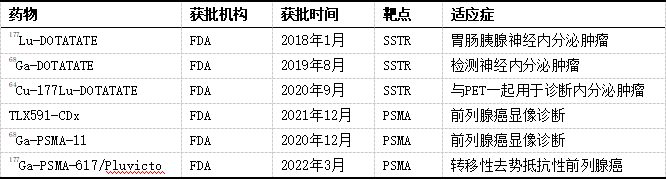
小分子偶联核素药物
小分子化合物与放射性核素偶联,依靠化合物与肿瘤碳水化合物、脂质、酶等的亲和力将核素聚集于肿瘤部位。代表药物有131I-MIBG、188Re-Lipiodol和131I-Chlorotoxin等,用于各种实体瘤和脑肿瘤的治疗,具有一定的非特异性摄取,多次给药。
上述三类药物各有优缺点,临床选择需根据肿瘤类型、病情严重程度等因素综合考虑。抗体偶联类药物虽然疗效最高但免疫原性强,多肽与小分子偶联类药物则各有其适应症。理想的核素偶联药物应同时具有高的肿瘤靶向性和选择性、低的免疫原性以及适度的体内半衰期。这需要在药物设计与研发过程中不断优化,才能最大限度地发挥核素治疗的效益。
RDC精准打击,肿瘤无所遁形
RDC治疗主要通过直接与间接的DNA损伤作用抑制肿瘤细胞增殖,同时也能在一定程度上改善抗肿瘤免疫力和改变肿瘤微环境以发挥协同的抗肿瘤效应,这使得核素治疗成为一种高效和全身的肿瘤治疗手段,具体机制如下:
RDC药物作用机制
Ø 直接DNA破坏作用:放射性核素发射的β粒子、α粒子和Auger电子可以直接作用于肿瘤细胞的DNA,引起DNA链断裂、碱基损伤和交联,从而诱导肿瘤细胞死亡。这是核素治疗的主要机制。
Ø 旁观者效应:β粒子和α粒子在穿过肿瘤细胞时会使周围的水分子电离和激发,产生自由基物质。这些自由基可进一步损害肿瘤细胞的DNA和其他生物大分子,达到杀伤肿瘤的目的。这种效应不依赖于核素与DNA的直接相互作用。
Ø 抗血管生成作用:放射性核素释放的β粒子和α粒子也可作用于肿瘤血管内皮细胞,破坏其DNA并诱导凋亡,起到抗血管生成的作用。减少肿瘤血供可使肿瘤细胞远离氧及营养物质,从而抑制肿瘤生长。
Ø 免疫增强作用:放射线可通过增强CTL细胞和NK细胞的活性,上调MHC-I和I-CAM的表达,增加TNF-α和IFN-γ的分泌等机制,强化机体的免疫监视功能,从而加强对肿瘤的免疫清除作用。
Ø 肿瘤微环境改变:放射线还能通过损伤肿瘤细胞和肿瘤微血管内皮细胞来改变肿瘤微环境,如减少营养物质的供应、增加髓外酸性、改变细胞因子的表达和分泌等。这些改变均不利于肿瘤的生长发展。
此外放射性核素靶向药物通过核射线不仅杀伤肿瘤组织表层或浅层的肿瘤组织及细胞,同时利用核射线的穿透力杀伤实体瘤内部的肿瘤细胞,即“交叉火力”效应。
RDC药物起步不久,但未来可期
自第一例核素类药物Na131I于1951年由FDA获批用于甲状腺疾病的治疗,至今不过七十年光景,全球已有超过100种放射性药物获批上市,虽然RDC药物大多还处于临床前以及临床研发阶段,总体来说处于刚起步阶段,但这并不影响我们从上市的几款药物看到的巨大抗肿瘤优势。具体体现在以下方面:
1.高度靶向:核素偶联药物可以通过与抗体、多肽或小分子的结合,实现对肿瘤细胞的高度选择性靶向,从而最大限度地减少对正常组织的损伤。相比之下,放疗和化疗的靶向性较差,易损害正常组织。
2.强效杀伤:放射性核素可以释放高能β粒子、α粒子和Auger电子,对DNA造成严重损伤,有效杀死癌细胞。放疗和化疗的杀伤效应相对较弱。
3.良好耐受性:由于高度靶向,核素治疗产生的毒性和副作用较小。而放疗和化疗造成的全身性毒性和副作用较大。
4.免疫增强:放射性核素还具有一定的免疫调节作用,可以增强机体的抗肿瘤免疫力。放疗和化疗的免疫影响相对较小。
根据全球新药情报库的数据,目前处于临床研究和上市阶段的RDC药物中,主要的研究靶点有CAIX(碳酸酐酶IX)、PSMA(前列腺特异性膜抗原)、SSTR(生长抑素受体);主要的适应症集中在神经内分泌肿瘤、前列腺癌、肾细胞癌。
RDC药物靶点
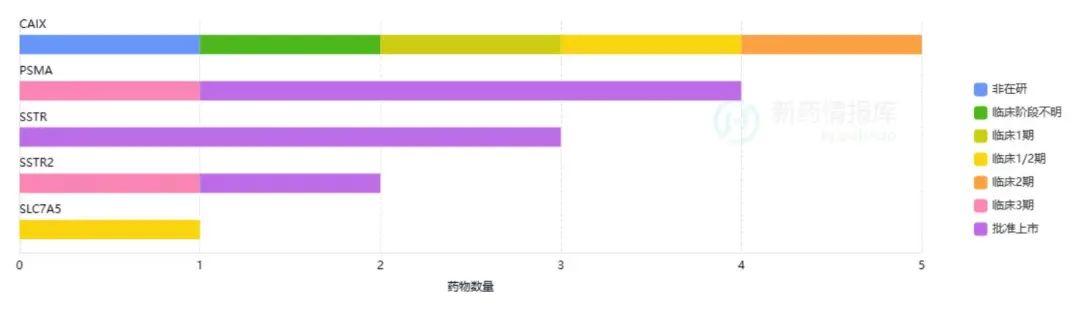
图片来源于全球新药竞争情报库
药物适应症
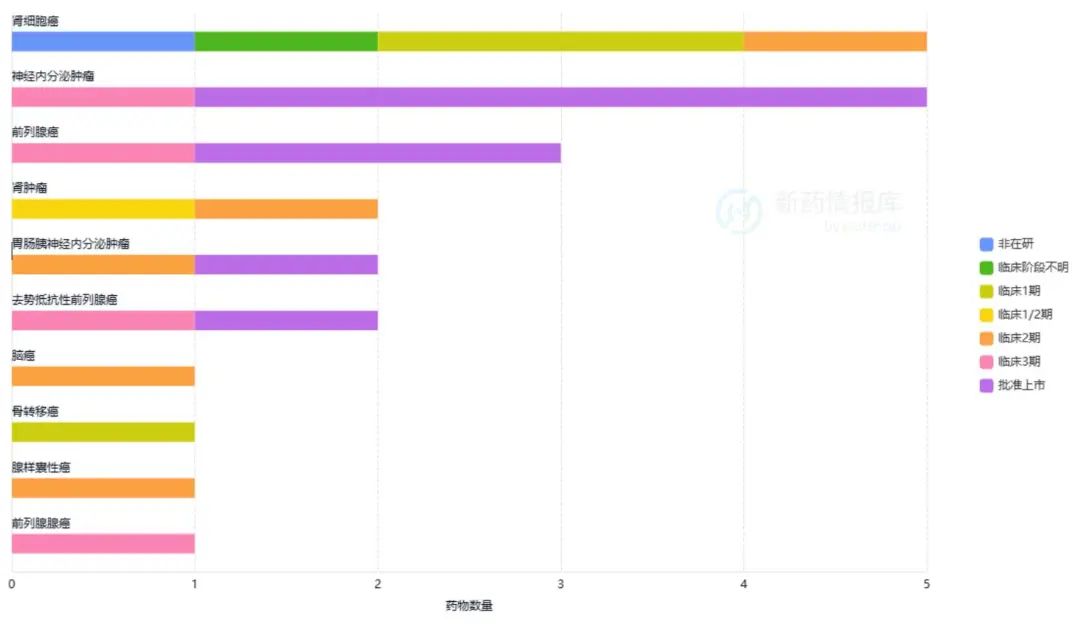
图片来源于全球新药竞争情报库
随着核医疗与核技术的创新和迭代,近年来RDC迎来了研发热潮,其突出特点还在于更换使用的放射性核素种类、可以发挥诊断或治疗等不同功能。在中国,政府对放射性药物研发的监管也在不断加强,为了指导国内放射性药物更好地研究,2020年、2021年以及2023年我国相继出台了3个技术指导原则,对体内诊断药物及体内治疗药物的临床对起到了指导作用,极大促进了放射性药物的发展。
相信在未来的几年或者十几年内,RDC药物研发和抗肿瘤治疗都会取得突破性的进展。这对肿瘤患者将是莫大的安慰,越来越好,并非说说而已。
参考文献:
[1]王雪,李倩,韦薇.浅析抗体偶联核素类产品药学研发和评价关注点[J].中国新药杂志,2023,32(02):143-147.
[2]江艳君,李晓阳,洪浩.核素药物在肿瘤细胞治疗中的应用研究进展[J].药学进展,2023,47(01):16-34.
[3]Gudkov S, Shilyagina N, Vodeneev V, et al. Targeted Radionuclide Therapy of Human Tumors[J]. International Journal of Molecular Sciences, 2015, 17(1): 33.


