替莫唑胺加入大剂量甲氨蝶呤/全脑放疗治疗初治PCNSL的3期研究失败
时间:2022-11-18 20:54:17 热度:37.1℃ 作者:网络
原发CNS淋巴瘤
原发性中枢神经系统淋巴瘤 (Primary central nervous system lymphoma,PCNSL) 是一种侵袭性、结外非霍奇金淋巴瘤,其标准方案先后包括全脑放射治疗 (WBRT)和大剂量甲氨蝶呤(HD-MTX)序贯 WBRT,中位生存时间可达33个月。然而,虽然 HD-MTX 序贯 WBRT 的初始完全缓解 (CR) 率较高,仍有超过50%的患者在诊断后的前两年内复发;并且由于神经毒性增加,30至40 Gy WBRT并不适合所有>60岁患者。
此外由于缺乏有效穿透血脑屏障 (BBB) 的药物和 PCNSL 的弥漫性浸润生长,化疗的治疗效果也有限,例如R-CHOP联合 WBRT的生存获益未优于WBRT,主要原因是BBB 阻碍了大多数药物(利妥昔单抗、多柔比星和长春新碱)的渗透。众所周知,即使在诱导化疗和 WBRT 完全缓解后,PCNSL的预后仍然较差,而延长缓解、延缓复发、维持肿瘤休眠的维持治疗也许可以改善 PCNSL 的疗效。
替莫唑胺 (TMZ) 是一种口服烷化剂,可穿透BBB且毒性中等,在新诊断和复发性PCNSL中具有一定疗效。因此埼玉医科大学病院Kazuhiko Mishima教授等假设,在 HD-MTX 和WBRT中纳入TMZ以及放疗后TMZ维持治疗可改善 PCNSL 的疾病控制,并开展了一项随机、III期研究(JCOG1114C),以检验该假设:在 HD-MTX 和 WBRT 标准治疗基础上加用TMZ伴随和维持化疗可改善新诊断 PCNSL 患者生存——然而结果令人失望。研究结果近日发表于《Neuro-Oncology》。

研究设计
本研究为随机、开放标签、III期研究,有日本30家医院参与,纳入首次登记的新诊断、非免疫功能低下的 PCNSL 患者。纳入标准包括:年龄20-70岁、经组织学证实的弥漫性大 B 细胞淋巴瘤、仅局限在 CNS 内的疾病(伴或不伴眼内淋巴瘤)、无淋巴瘤性脑膜炎、无大脑淋巴瘤病、术后3-35天进行肿瘤活检或切除、ECOG为0-2(如果是由于神经功能缺损,允许3分)、既往未针对任何癌症进行化疗或RT、器官功能良好等。
14天/周期,每周期第1天给予HD-MTX(3.5 g/m2,静脉输注3小时)共3个周期,MTX 后24小时给予充分补水、尿碱化和亚叶酸解救治疗。在第1和2周期 HD-MTX 给药后8-14天通过对比增强脑部 MRI 评估 HD-MTX 治疗反应,并在第3周期 MTX 给药后8-21天通过对比增强脑部MRI、CSF细胞学、裂隙灯检查(眼部受累患者必须进行)和皮质类固醇的使用评估 HD-MTX 治疗反应。采用国际 PCNSL 协作组缓解标准进行缓解评估。
接受至少1个周期 HD-MTX 治疗的患者,按1:1的比例随机分配接受 30 Gy 剂量WBRT(用于HD-MTX 治疗后无脑实质内肿瘤)或30 Gy剂量WBRT + 10 Gy局部加强(用于脑实质内肿瘤阳性)作为对照(a组),或WBRT± TMZ联合加强和TMZ 维持治疗两年作为试验治疗(B组)。TMZ 与 RT 同时连续给药,剂量为75 mg/m2,从 RT 第1天开始并在 RT 最后一天结束。放疗后4-5周开始 TMZ 维持治疗(100-200 mg/m2/天,第1-5天,每4周一次)2年(从 HD-MTX 开始计算)。
HD-MTX 治疗后无可见实质内肿瘤的患者接受15次2 Gy WBRT,WBRT 包括颈髓第一节段下缘和眼眶后2/3,眼部受累病例包括眼球进行照射。对于 HD-MTX 治疗后存在可见实质内肿瘤的患者,在肿瘤区域给予5次 2 Gy 的综合加强。
本研究的主要终点为OS,定义为从1:1随机化至全因死亡或末次联系存活患者的时间。次要终点为 HD-MTX 后有效率、放疗后有效率、HD-MTX后 CR 率、放疗后 CR 率、PFS、不良事件发生率、早期死亡发生率、治疗相关死亡发生率、4级非血液学不良事件发生率等。
研究结果
122例患者接受了随机化,其中62例和60例患者分别被分配至WBRT±局部加强放疗(A组)和WBRT±局部加强放疗联合TMZ + TMZ维持(B组),并分析了疗效和安全性。两组之间的基线特征平衡良好(表1)。
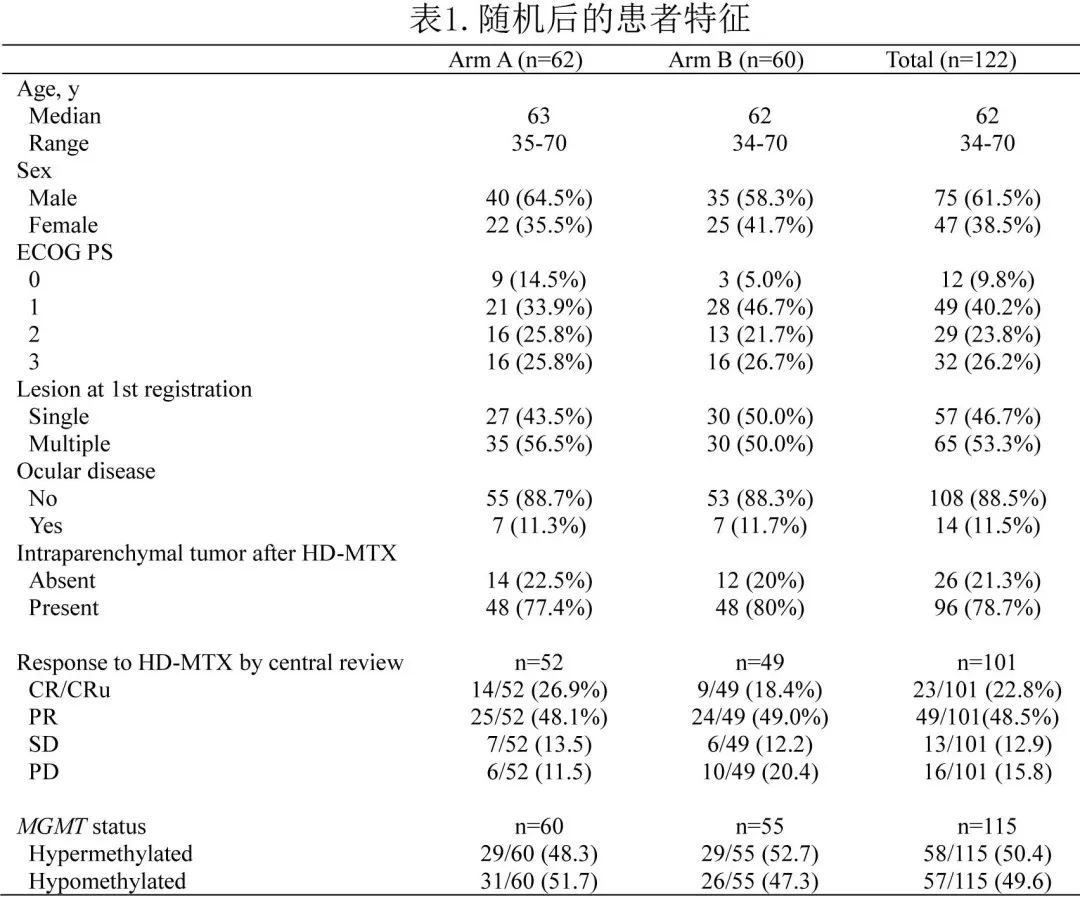
根据中心审查的缓解评估结果,HD-MTX治疗后,A组中14/52 (26.9%) 例患者达到 CR 或未确认的CR(CRu,定义为 MRI 显示微小残留肿瘤),比例高于 B 组 (9/49 [18.4%),而两组之间的 PR 和 SD 比例相似(PR:48.1% vs 49.0%,SD:13.5% vs 12.2%)。此外B 组中10/49(20.4%) 的患者PD,高于 A 组 (6/52[11.5%])。
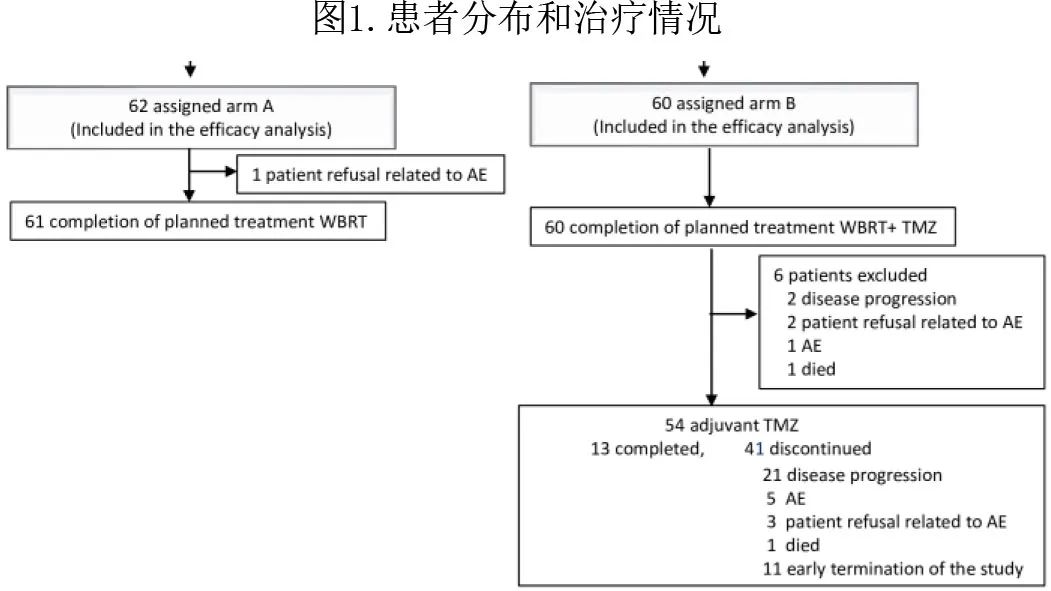
A 组1例患者在 WBRT 期间因拒绝而终止治疗,B组RT 联合 TMZ 治疗期间无患者终止方案治疗。6例患者未接受计划的TMZ维持治疗(图1),因此60例患者中有54例 (90%) 开始 TMZ 维持治疗。在维持治疗期,41例患者因不良事件(n=5)、疾病进展(n=21)、患者因不良事件拒绝(3例患者)、不明原因死亡(1例患者)和提前终止研究(11例患者)而终止治疗,仅13例患者完成了计划的两年维持治疗。TMZ 维持的中位周期数为14.5。
通过中心审查评估的 RT 缓解率:A组29/52例 (55.8%) 和 B 组17/49例 (55.1%) 达到CR/Cru,RT 后总缓解率 (CR/CRu +PR) 分别为96.2%和100%。
毒性
HD-MTX 治疗期间,133例患者中有69例 (51.9%) 发生3-4级不良事件,淋巴细胞减少是最常见的3-4级不良事件(22.6%)。其他常见的3-4级不良事件包括中性粒细胞减少(12例,9%)、白细胞减少(6例,4.5%)、ALT升高(17例,12.8%)、低钠血症(10例,7.5%)、低钾血症(6例,4.5%)和尿路感染(4例,3%)。
表2为RT 期间发生的不良事件。最常见的3-4级不良事件为淋巴细胞减少(B组18/60例 [30%] 和 A 组7/61例 [11.5%])。两组均未观察到 RT 期间不良事件导致的治疗终止。
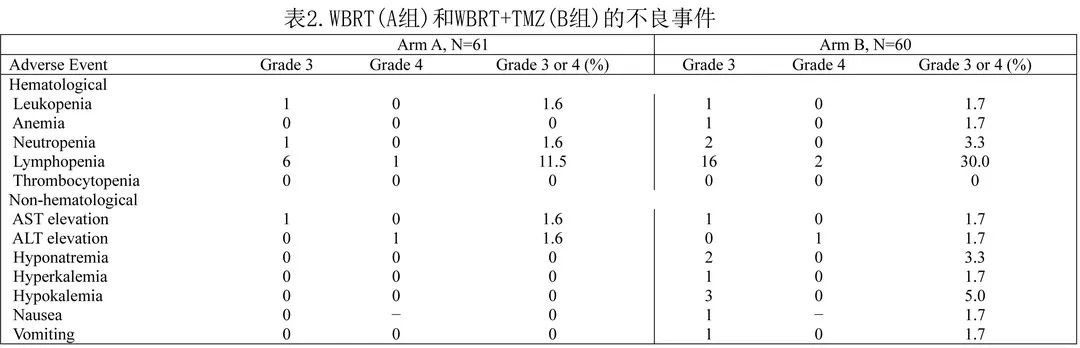
B 组维持阶段的不良事件,最常见的3-4级不良事件是淋巴细胞减少(24/54[44.4%])、疲乏(5/54[9.3%])、白细胞减少(4/54[7.4%])和中性粒细胞减少(2/54[3.7%])。TMZ联合RT 期间严重淋巴细胞减少的高发生率可能反映了 TMZ 与 WBRT 的联合治疗,而维持治疗期间重度淋巴细胞减少的高发生率可能反映了 TMZ 给药持续时间长。
疗效
2020年6月的中期分析中,中位随访1.64年,A 组患者的2年 OS 为86.8%, B 组患者为71.4%(HR= 2.18;P= 0.97)。因结果无效,根据预先规定的停止标准提前终止研究。A 组的中位 PFS 为2.6年,B组为1.8年(HR= 1.54)。
2021年11月中位随访3.5年的更新分析中共有122例患者,A组2年 OS 为86.7%,B 组为76.2%(图2A)。A 组的中位 PFS 为3.5年,B组为2.3年(图2B)。
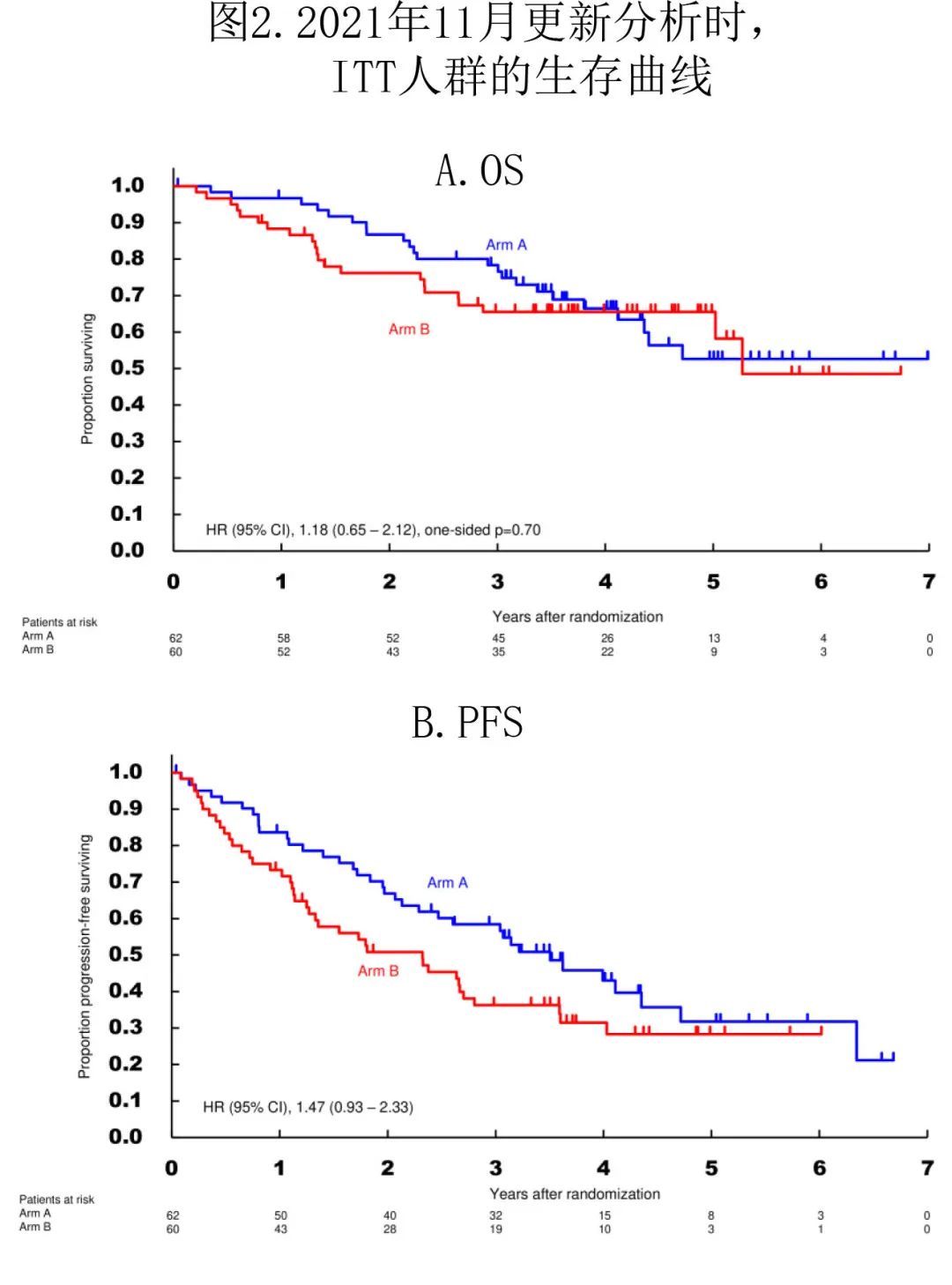
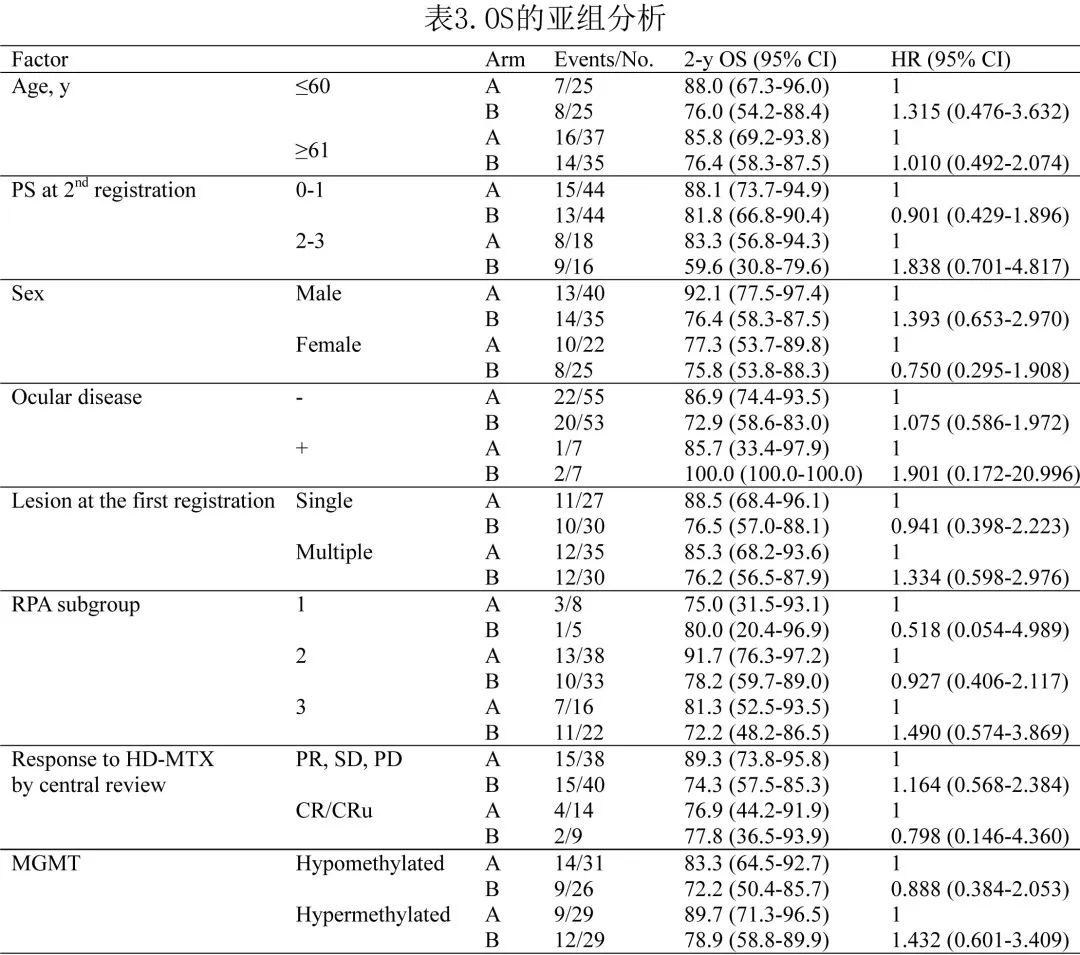
作者单独分析了HD-MTX 诱导后CR/CRu 患者的生存期(表3),结果A 组和 B 组中 CR/CRu 患者的 PFS 和 OS 完全相同。此外按性别(男性vs.女性)、年龄(≤60 vs.≥61岁)、HD-MTX治疗后残留增强肿瘤(无vs.有)和 MSKCC RPA 分类(1类vs. 2类vs. 3类)进行亚组分析和治疗组间 OS 比较,未发现获益于TMZ伴随和维持治疗的亚组(表3)。Kaplan-Meier曲线也显示 CR/CRu 患者的生存期无差异。
讨论
本研究是 HD-MTX 后 WBRT 联合/不联合放疗增强、联合TMZ作为伴随和维持治疗的首次随机试验,作者通过这项随机、III期研究作者证实,在 HD-MTX 和 WBRT 的标准治疗基础上加用TMZ伴随和维持治疗未改善新诊断 PCNSL 患者的 OS 和PFS。鉴于 TMZ 治疗组缺乏临床获益,本研究中所有仍接受方案规定治疗的患者均停用TMZ——但事实上这一结果并不在预期之中。
既往报道认为,PCNSL患者在HD-MTX、利妥昔单抗和 TMZ 诱导化疗后 WBRT 和照射后10个月TMZ维持治疗可延长2年 PFS 和OS。由于 TMZ 已被用于临床试验,并被认为是 PCNSL 治疗开发的重要药物,而本研究发现 TMZ 在 PCNSL 的巩固和维持治疗中无效,这既令人失望又耐人寻味。
对这些非预期结果可提出几种解释。首先,生存结局差异的最可能原因可能是 TMZ 治疗相关不良事件,如重度淋巴细胞减少:在WBRT +伴随 TMZ 治疗期间,30%的患者观察到3-4级淋巴细胞减少,在维持 TMZ 治疗期间,44.4%的患者观察到3-4级淋巴细胞减少。淋巴细胞减少可能是癌症患者宿主免疫受损的生物标志物,因为研究显示低绝对淋巴细胞计数降低与淋巴瘤和其他癌症患者的不良预后相关;尽管尚不清楚 PCNSL 患者中淋巴细胞减少与 OS 和 PFS 较差结局相关的潜在机制和原因,但淋巴细胞减少可能与细胞因子生成不足相关,细胞因子刺激趋化因子生成,导致抗肿瘤免疫降低。第二个可能的原因可能是诱导 HD-MTX 后组间 CR 率不平衡(A组 CR 率26.9%高于 B 组18.4%)。但这是一个弱假设,因为在 HD-MTX 治疗后 CR 患者亚组中未证实 TMZ 的显著累加效应。
参考文献
Kazuhiko Mishima,et al.Randomized phase III study of high-dose methotrexate and whole-brain radiotherapy with/without temozolomide for newly diagnosed primary CNS lymphoma: JCOG1114C.Neuro Oncol . 2022 Nov 5;noac246. doi: 10.1093/neuonc/noac246.
: , 。 视频 小程序 赞 ,轻点两下取消赞 在看 ,轻点两下取消在看


